خون رسانی مختل شده است. پرخونی وریدی عمومی مزمن. مورفوژنز ترومبوز توسط مسیر خارجی
تصور فعالیت حیاتی طبیعی بدن بدون عملکرد طبیعی اندام های گردش خون و گردش لنفاوی که در وحدت ساختاری و عملکردی نزدیک هستند دشوار است.
کار سیستم گردش خون، اول از همه، خود را تعیین می کند سطح فرآیند متابولیسم در هر بافت و هر اندامی که برای انجام یک عملکرد تخصصی لازم است. این تابع تبادل حمل و نقلسیستم گردش خون در ارتباط با سیستم تخلیه لنفاوی و سیستم خون عمل می کند. از این نتیجه می شود که در جریان میکروسیرکولاسیون، که با کمک آن تبادل بین مویرگ انجام می شود، سیستم گردش خون و لنفاوی، مانند خون، یک وظیفه و عملکرد را با هم انجام می دهند.
مفهوم "ریز گردش" تعدادی از فرآیندها را در بر می گیرد، در درجه اول مانند الگوهای گردش خون و لنف در رگ های کوچک، الگوهای رفتار سلول های خونی (تغییر شکل، تجمع، چسبندگی)، مکانیسم های انعقاد خون، و مهمتر از همه، مکانیسم های متابولیسم ترانس مویرگی با انجام تبادل ترانس مویرگ، میکروسیرکولاسیون هموستاز بافت را فراهم می کند.
سیستم گردش خون، اندامها و سیستمهای مختلف عملکردی را به نفع بدن بهعنوان یک کل هماهنگ میکند و به هم پیوند میدهد. این عملکرد هماهنگ کننده هموستازسیستم گردش خون با کمک سیستم لنفاوی تخلیه می شود. عملکرد سیستم گردش خون، مانند سیستم لنفاوی، توسط مکانیسم های تنظیم عصبی-هومورال (دستگاه های عصبی قلب، گیرنده های عروق خونی، مرکز وازوموتور، ثابت های هومورال خون، لنف، منقبض کننده های عروق و گشادکننده عروق و غیره) تامین می شود. اما سیستم گردش خون، مانند سیستم لنفاوی، نه تنها از نظر عملکردی، بلکه از نظر ساختاری نیز در یک کل واحد ترکیب شده است: قلب منبع جریان خون است، رگ ها منبع توزیع خون و جمع آوری لنف هستند، عروق میکروسکولار سکوی پرشی است. برای متابولیسم ترانس مویرگ و متابولیسم بافتی. با این حال، یکپارچگی ساختاری و عملکردی هر دو سیستم گردش خون و لنفاوی، اصالت ساختاری و ویژگی های عملکردی این سیستم ها را در اندام ها و بافت های مختلف رد نمی کند.
بر اساس بررسی اجمالی ارائه شده، می توان تعدادی از مقررات اساسی را در مورد اختلالات گردش خون و لنف بیان کرد. اول، اختلالات گردش خون را نمی توان جدا از اختلالات گردش لنفاوی و وضعیت سیستم خون در نظر گرفت، زیرا این سیستم ها از نظر ساختاری و عملکردی نزدیک به هم مرتبط هستند. ثانیاً
اختلالات گردش خون و لنف منجر به اختلال در متابولیسم بافت (سلولی) می شود که به معنای آسیب به ساختار بافت (سلول ها)، ایجاد یک یا نوع دیگری از دیستروفی یا نکروز است. مورفولوژی این ضایعات، علاوه بر ویژگی های مشترک، ذاتی در همه اندام ها و بافت ها، دارای تعدادی ویژگی است که فقط برای یک اندام یا بافت مشخص است که با ویژگی های ساختاری و عملکردی آنها و به ویژه با ویژگی های سیستم گردش خون و لنفاوی تعیین می شود.
اختلالات گردش خون و لنف نه تنها در نتیجه اختلالات سیستم گردش خون و لنفاوی، بلکه همچنین تنظیم عصبی-هومورال قلب، تجزیه ساختاری در هر سطح - قلب، عروق خونی، عروق ریز، عروق لنفاوی، مجرای قفسه سینه رخ می دهد. با اختلال در تنظیم فعالیت قلب، توسعه در آن فرآیند پاتولوژیکشایع است، و با اختلال در تنظیم عملکرد بستر عروقی در یک منطقه خاص، و همچنین کف ساختاری آن، - محلی اختلالات گردش خون و لنف. اختلالات گردش خون موضعی (مانند خونریزی مغزی) می تواند باعث شود تخلفات عمومی... عمومی و تخلفات محلیگردش خون و لنف در بسیاری از بیماری ها مشاهده می شود، آنها می توانند روند خود را پیچیده کنند و منجر به عواقب خطرناکی شوند.
اختلالات گردش خون
اختلالات گردش خون را می توان به 3 گروه تقسیم کرد: 1) اختلالات گردش خون، که با مجموعه ای (شریانی یا وریدی) و کم خونی نشان داده می شود. 2) نقض نفوذپذیری دیواره عروقی که شامل خونریزی (خونریزی) و پلاسموراژ می شود. 3) اختلال در جریان و حالت (یعنی رئولوژی) خون به صورت استاز، پدیده لجن، ترومبوز و آمبولی.
بسیاری از انواع اختلالات گردش خون از نظر بیماری زایی بسیار مرتبط هستند و با هم رابطه علّی دارند، به عنوان مثال، رابطه خونریزی، پلاسموراژ و ادم با پلتورا، ارتباط کم خونی با آمبولی و ترومبوز، و دومی با استاز و پلتورای وریدی. اختلالات گردش خون زمینه ساز بسیاری از سندرم های بالینی مانند تیزو نارسایی مزمن قلب (قلبی عروقی)، انعقاد داخل عروقی منتشر (انعقاد داخل عروقی منتشر)، سندرم ترومبوآمبولیک.آنها در هسته هستند شوکه شدن.
در جنین، نوزاد و کودک 3 سال اول زندگی، توده عمومی و موضعی، کم خونی، خونریزی، استاز راحت تر و بیشتر از بزرگسالان رخ می دهد که به نابالغی مکانیسم های تنظیمی گردش خون بستگی دارد. ترومبوز و حمله قلبی در کودکان بسیار کمتر از بزرگسالان است. این اختلالات گردش خون عمدتاً در ارتباط با ناهنجاری سیستم قلبی عروقی، اضافه شدن یک عفونت سپتیک ثانویه به آنها یا در برخی بیماری های عفونی حاد (دیفتری، میوکاردیت ویروسی و غیره) رخ می دهد.
مقدار زیاد
احتقان (هیپرمی)می تواند شریانی و وریدی باشد.
مجموعه شریانی
مجموعه شریانی- افزایش خون رسانی به اندام، بافت به دلیل افزایش جریان ورودی خون شریانی... ممکن است داشته باشد عمومی شخصیت، که با افزایش حجم خون در گردش یا تعداد گلبول های قرمز مشاهده می شود. در چنین مواردی، رنگ قرمز مشخص می شود. پوستو غشاهای مخاطی و افزایش یافته است فشار خون... بیشتر اوقات پرخونی شریانی دارد محلی شخصیت و از دلایل مختلفی ناشی می شود.
تمیز دادن فیزیولوژیکی پرخونی شریانی که تحت تأثیر دوزهای کافی از عوامل فیزیکی و شیمیایی، همراه با احساس شرم و خشم (پرخونی رفلکس)، با افزایش عملکرد اندام ها (پرخونی کاری) و آسیب شناسی پرخونی شریانی
بر اساس ویژگی های علت و مکانیسم توسعه، انواع زیر متمایز می شوند هیپرمی شریانی پاتولوژیک: آنژینوروتیک (نورپرالیتیک)؛ وثیقه؛ پرخونی پس از کم خونی (پس از کم خونی)؛ خالی التهابی؛ پرخونی ناشی از فیستول شریانی وریدی.
پرخونی آنژیونورتیک (نورپرالیتیک).در نتیجه تحریک اعصاب گشادکننده عروق یا فلج اعصاب منقبض کننده عروق مشاهده می شود. پوست، غشاهای مخاطی قرمز، کمی متورم، در لمس گرم یا داغ می شوند. این نوع پرخونی می تواند در قسمت های خاصی از بدن با نقض عصب، روی پوست و غشاهای مخاطی صورت با برخی عفونت ها، همراه با آسیب به گره های سمپاتیک رخ دهد. سیستم عصبی... معمولا این پرخونی به سرعت از بین می رود و اثری از خود باقی نمی گذارد.
پرخونی جانبیدر ارتباط با انسداد جریان خون در امتداد تنه شریانی اصلی که توسط ترومبوس یا آمبولی بسته شده است، ایجاد می شود. در این موارد، خون از رگ های جانبی عبور می کند. لومن آنها بطور انعکاسی منبسط می شود، جریان خون شریانی افزایش می یابد و بافت مقدار بیشتری خون دریافت می کند.
هیپرمی بعد از کم خونی(پوستانمی) در مواردی ایجاد می شود که عاملی که منجر به فشردگی شریان می شود (تومور، تجمع مایع در حفره، لیگاتور و غیره) و کم خونی بافتی به سرعت از بین می رود. در این موارد، رگهای بافتی که قبلاً تخلیه شدهاند، به شدت منبسط میشوند و از خون سرریز میشوند، که میتواند نه تنها منجر به پارگی و خونریزی شود، بلکه به دلیل توزیع مجدد شدید خون، منجر به کمخونی سایر اندامها مانند مغز نیز میشود. بنابراین، دستکاری هایی مانند برداشتن مایع از حفره های بدن، از بین بردن تومورهای بزرگ، برداشتن یک تورنیکت الاستیک به آرامی انجام می شود.
پرخونی واکاتنی(از لات خلاء- خالی) به دلیل کاهش فشار هوا ایجاد می شود. می توان آن را به اشتراک گذاشت، در-
نمونه ای در غواصان و کارگران کیسون در هنگام صعود سریع از ناحیه ای با فشار زیاد. پرخونی حاصل با آمبولی گاز، ترومبوز عروقی و خونریزی همراه است.
محلیپرخونی خالی تحت تأثیر، به عنوان مثال، قوطی های پزشکی، که فضای کمیاب را در یک منطقه خاص ایجاد می کنند، روی پوست ظاهر می شود.
پرخونی التهابی- همراه ثابت التهاب (نگاه کنید به. التهاب).
هیپرمی ناشی از فیستول شریانی وریدیدر مواردی بوجود می آید که مثلاً وقتی زخم گلولهیا آسیب دیگر، آناستوموز بین شریان و سیاهرگ ایجاد می شود و خون شریانی به داخل ورید می رود.
معنی هیپرمی شریانی پاتولوژیک عمدتاً بر اساس نوع آن تعیین می شود. برای مثال، پرخونی جانبی، اساساً جبرانی است و گردش خون را پس از بسته شدن تنه شریانی فراهم می کند. پرخونی التهابی جزء ضروری این واکنش محافظ و تطبیقی است. با این حال، پرخونی خالی به یکی از اجزای بیماری رفع فشار تبدیل می شود.
احتقان وریدی
احتقان وریدی- افزایش خون رسانی به اندام یا بافت به دلیل کاهش (مشکل) در خروج خون. جریان خون تغییر یا کاهش نمی یابد. رکود خون وریدی (هیپرمی احتقانی)منجر به گسترش وریدها و مویرگ ها می شود (شکل 53)، کاهش جریان خون در آنها، که با ایجاد هیپوکسی، افزایش نفوذپذیری غشای پایه مویرگ ها همراه است.
احتقان وریدی می تواند عمومی و موضعی باشد.
احتقان وریدی عمومی
احتقان وریدی عمومیدر آسیب شناسی قلبی ایجاد می شود که منجر به نارسایی حاد یا مزمن قلبی (قلبی عروقی) می شود. می تواند حاد یا مزمن باشد.
برنج. 53.احتقان وریدی. مویرگ ها و سیاهرگ های ریه گشاد شده و پر از خون هستند
در احتقان عمومی حاد وریدی،که تظاهر این سندرم است نارسایی حاد قلبی(ناکافی بودن انقباض میوکارد، به عنوان مثال، با انفارکتوس میوکارد، میوکاردیت حاد)، در نتیجه آسیب هیپوکسیک به موانع هیستوهماتوژن و افزایش شدید نفوذپذیری مویرگی در بافت ها، خیساندن پلاسما (پلاسموراژی) و ادم، استاز در مویرگ ها. و خونریزی های متعدد با ماهیت دیاپدتیک در بافت ها تغییرات دیستروفیک و نکروز ظاهر می شود. ویژگی های ساختاری و عملکردی اندامی که در آن استاز حاد وریدی ایجاد می شود، غالب تغییرات ادماتوز-پلاسموراژیک، هموراژیک یا دیستروفیک و نکروزیک را تعیین می کند. ترکیبی از آنها نیز امکان پذیر است. در ریه ها، ویژگی های هیستوفیزیولوژیکی سد هوا-خونی، توسعه ادم و خونریزی را در استاز حاد وریدی توضیح می دهد. در کلیه ها، به دلیل ویژگی های ساختار نفرون و گردش خون، تغییرات عمدتا دیستروفیک و نکروز، به ویژه اپیتلیوم لوله ها رخ می دهد. در کبد، در ارتباط با ویژگی های معماری لوبول کبدی و گردش خون آن در توده حاد، خونریزی های مرکز لوبولار و نکروز ظاهر می شود.
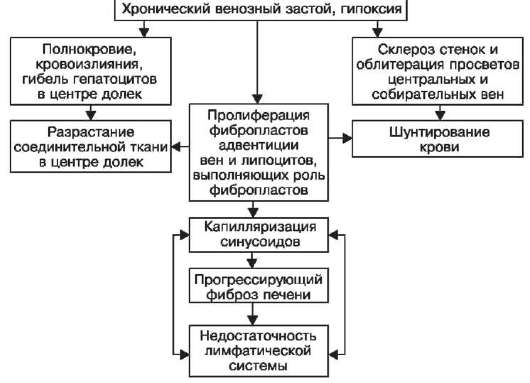
احتقان وریدی عمومی مزمنبا سندرم ایجاد می شود نارسایی مزمن قلبی (قلبی عروقی)،بسیاری از بیماری های مزمن قلبی (نقص، بیماری عروق کرونر قلب، میوکاردیت مزمن، کاردیومیوپاتی، فیبروالاستوز اندوکارد و غیره) را پیچیده می کند. منجر به تغییرات شدید و اغلب غیرقابل برگشت در اندام ها و بافت ها می شود. با حفظ وضعیت هیپوکسی بافتی برای مدت طولانی، نه تنها ایجاد پلاسموراژ، ادم، استاز و خونریزی، دیستروفی و نکروز را تعیین می کند. آتروفیکو تغییرات اسکلروتیکتغییرات اسکلروتیک، به عنوان مثال. رشد بیش از حد بافت همبند، با این واقعیت مرتبط هستند که هیپوکسی مزمن سنتز کلاژن را توسط فیبروبلاست ها و سلول های فیبروبلاست مانند تحریک می کند. بافت همبند عناصر پارانشیمی را جابجا می کند، توسعه می یابد پایداری راکد (استقامت)اندام ها و بافت ها دایره باطل در احتقان وریدی مزمن با توسعه بسته می شود مویرگی - پارانشیمیبلوک به دلیل "ضخیم شدن" غشای پایه اندوتلیوم و اپیتلیوم به دلیل افزایش تولید کلاژن توسط فیبروبلاست ها، سلول های ماهیچه صاف و لیپوفیبروبلاست ها.
تغییرات اندام با استاز وریدی مزمن، علیرغم تعدادی از ویژگی های مشترک(استقامت راکد)، دارای تعدادی ویژگی است.
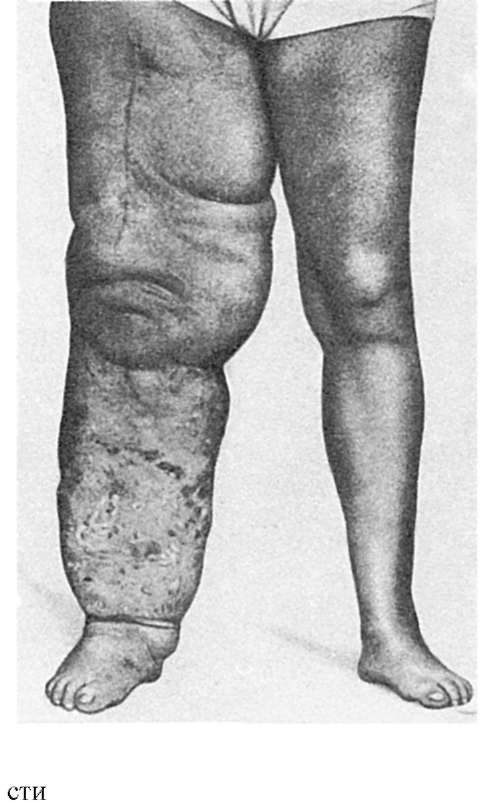
پوست به خصوص اندام تحتانی سرد می شود و به رنگ آبی متمایل می شود (سیانوز).وریدهای پوست و بافت زیر جلدیبزرگ شده، پر از خون؛ همچنین عروق لنفاوی گشاد شده و پر از لنف است. ادم بیان شده درم و بافت زیر جلدی، تکثیر بافت همبند در پوست. در ارتباط با احتقان وریدی، ادم و اسکلروز، التهاب و زخم به راحتی در پوست ایجاد می شود که برای مدت طولانی بهبود نمی یابد.
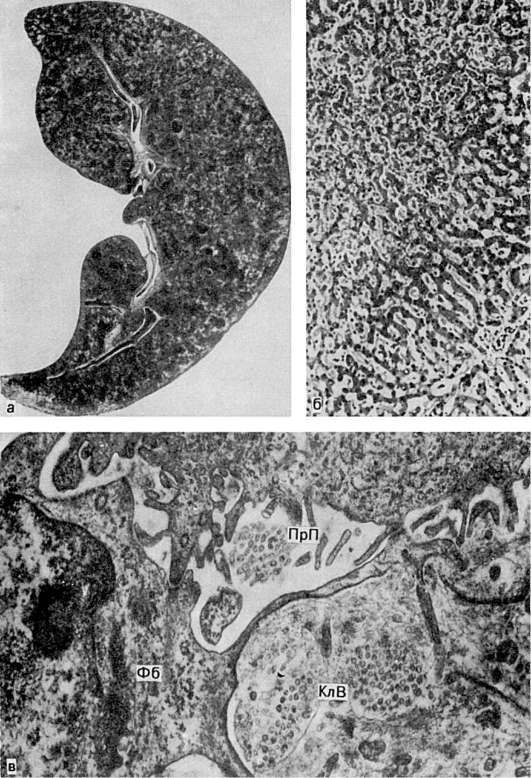
کبد در استاز وریدی مزمن بزرگ، متراکم، لبه های آن گرد، سطح برش رنگارنگ، خاکستری مایل به زرد با لکه های قرمز تیره و شبیه جوز هندی است، بنابراین چنین کبدی نامیده می شود. جوز هندی(شکل 54).
در می توان مشاهده کرد که تنها قسمت های مرکزی لوبول ها خون کامل هستند، جایی که سلول های کبدی از بین می روند (شکل 54 را ببینید). این بخش ها به رنگ قرمز تیره در برش کبد به نظر می رسند. در حاشیه لوبول ها، سلول های کبدی در حالت دیستروفی، اغلب چرب هستند، که رنگ خاکستری مایل به زرد بافت کبد را توضیح می دهد.
مورفوژنز تغییرات کبد در طول استاز وریدی طولانی مدت پیچیده است (طرح VI). مجموعه انتخابی مرکز لوبول ها به این دلیل است که رکود کبد در درجه اول وریدهای کبدی را می پوشاند و به رگ های جمعی و وریدهای مرکزیو سپس روی سینوسی ها. دومی گسترش می یابد، اما فقط در بخش مرکزی و میانی لوبول، جایی که آنها با مقاومت از شاخه های مویرگی شریان کبدی که به داخل سینوس ها جریان می یابد، مواجه می شوند، که فشار در آن بیشتر از سینوسوئیدها است. با افزایش تعداد زیادی در مرکز لوبول ها، خونریزی ظاهر می شود، سلول های کبدی در اینجا دچار دیستروفی، نکروز و آتروفی می شوند. هپاتوسیت های حاشیه لوبول ها هیپرتروفی جبرانی می شوند و شبیه سلول های مرکز لوبولار می شوند. تکثیر بافت همبند در ناحیه خونریزی و مرگ سلول های کبدی با تکثیر سلول های سینوسی - لیپوسیت ها که می توانند به عنوان فیبروبلاست عمل کنند (نگاه کنید به شکل 54) و در نزدیکی وریدهای مرکزی و جمع کننده - با تکثیر همراه است. فیبروبلاست های adventitia این وریدها. در نتیجه تکثیر بافت همبند در سینوسی ها، یک غشای پایه پیوسته ظاهر می شود (در کبد طبیعی وجود ندارد)، یعنی. در جریان مویرگ شدن سینوسی ها،ناشی می شود مویرگی - پارانشیمیبلوک، که با تشدید هیپوکسی، منجر به پیشرفت تغییرات آتروفیک و اسکلروتیک در کبد می شود. این امر همچنین با شنت خون، که با اسکلروز دیواره ها و انسداد مجرای بسیاری از وریدهای مرکزی و جمع کننده، و همچنین افزایش رکود لنف ایجاد می شود، تسهیل می کند. در نهایی توسعه می یابد فیبروز احتقانی (اسکلروز) کبد.
با تکثیر تدریجی بافت همبند، بازسازی ناقص سلول های کبدی با تشکیل گره های بازسازی، بازسازی و تغییر شکل اندام ظاهر می شود. در حال توسعه است سیروز کبدی راکد (جوز هندی)،که به آن نیز گفته می شود از صمیم قلب،همانطور که معمولا در نارسایی مزمن قلبی رخ می دهد.
V ریه ها با توده وریدی مزمن، دو نوع تغییر ایجاد می شود - خونریزی های متعدد، باعث ایجاد هموسیدروز ریه،و تکثیر بافت همبند، یعنی. اسکلروزریه ها بزرگ، قهوه ای و متراکم می شوند - سفتی قهوه ای ریه ها(شکل 55).
V مورفوژنز تراکم قهوهای ریهها، نقش اصلی را توده احتقانی و فشار خون بالا در گردش خون ریوی ایفا میکند که منجر به هیپوکسی و افزایش نفوذپذیری عروق، ادم، خونریزی دیاپدتیک میشود (طرح VII). توسعه این تغییرات
 برنج. 54.جگر جوز هندی:
برنج. 54.جگر جوز هندی:
الف - نمای مقطعی؛ ب - در مرکز لوبول کبدی (بالا سمت چپ)، سینوس ها به شدت منبسط شده و خون کامل هستند، سلول های کبدی از بین می روند. در حاشیه لوبول (پایین سمت راست) آنها حفظ می شوند (تصویر میکروسکوپی). ج - در فضای پری سینوسی (PrP) فیبروبلاست ها (Fb) و رشته های کلاژن (CLV) (الکترونوگرام). x27000
طرح ششممورفوژنز فیبروز احتقانی کبد
 برنج. 55.انجماد قهوه ای ریه ها:
برنج. 55.انجماد قهوه ای ریه ها:
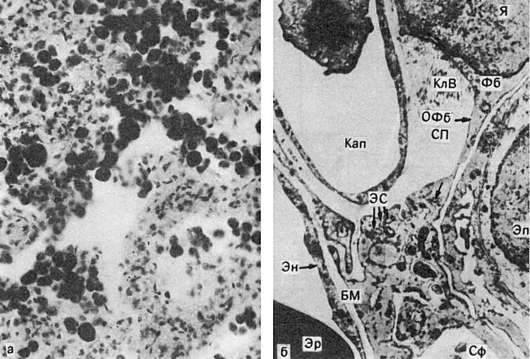
الف - سیدروبلاست ها و سیدروفاژها در لومن آلوئول های ریوی، اسکلروز سپتوم آلوئولار (تصویر میکروسکوپی). ب - در فضای سپتوم بزرگ شده (SP) سیدروفاژ (Sph) و فیبروبلاست فعال (Fb) که سیتوپلاسم آن فرآیند طولانی (OFB) را تشکیل می دهد و حاوی بسیاری از لوله های شبکه آندوپلاسمی دانه ای (ES)، ریبوزوم های آزاد است. فیبرهای کلاژن (CLF) در نزدیکی بدن فیبروبلاست قابل مشاهده هستند. کلاهک - مویرگی؛ BM - غشای پایه؛ En - اندوتلیوم؛ Ep - اپیتلیوم آلوئولار؛ Er - گلبول قرمز، I - هسته. الکترونوگرام. x12 500
طرح VII.مورفوژنز تراکم قهوه ای ریه ها
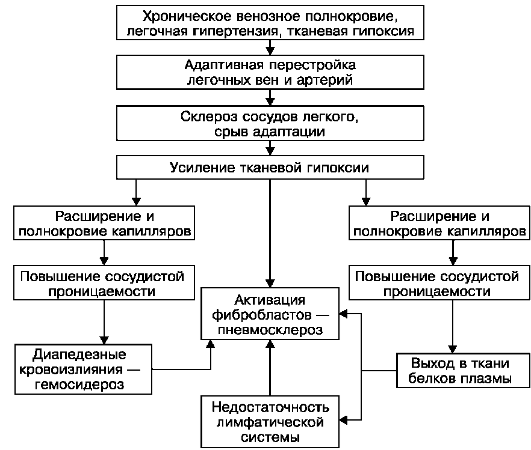 قبل از تعدادی از فرآیندهای تطبیقی در بستر عروقی ریه ها. در پاسخ به فشار خون بالا در گردش خون ریوی، هیپرتروفی ساختارهای عضلانی-الاستیک شاخه های کوچک ورید و شریان ریوی با تغییر ساختار عروق بر اساس نوع بسته شدن شریان ها رخ می دهد که مویرگ های ریه را از ناگهانی محافظت می کند. سرریز خون با گذشت زمان، تغییرات تطبیقی در رگ های ریه با تغییرات اسکلروتیک جایگزین می شود، جبران خسارت ایجاد می شود. گردش خون ریوی، سرریز خون مویرگ های سپتوم بین آلوئولار. هیپوکسی بافت افزایش می یابد، و بنابراین نفوذپذیری عروق افزایش می یابد، خونریزی های دیاپدی متعدد رخ می دهد. در آلوئول ها، برونش ها، سپتوم های بین آلوئولار، عروق لنفاوی و گره های ریه، خوشه هایی از سلول های مملو از هموسیدرین - سیدروبلاست ها و سیدروفاژها (نگاه کنید به شکل 55) و هموسیدرین آزاد ظاهر می شوند. ناشی می شود هموسیدروز ریوی منتشرهموسیدرین و پروتئینهای پلاسما (فیبرین) استروما و تخلیه لنفاوی ریهها را مسدود میکنند، که منجر به نارسایی جذب سیستم لنفاوی آنها میشود که با سیستم مکانیکی جایگزین میشود. اسکلروز رگ های خونی و نارسایی سیستم لنفاوی هیپوکسی ریوی را افزایش می دهد که باعث تکثیر فیبروبلاست، ضخیم شدن سپتوم بین آلوئولار می شود (شکل 55 را ببینید). ناشی می شود مویرگی
قبل از تعدادی از فرآیندهای تطبیقی در بستر عروقی ریه ها. در پاسخ به فشار خون بالا در گردش خون ریوی، هیپرتروفی ساختارهای عضلانی-الاستیک شاخه های کوچک ورید و شریان ریوی با تغییر ساختار عروق بر اساس نوع بسته شدن شریان ها رخ می دهد که مویرگ های ریه را از ناگهانی محافظت می کند. سرریز خون با گذشت زمان، تغییرات تطبیقی در رگ های ریه با تغییرات اسکلروتیک جایگزین می شود، جبران خسارت ایجاد می شود. گردش خون ریوی، سرریز خون مویرگ های سپتوم بین آلوئولار. هیپوکسی بافت افزایش می یابد، و بنابراین نفوذپذیری عروق افزایش می یابد، خونریزی های دیاپدی متعدد رخ می دهد. در آلوئول ها، برونش ها، سپتوم های بین آلوئولار، عروق لنفاوی و گره های ریه، خوشه هایی از سلول های مملو از هموسیدرین - سیدروبلاست ها و سیدروفاژها (نگاه کنید به شکل 55) و هموسیدرین آزاد ظاهر می شوند. ناشی می شود هموسیدروز ریوی منتشرهموسیدرین و پروتئینهای پلاسما (فیبرین) استروما و تخلیه لنفاوی ریهها را مسدود میکنند، که منجر به نارسایی جذب سیستم لنفاوی آنها میشود که با سیستم مکانیکی جایگزین میشود. اسکلروز رگ های خونی و نارسایی سیستم لنفاوی هیپوکسی ریوی را افزایش می دهد که باعث تکثیر فیبروبلاست، ضخیم شدن سپتوم بین آلوئولار می شود (شکل 55 را ببینید). ناشی می شود مویرگی
بلوک پارانشیمی،یک دور باطل بسته شدن در مورفوژنز سفتی ریه ایجاد می شود اسکلروز احتقانیریه ها در قسمتهای پایینتر ریهها، جایی که استاز وریدی بارزتر است و تجمع رنگدانههای خون و فیبرین بیشتر است، بیشتر است. پنوموسکلروز مانند هموسیدروزیس با فشردگی قهوه ای رنگ ریه ها دارای توزیع دمی اپیکال است و به درجه و مدت احتقان وریدی در ریه ها بستگی دارد.
وجود دارد سفتی قهوه ای ایدیوپاتیک ریه ها(هموسیدروز ریوی ایدیوپاتیک یا ضروری؛ کم خونی فروکش کننده پنومو هموراژیک؛ سندرم سلن گلرستد). این بیماری نادر است، عمدتا در کودکان 3 تا 8 ساله. مورفوژنز هموسیدروز ضروری ریه ها اساساً با آنچه برای تراکم قهوه ای ثانویه ریه ها توصیف شده است، تفاوت ندارد. با این حال، هموسیدروز بارزتر است و اغلب با خونریزی های متعدد همراه است. علت این بیماری عدم توسعه اولیه قاب الاستیک عروق ریوی در نظر گرفته می شود که در نتیجه آنوریسم های عروقی، استاز خون و خونریزی های دیاپدی در ریه ها رخ می دهد. نقش عفونتها و مسمومیتها، آلرژیها و خودایمنیسازی را رد نکنید.
کلیه با استاز وریدی عمومی مزمن، آنها بزرگ، متراکم و سیانوتیک می شوند - سفتی سیانوتیک کلیه هاسیاهرگ های مدولا و ناحیه مرزی به خصوص پر خون هستند. در برابر پس زمینه استاز وریدی، لنفوستاز ایجاد می شود. در شرایط افزایش هیپوکسی، دیستروفی نفروسیت های بخش های اصلی نفرون و اسکلروز رخ می دهد، که با این حال، تلفظ نمی شود.
احتقان وریدی مزمن در طحال نیز به او منتهی می شود استحکام سیانوتیکبزرگ شده، متراکم، رنگ گیلاسی تیره، آتروفی فولیکولی و اسکلروز پالپ مشخص می شود. با استاز وریدی مزمن عمومی، سفتی سیانوتیک مشخصه سایر اندام ها نیز می باشد.
احتقان وریدی موضعی
توده وریدی موضعی زمانی مشاهده می شود که خروج خون وریدی از یک اندام خاص یا قسمتی از بدن به دلیل بسته شدن مجرای سیاهرگ (ترومبوس، آمبولی) یا فشار دادن آن از خارج (تومور، بافت همبند در حال رشد) مسدود شود. . بنابراین، یک مجموعه وریدی تیز دستگاه گوارش با ترومبوز ورید پورتال ایجاد می شود. کبد جوز هندی و سیروز کبدی جوز هندینه تنها با توده وریدی عمومی، بلکه با التهاب وریدهای کبدی و ترومبوز مجرای آنها (ترومبوفلبیت محو کننده وریدهای کبدی) که مشخصه بیماری Budd-Chiari (سندرم) است نیز یافت می شود. دلیل استحکام سیانوتیکممکن است ترومبوز سیاهرگ کلیوی ایجاد شود. احتقان وریدی و ادم اندام ها همچنین اگر گردش خون جانبی کافی نباشد منجر به ترومبوز وریدی می شود.
احتقان وریدی موضعی نیز می تواند در نتیجه توسعه رخ دهد وثیقه های وریدیدر صورت مشکل یا توقف جریان خون در امتداد بزرگراه های وریدی اصلی (به عنوان مثال، آناستوموز پورتوکاوال با مشکل در خروج خون از طریق سیاهرگ باب). رگهای جانبی سرریز از خون به شدت گسترش می یابد و دیواره آنها
نازک شدن، که می تواند باعث خونریزی خطرناک شود (به عنوان مثال، از وریدهای گشاد شده و نازک مری همراه با سیروز کبدی).
توده وریدی نه تنها با بروز تغییرات هموراژیک، دیستروفیک، آتروفیک و اسکلروتیک پلاسما همراه است، بلکه حملات قلبی وریدی (احتقانی).
کم خونی
کم خونییا ایسکمی(از یونانی. ischo- به تأخیر انداختن)، به کاهش خون رسانی به بافت، اندام، بخشی از بدن در نتیجه جریان ناکافی خون گفته می شود. ما هم در مورد پر شدن خون ناکافی و هم در مورد تخلیه کامل صحبت می کنیم.
کم خونی عمومی یا کم خونییک بیماری سیستم خونساز است و با محتوای ناکافی گلبول های قرمز و هموگلوبین مشخص می شود. کم خونی).کم خونی ربطی به اختلالات گردش خون ندارد.
تغییرات بافتی که در طول کم خونی رخ می دهد در نهایت با هیپوکسی یا آنوکسی همراه است، به عنوان مثال. گرسنگی اکسیژن... بسته به علت ایجاد کم خونی، لحظه شروع ناگهانی آن، مدت زمان هیپوکسی و میزان حساسیت بافتی به آن، با کم خونی، یا تغییرات ظریف در سطح فراساختارها رخ می دهد یا تغییرات مخرب فاحش تا نکروز ایسکمیک - حمله قلبی.
در کم خونی حاد تغییرات دیستروفیک و نکروبیوتیک معمولا رخ می دهد. قبل از آنها تغییرات هیستوشیمیایی و فراساختاری وجود دارد - ناپدید شدن گلیکوژن از بافت، کاهش فعالیت آنزیم های ردوکس و تخریب میتوکندری. برای تشخیص ماکروسکوپی، از نمک های مختلف تترازولیوم، تلوریت پتاسیم استفاده می شود که در خارج از نواحی ایسکمی (جایی که فعالیت دهیدروژنازها زیاد است)، ترمیم می شود و بافت را خاکستری یا سیاه می کند، در حالی که نواحی ایسکمی (که در آن فعالیت آنزیم ها کاهش یافته یا وجود ندارند) بدون رنگ باقی می مانند. بر اساس نتایج یک مطالعه الکترونی هیستوشیمیایی تغییرات بافتی در کم خونی حاد و حمله قلبی، ایسکمی حاد باید به عنوان وضعیت پیش نکروز (پیش انفارکتوس).در کم خونی طولانی مدت آتروفی عناصر پارانشیمی و اسکلروز در نتیجه افزایش فعالیت کلاژن سازی فیبروبلاست ها ایجاد می شود.
بسته به دلایل و شرایط در صورت وقوع، انواع زیر از کم خونی متمایز می شود: آنژیواسپاستیک، انسدادی، فشرده سازی، در نتیجه توزیع مجدد خون.
کم خونی آنژیو اسپاستیکبه دلیل اسپاسم شریان در اثر عمل محرک های مختلف رخ می دهد. به عنوان مثال، تحریک دردناک می تواند باعث اسپاسم عروق و کم خونی در مناطق خاصی از بدن شود. مکانیسم اثر منقبض کننده عروق نیز به همین صورت است مواد مخدر(مثل آدرنالین). ایسکمی آنژیو اسپاستیک نیز با تأثیرات عاطفی منفی ظاهر می شود ("آنژیواسپاسم احساسات بدون واکنش").
کم خونی انسدادیدر نتیجه بسته شدن مجرای شریان توسط ترومبوز یا آمبولی، در نتیجه تکثیر بافت همبند در مجرای شریان همراه با التهاب دیواره آن (اندرتریت محو کننده)، باریک شدن لومن شریان ایجاد می شود. شریان توسط یک پلاک آترواسکلروتیک. ایسکمی انسدادی ناشی از ترومبوز شریانی اغلب آنژیواسپاسم را کامل می کند و بالعکس، آنژیواسپاسم انسداد شریان را با ترومبوز یا آمبولی تکمیل می کند.
کم خونی فشاریهنگامی ظاهر می شود که شریان توسط تومور، افیوژن، تورنیکه، لیگاتور فشرده می شود.
ایسکمی ناشی از توزیع مجدد خوندر موارد پرخونی پس از کم خونی مشاهده می شود (نگاه کنید به. مجموعه شریانی).به عنوان مثال، ایسکمی مغزی در هنگام استخراج مایع از حفره شکمیجایی که توده ی بزرگی از خون سرازیر می شود.
معنی و عواقب کم خونی متفاوت است و به ویژگی های علت و مدت اثر آن بستگی دارد. بنابراین کم خونی ناشی از اسپاسم رگ ها معمولاً کوتاه مدت است و اختلال خاصی ایجاد نمی کند. با این حال، با اسپاسم طولانی مدت، تغییرات دیستروفیک و حتی نکروز ایسکمیک (حمله قلبی) ممکن است ایجاد شود. کم خونی انسدادی حاد به ویژه خطرناک است، زیرا اغلب منجر به حمله قلبی می شود. اگر بسته شدن مجرای شریان به آرامی ایجاد شود، می توان گردش خون را با کمک وسایل جانبی بازیابی کرد و عواقب چنین کم خونی ممکن است جزئی باشد. با این حال، کم خونی طولانی مدت دیر یا زود منجر به آتروفی و اسکلروز می شود.
خون ریزی
خونریزی (خونریزی)- خروج خون از لومن رگ خونییا حفره قلب وارد محیط می شود (در فضای باز خونریزی) یا در حفره بدن (درونی؛ داخلی خون ریزی). نمونه هایی از خونریزی خارجی شامل هموپتیزی است (هموپتوآ)،خونریزی بینی (خون دماغ شدن)،استفراغ خون (هموتنزیس)دفع خون در مدفوع (ملنا)خونریزی از رحم (متروراژی).با خونریزی داخلی، خون می تواند در حفره پریکارد (هموپریکاردیوم)، پلور (هموتوراکس) و حفره شکمی (هموپریتونئوم) جمع شود.
اگر در هنگام خونریزی خون در بافت ها جمع می شود، پس از آن صحبت می کنند خونریزیاز این نتیجه می شود که خونریزی نوع خاصی از خونریزی است. تجمع خون منعقد شده در بافت با نقض یکپارچگی آن نامیده می شود هماتوم(شکل 56)، و با حفظ عناصر بافت - اشباع هموراژیک(انفیلتراسیون هموراژیک).
خونریزی های مسطح، به عنوان مثال، در پوست، غشاهای مخاطی نامیده می شوند کبودیو خونریزی های نقطه ای کوچک - پتشی هامن، یا اکیموز
دلایل خونریزی (خونریزی) می تواند پارگی، خوردگی و افزایش نفوذپذیری دیواره عروق (قلب) باشد. خونریزی به دلیل پارگیدیواره های قلب یا رگ (خونریزی در هر رکسین،لات
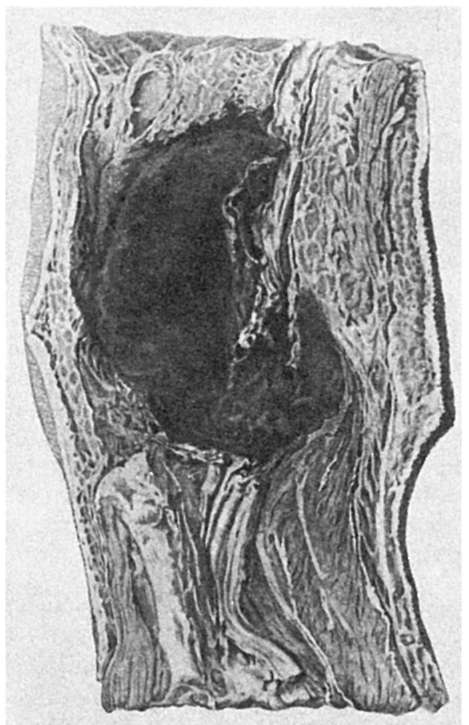 برنج. 56.هماتوم گسترده در بافت های نرم مفصل زانوپس از شلیک گلوله
برنج. 56.هماتوم گسترده در بافت های نرم مفصل زانوپس از شلیک گلوله
رکسو- پارگی) هنگام آسیب دیدگی، ضربه به دیوار یا ایجاد فرآیندهای پاتولوژیک مانند نکروز (سکته قلبی)، التهاب یا اسکلروز در آن رخ می دهد.
خونریزی زمانی که رگ آسیب می بیند به اولیه و ثانویه تقسیم می شود. خونریزی اولیه در زمان آسیب اتفاق می افتد و خونریزی ثانویه پس از مدتی مشخص به دلیل خفگی زخم و ذوب شدن لخته خون که باعث بسته شدن نقص عروق شده است.
برای پارگی قلب و خونریزیاغلب منجر می شود نکروز (سکته قلبی).پارگی فوق دریچه ای آئورت اغلب به دلیل نکروز غشای میانی آن ایجاد می شود (مدیونکروز).التهاب لایه میانی آئورت (مزائورتیت)با یک نتیجه در اسکلروز در سیفلیس همچنین می تواند منجر به پارگی دیواره آئورت و خونریزی شود. اغلب ملاقات می کنند پارگی آنوریسم قلب،آئورت، شریان های مغز، شریان ریویو عروق سایر اندام ها، منجر به خونریزی کشنده می شود. این دسته همچنین شامل خونریزی در هنگام پاره شدن کپسول اندام ها به دلیل ایجاد فرآیندهای پاتولوژیک در آنها می شود.
خونریزی در نتیجه فرسایش دیواره عروق (هموراژی در دیابروزین،یونانی دیابروز- فرسایش، خوردگی)، یا خونریزی خورنده،در بسیاری از فرآیندهای پاتولوژیک رخ می دهد، اما اغلب با التهاب، نکروز و تومور بدخیم. از جمله خونریزی های ساینده هنگامی که دیواره عروق توسط آنزیم های پروتئولیتیک در کانون التهاب چرکی خورده می شود (به عنوان مثال، با آپاندیسیت چرکی)، شیره معده - در پایین زخم معده، نکروز کازئوس (در دیواره حفره سل) ، با زخم تومور سرطانی (به عنوان مثال، زخم معده سرطان رکتوم، سینه). خونریزی خورنده نیز در طول حاملگی خارج رحمی (لوله ای) ایجاد می شود، زمانی که پرزهای کوریونی رشد می کنند و دیواره لوله رحمی (فالوپی) و عروق آن را خورده می کنند.
خونریزی به دلیل افزایش نفوذپذیری دیواره عروق،یا خونریزی دیاپدتیک (هموراژی در هر دیاپدیز،از یونانی دیا- از طریق و پدائو- پریدن) (شکل 57)، به دلایل زیادی از شریان ها، مویرگ ها و ونول ها ناشی می شود. در میان آنها، angionev-
اختلالات چرخشی، تغییر در میکروسیرکولاسیون، هیپوکسی بافت. بنابراین، خونریزی های دیاپدزی اغلب با آسیب مغزی یافت می شود. فشار خون شریانیواسکولیت سیستمیک، بیماری های عفونی و عفونی آلرژیک، با بیماری های سیستم خونی (هموبلاستوز و کم خونی)، کواگولوپاتی ها. خونریزی های دیاپدی - کوچک، نقطه ای (پورپورا هموراژیک).هنگامی که خونریزی های دیاپدزی سیستمیک می شوند، به یک تظاهرات تبدیل می شوند سندرم هموراژیک
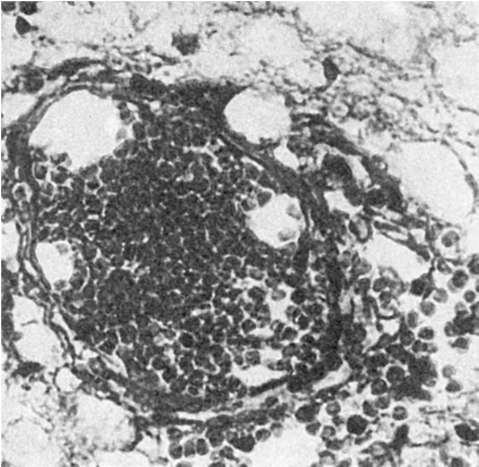 برنج. 57.خونریزی دیاپدتیک در بافت مغز
برنج. 57.خونریزی دیاپدتیک در بافت مغز
خروج تحلیل خون، تشکیل کیست در محل خونریزی (مثلاً در مغز)، کپسوله کردن یا تهاجم هماتوم توسط بافت همبند، ایجاد عفونت و چرکی.
معنی خونریزی بر اساس نوع و علت آن، میزان خون از دست رفته، سرعت از دست دادن خون تعیین می شود. پارگی قلب، آئورت و آنوریسم آن منجر به از دست دادن سریع مقادیر زیادی خون و در اکثریت قریب به اتفاق موارد به مرگ (مرگ بر اثر خونریزی حاد) می شود. خونریزی که برای چند روز ادامه می یابد نیز می تواند باعث از دست دادن خون قابل توجه و مرگ (به دلیل کم خونی حاد) شود. خونریزی طولانی مدت و مکرر (به عنوان مثال، با زخم معدهمعده و دوازدهه، هموروئید) می تواند منجر به کم خونی مزمن (کم خونی پس از هموراژیک) شود. اهمیت خونریزی برای بدن تا حد زیادی به محل آن بستگی دارد. به ویژه خطرناک، اغلب کشنده، خونریزی مغزی است (یک تظاهرات سکته مغزی هموراژیک در فشار خون، پارگی آنوریسم شریان مغز). خونریزی در ریه ها اغلب کشنده است زمانی که آنوریسم ریوی پاره می شود، ساییدگی عروق در دیواره حفره سل و غیره. در عین حال، خونریزی های شدید در بافت چربی زیر جلدی و ماهیچه ها اغلب هیچ خطری برای زندگی ندارند.
پلاسموراژی
پلاسموراژی- خروج پلاسما از جریان خون. پیامد پلاسموراژ، اشباع پلاسمایی دیواره عروق و بافت های اطراف آن است. اشباع پلاسمایکی از تظاهرات پلاسموراژی است اختلال در نفوذپذیری عروقی،ارائه تبادل طبیعی ترانس مویرگ
متابولیسم از طریق دیواره مویرگی با استفاده از مکانیسم های اولترافیلتراسیون، انتشار و انتقال میکرووزیکولار انجام می شود. زیر اولترافیلتراسیونبه معنای نفوذ مواد از طریق منافذ به غشاء تحت تأثیر فشار هیدرواستاتیک یا اسمزی است. در انتشارانتقال مواد از خون به بافت و از بافت به خون با گرادیان غلظت این مواد در هر دو طرف دیواره مویرگی (نشر غیرفعال) یا با کمک آنزیم های غشای سلولی - پرمازها (نشر فعال) تعیین می شود. انتقال میکرووزیکولار، میکروپینوسیتوز،یا سیتوپمسیس،انتقال هر ماکرومولکول پلاسمای خون را از طریق سلول های اندوتلیال فراهم می کند. این یک فرآیند متابولیک فعال است که توسط فعالیت آنزیمی بالای میکرووزیکول ها مشهود است. مسیر بین سلولی نقش ناچیزی در تبادل بین مویرگ ایفا می کند. وجود اثبات شده تفاوت اعضای بدن نفوذپذیری عروقی اندام هایی با نفوذپذیری عروقی نسبتاً بالا عبارتند از: کبد، طحال، مغز استخوان، با نفوذپذیری عروقی نسبتاً کم - قلب، ریه ها، مغز و اندام هایی که موقعیت میانی را اشغال می کنند - کلیه ها، روده ها، غدد درون ریز.
در آزمایش میکروسکوپیآغشته شدن دیواره شریان به پلاسما باعث ضخیم شدن و همگن شدن آن می شود (شکل 58). با درجه شدید پلاسموراژ رخ می دهد نکروز فیبرینوئید
در بررسی میکروسکوپی الکترونی افزایش نفوذپذیری عروقی با هیپروزیکولاسیون، ادم یا نازک شدن اندوتلیوم، تشکیل فنسترا و تونل ها در آن، ظهور شکاف های بین سلولی گسترده و نقض یکپارچگی غشای پایه مشهود است. این تغییرات نشان می دهد که از هر دو مسیر ترانس و بین اندوتلیال در پلاسموراژ استفاده می شود.
مکانیسم توسعهپاتوژنز پلاسموراژ و اشباع پلاسما توسط دو شرط اصلی تعیین می شود - خسارت
عروق ریز عروق و تغییرات ثابت خون،به افزایش نفوذپذیری عروق کمک می کند. آسیب به رگهای کوچک اغلب با اختلالات عصبی عروقی (اسپاسم)، هیپوکسی بافتی و واکنشهای آسیبشناسی ایمنی همراه است. تغییرات خونی که به پلاسموراژ کمک می کند به افزایش محتوای پلاسما در مواد وازواکتیو (هیستامین، سروتونین)، داروهای ضد انعقاد طبیعی (هپارین، فیبرینولیزین)، پروتئین های درشت، لیپوپروتئین ها، ظاهر مجتمع های ایمنی و نقض خواص رئولوژیکی کاهش می یابد. پلاسموراژی اغلب در فشار خون بالا رخ می دهد،
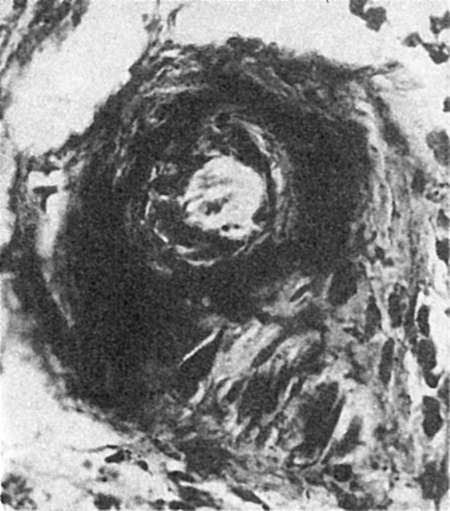 برنج. 58.آغشته شدن دیواره یک شریان کوچک به پلاسما (پروتئین های پلاسما سیاه هستند)
برنج. 58.آغشته شدن دیواره یک شریان کوچک به پلاسما (پروتئین های پلاسما سیاه هستند)
آترواسکلروز، نقص های جبران نشده قلبی، بیماری های عفونی، عفونی-آلرژیک و خود ایمنی.
خروجدر نتیجه اشباع پلاسما، نکروز فیبرینوئیدو هیالینوز عروقی
معنی پلاسموراژ در درجه اول شامل اختلالات متابولیسم ترانس مویرگی است که منجر به تغییرات ساختاری در اندام ها و بافت ها می شود.
ایستایی
ایستایی(از لات ایستایی- توقف) - توقف جریان خون در عروق میکروواسکولار، عمدتا در مویرگ ها. توقف جریان خون معمولاً با کاهش شدید سرعت انجام می شود که به عنوان تعیین می شود وضعیت پروستات،یا پیش استاز
ویژگی های اصلی پدیده لجن(از انگلیسی. لجن- تینا) چسبندگی گلبول های قرمز، لکوسیت ها یا پلاکت ها به یکدیگر و افزایش ویسکوزیته پلاسما را در نظر بگیرید که منجر به مشکل در جریان خون از طریق عروق ریز عروق می شود. پدیده لجن را می توان نوعی سکون در نظر گرفت.
مکانیسم توسعهدر شروع استاز، تغییرات در درجه اول اهمیت قرار دارند خواص رئولوژیکیخون ارسال شد افزایش تجمع داخل مویرگ گلبول های قرمز،که منجر به افزایش مقاومت در برابر جریان خون از طریق مویرگ ها، کاهش سرعت و توقف آن می شود. همولیز و انعقاد خون در هنگام استاز رخ نمی دهد. توسعه تجمع داخل مویرگ گلبول های قرمز توسط: تغییرات در مویرگ ها که منجر به افزایش نفوذپذیری دیواره های آنها می شود تسهیل می شود. پلاسموراژی؛ نقض خواص فیزیکوشیمیایی گلبول های قرمز، به ویژه کاهش پتانسیل سطحی آنها. تغییر در ترکیب پروتئین های خون به دلیل افزایش بخش های درشت. اختلالات دیسیرکولاتور - احتقان وریدی (ایستایی احتقانی)یا ایسکمی (استاز ایسکمیک)،نقض عصب ریز عروق.
دلیل ایجاد استاز اختلالات دیسیرکولاتوری هستند. آنها می توانند با عمل فیزیکی ( حرارت، سرما) و عوامل شیمیایی (اسیدها، قلیایی ها) در بیماری های عفونی (مالاریا، تیفوس)، عفونی-آلرژیک و خود ایمنی (بیماری های روماتیسمی)، بیماری های قلب و عروق خونی (نقایص قلبی، بیماری عروق کرونر قلب) ایجاد می شوند.
معنی استاز نه تنها با طول مدت آن، بلکه همچنین با حساسیت یک اندام یا بافت به گرسنگی اکسیژن (مغز) تعیین می شود. استاز یک پدیده برگشت پذیر است. حالت پس از حل سکون نامیده می شود پست استاتیک استاز برگشت ناپذیر منجر به نکروز و نکروز می شود.
ترومبوز
ترومبوز(از یونانی. ترومبوز- انعقاد) - انعقاد خون داخل حیاتی در مجرای رگ یا در حفره های قلب. لخته خون حاصل نامیده می شود ترومبوز
هنگام لخته شدن لنفاوی، از ترومبوز نیز صحبت می شود و لخته شدن لنفاوی داخل عروقی ترومبوز نامیده می شود، با این حال، الگوهای ترومبوز لنفاوی و هموترومبوز متفاوت است.
بر اساس مفهوم مدرن، لخته شدن خون از چهار مرحله عبور می کند:
I - پروترومبوکیناز + فعال کننده -> ترومبوکیناز (ترومبوپلاستین فعال)؛
II - پروترومبین + Ca 2 + + ترومبوکیناز -> ترومبین.
III - فیبرینوژن + ترومبین -> مونومر فیبرین.
IV - مونومر فیبرین + فاکتور محرک فیبرین -> پلیمر فیبرین.
فرآیند انعقاد خون به شکل یک واکنش آبشاری (نظریه "آبشار") با فعال سازی متوالی پروتئین های پیش ساز یا عوامل انعقادی،در خون یا بافت ها قرار دارد. بر این اساس، سیستم های انعقادی داخلی (خون) و خارجی (بافت) متمایز می شوند. رابطه بین سیستم های داخلی و خارجی در نمودار 8 نشان داده شده است.
باید در نظر داشت که علاوه بر سیستم انعقاد، وجود دارد سیستم ضد انعقاد،که تنظیم سیستم هموستاز - حالت مایع خون در بستر عروقی را در شرایط عادی تضمین می کند. بر این اساس، ترومبوز تظاهر اختلال در تنظیم سیستم هموستاتیک است.
مکانیسم توسعهتشکیل ترومبوز شامل چهار مرحله متوالی است: آگلوتیناسیون پلاکتی، انعقاد فیبرینوژن و تشکیل فیبرین، آگلوتیناسیون گلبول قرمز، رسوب پروتئین پلاسما.
آگلوتیناسیون پلاکتیقبل از آنها افتادن آنها از جریان خون، حرکت هدایت شده و چسبندگی (چسبندگی) به محل آسیب دیده می شود.
طرح هشتم.رابطه بین سیستم های انعقاد خون داخلی و خارجی (طبق گفته V.A.Kudryashov)
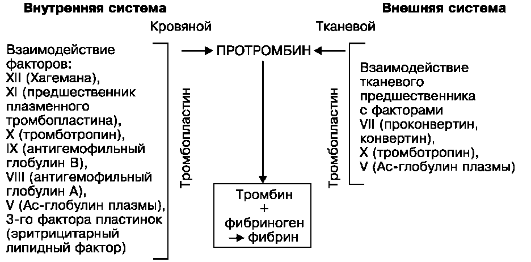 پوشش اندوتلیال (شکل 59). ظاهراً "آسیب" پلاکت ها باعث آزاد شدن کمپلکس لیپوپروتئین ناحیه محیطی صفحات (هیالومر) می شود که خاصیت آگلوتیناسیون دارد. آگلوتیناسیون پلاکت ها با دگرانولاسیون آنها، آزادسازی سروتونین و فاکتور ترومبوپلاستیک صفحه پایان می یابد که منجر به تشکیل ترومبوپلاستین فعال و گنجاندن مراحل بعدی انعقاد خون می شود.
پوشش اندوتلیال (شکل 59). ظاهراً "آسیب" پلاکت ها باعث آزاد شدن کمپلکس لیپوپروتئین ناحیه محیطی صفحات (هیالومر) می شود که خاصیت آگلوتیناسیون دارد. آگلوتیناسیون پلاکت ها با دگرانولاسیون آنها، آزادسازی سروتونین و فاکتور ترومبوپلاستیک صفحه پایان می یابد که منجر به تشکیل ترومبوپلاستین فعال و گنجاندن مراحل بعدی انعقاد خون می شود.
 برنج. 59.مورفوژنز ترومبوز:
برنج. 59.مورفوژنز ترومبوز:
الف - مرحله اول تشکیل ترومبوز. توده های کوچک پلاکت ها (Tr) در نزدیکی سلول اندوتلیال آسیب دیده (EN). х14000 (طبق گفته اشفورد و فریمن)؛ ب - مرحله دوم تشکیل ترومبوز. در ناحیه اندوتلیوم تخریب شده، تجمع پلاکت ها (Tr1) و فیبرین (F) قابل مشاهده است. Tr2 - پلاکت های بدون تغییر. x7500 (طبق گفته اشفورد و فریمن)؛ ج - توده های ترومبوتیک، متشکل از فیبرین، لکوسیت ها و گلبول های قرمز آگلوتینه شده.
انعقاد فیبرینوژنو تشکیل فیبرین(نگاه کنید به شکل 59) با یک واکنش آنزیمی (ترومبوپلاستین - ترومبین - فیبرینوژن - فیبرین) همراه است و ماتریکس فیبرین به منطقه مرکزی "لخت" صفحات (گرانولومر) تبدیل می شود که حاوی آنزیمی با خاصیت جمع شوندگی (صفحه) است. رتراکتوزیم). فعالیت رتراکتوزیم و همچنین سروتونین که در حین از هم پاشیدگی صفحات آزاد می شود و دارای خاصیت منقبض کننده عروق است به شما امکان می دهد چین فیبرین را "فشرده" کنید. لکوسیت ها، گلبول های قرمز آگلوتینه شدهو رسوب پروتئین های پلاسما(شکل 59 را ببینید).
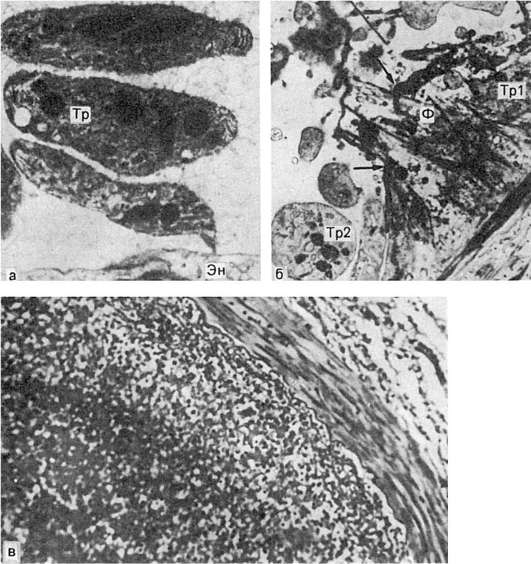
مورفولوژی ترومبوز.یک ترومبوس معمولاً در محل آسیب به دیواره رگ متصل می شود، جایی که فرآیند تشکیل ترومبوز آغاز شد. سطح آن موجدار است (شکل 60)، که منعکس کننده از دست دادن ریتمیک پلاکت های چسبنده و رسوب رشته های فیبرین به دنبال پوسیدگی آنها با ادامه جریان خون است. ترومبوس، به عنوان یک قاعده، قوام متراکم، خشک است. اندازههای ترومبوز متفاوت است - از اندازههایی که فقط با بررسی میکروسکوپی تعیین میشوند تا اندازههایی که حفره قلب یا مجرای یک رگ بزرگ را در طول قابل توجهی پر میکنند.
یک ترومبوس معمولاً از پرتوهای انشعاب پلاکتهای چسبانده و دستههای فیبرین با گلبولهای قرمز و لکوسیتهایی که بین آنها قرار دارند ساخته میشود (شکل 59 را ببینید).
بسته به ساختمان ها و ظاهر، که بر اساس ویژگی ها و سرعت تشکیل ترومبوز مشخص می شود، ترومب های سفید، قرمز، مخلوط (لایه ای) و هیالین وجود دارد.
لخته خون سفیداز پلاکت ها، فیبرین و لکوسیت ها تشکیل شده است (شکل 60 را ببینید)، به آرامی با جریان خون سریع (اغلب در شریان ها) تشکیل می شود. لخته خون قرمزعلاوه بر پلاکت ها و فیبرین، حاوی تعداد زیادی گلبول قرمز است (شکل 60 را ببینید)، به سرعت با جریان خون آهسته (معمولاً در وریدها) تشکیل می شود. در رایج ترین لخته خون مخلوط(نگاه کنید به شکل 60)، که ساختار لایه ای دارد (ترومبوز لایه ای)و ظاهری متنوع، حاوی عناصری از لخته های خون سفید و قرمز است. در یک ترومبوز مختلط، وجود دارد سر (ساختار لخته سفید خون دارد) بدن (در واقع لخته خون مخلوط) و دم (ساختار لخته خون قرمز دارد). سر به پوشش اندوتلیال رگ متصل است که ترومبوز را از لخته خون پس از مرگ متمایز می کند. لخته های خونی لایه ای بیشتر در وریدها، در حفره آنوریسم آئورت و قلب ایجاد می شوند. ترومبوز هیالین- نوع خاصی از لخته شدن خون؛ به ندرت حاوی فیبرین است، از گلبول های قرمز تخریب شده، پلاکت ها و پروتئین های پلاسما تشکیل شده است. در حالی که توده های ترومبوتیک شبیه هیالین هستند. چنین لخته های خونی در عروق میکروواسکولار یافت می شوند.
ممکن است ترومبوز باشد جداری،سپس بیشتر لومن آزاد است (شکل 60 را ببینید)، یا گرفتگیمسدود کننده لومن (انسداد ترومبوز- شکل را ببینید. 60). ترومبوز جداری اغلب در قلب در دریچه یا اندوکارد جداری در هنگام التهاب (ترومبوآندوکاردیت)، در گوش ها و بین ترابکول ها در نارسایی مزمن قلب (بیماری قلبی، بیماری ایسکمیک مزمن) یافت می شود.
 بیماری قلبی)، در شریان های بزرگ با آترواسکلروز، در سیاهرگ های دارای التهاب (ترومبوفلبیت، به شکل 60)، در آنوریسم های قلب و عروق خونی. ترومبوس گرفتگی اغلب در وریدها و شریان های کوچک با رشد ترومب جداری تشکیل می شود و کمتر در شریان های بزرگ و آئورت.
بیماری قلبی)، در شریان های بزرگ با آترواسکلروز، در سیاهرگ های دارای التهاب (ترومبوفلبیت، به شکل 60)، در آنوریسم های قلب و عروق خونی. ترومبوس گرفتگی اغلب در وریدها و شریان های کوچک با رشد ترومب جداری تشکیل می شود و کمتر در شریان های بزرگ و آئورت.
افزایش اندازه ترومبوز با لایهبندی تودههای ترومبوتیک روی ترومبوز اولیه اتفاق میافتد و رشد ترومبوز میتواند هم در جریان و هم در برابر جریان خون رخ دهد. گاهی اوقات لخته خونی که در وریدها مانند ساق پا شروع به تشکیل شده است، به سرعت در جریان خون رشد می کند و به رگ های وریدی جمع کننده مانند ورید اجوف تحتانی می رسد. این ترومبوز نامیده می شود ترقی خواه.یک ترومب در حال رشد دهلیز چپ ممکن است از اندوکارد جدا شود. از آنجایی که در حفره دهلیزی آزاد است، با حرکات خون "صیقل" می شود و شکل کروی به خود می گیرد - ترومبوس کروی(شکل 60 را ببینید). لخته خون در آنوریسم نامیده می شود گشاد شده
مکانیسم توسعهپاتوژنز ترومبوز پیچیده است و شامل مشارکت عوامل محلی و عمومی است که در تعامل با یکدیگر منجر به تشکیل ترومبوز می شود. به محلی عوامل شامل تغییرات است دیواره عروقیکاهش سرعت و اختلال در جریان خون؛ به مشترک عوامل - اختلال در سیستم انعقادی و ضد انعقاد وضعیت مایع خون در بستر عروقی و تغییر در ترکیب خون.
در میان تغییرات در دیواره عروقیبه خصوص مهم است که آسیب به پوشش داخلی رگ، اندوتلیوم آن، که باعث چسبیدن پلاکت ها به محل آسیب، دگرانولاسیون آنها و آزاد شدن ترومبوپلاستین می شود، یعنی. شروع تشکیل ترومبوز ماهیت تغییرات در دیواره شریان ها و وریدها که به ایجاد ترومبوز کمک می کند متفاوت است. اغلب این تغییرات التهابی- واسکولیت(آرتریت و فلبیت) در بسیاری از بیماری های عفونی و عفونی - آلرژیک. با توسعه ترومبوز به دلیل واسکولیت، آنها در مورد صحبت می کنند ترومبوواسکولیت (ترومبوآرتریتیا ترومبوفلبیت).این دسته نیز شامل می شود ترومبوآندوکاردیت،آن ها اندوکاردیت که با ترومبوز پیچیده می شود. اغلب منجر به ترومبوز می شود تغییرات آترواسکلروتیکشریان ها، به ویژه با زخم پلاک. اختلالات آنژینوروتیک همچنین منجر به آسیب به دیواره عروق می شود - اسپاسم شریان هاو شریان هادر این مورد، اندوتلیوم و غشای آن به ویژه آسیب می بینند، که به ایجاد پلاسموراژ و ترومبوز کمک می کند. بنابراین، چنین ترومبوز مکرری در فشار خون شریانی تعجب آور نیست. با این حال، یک تغییر در دیواره عروق برای ایجاد ترومبوز کافی نیست. اغلب، حتی با تغییرات شدید التهابی و آترواسکلروتیک در شریان ها، زمانی که سایر عوامل ترومبوز وجود ندارند، رخ نمی دهد.
کاهش سرعتو نقض (گرداب) جریان خونایجاد شرایط مطلوب برای از دست دادن پلاکت ها از جریان خون و چسبیدن آنها به اندوتلیوم در محل آسیب آن. وقوع لخته های خون بسیار بیشتر (5 برابر) می تواند با کاهش سرعت جریان خون همراه باشد.
در وریدها در مقایسه با شریانها، بروز مکرر لختههای خون در سیاهرگهای پا، بهویژه پاها، در نواحی واریس، در آنوریسمهای قلب و عروق خونی است. اهمیت کاهش جریان خون برای تشکیل ترومبوز نیز با وقوع مکرر ترومبوس همراه با تضعیف فعالیت قلبی، توسعه جبران ناپذیر قلبی عروقی مشهود است. در چنین مواردی صحبت می کنند لخته های خون راکدنقش اختلالات جریان خون در ایجاد ترومبوزها با محلی سازی مکرر آنها در محل انشعاب عروقی، جایی که شرایط مطلوب برای رسوب پلاکت ایجاد می شود، تأیید می شود. با این حال، اختلالات جریان خون به خودی خود، بدون مشارکت عوامل دیگر، منجر به تشکیل ترومبوز نمی شود.
در میان عوامل رایج تشکیل ترومبوز، نقش اصلی متعلق به اختلالات رابطهبین سیستم های انعقادی و ضد انعقاد در تنظیم وضعیت مایع خون در بستر عروقی. هم به فعال شدن عملکرد سیستم انعقادی و هم به سرکوب عملکرد سیستم ضد انعقاد اهمیت داده می شود. اعتقاد بر این است که مهار عملکرد سیستم ضد انعقاد، توسعه را تعیین می کند حالت پیش ترومبوتیکبا این حال، اساس ترومبوز در فعال شدن انعقاد یا مهار سیستم ضد انعقاد نیست، بلکه در اختلال در رابطه تنظیمی بین این سیستم ها است.
در تشکیل لخته های خون نقش تغییرات زیاد است ترکیب (کیفیت) خون، مانند افزایش محتوای بخش های درشت پراکنده پروتئین ها، به ویژه فیبرینوژن، لیپوپروتئین ها، لیپیدها در پلاسما، افزایش تعداد پلاکت ها، تغییر در ویسکوزیته و سایر خواص رئولوژیکی خون. چنین تغییراتی در بیماری ها (آترواسکلروز، بیماری های خودایمنی، هموبلاستوز) که اغلب با ترومبوز پیچیده می شوند، غیر معمول نیست.
آسیب شناسی هموستاز، که در آن ترومبوز عامل محرک اصلی است، به وضوح در تعدادی از سندرم ها نشان داده می شود که در این میان سندرم انعقاد داخل عروقی منتشر (DIC) و سندرم ترومبوآمبولیک بیشترین اهمیت بالینی را دارند.
سندرم انعقاد داخل عروقی منتشر (سندرم انعقاد داخل عروقی منتشر، سندرم ترومبوهموراژیک، انعقاد مصرفی)با تشکیل لخته های خونی منتشر (فیبرین و اریتروسیتیک، هیالین) در عروق میکروسکولار در ترکیب با انعقاد ناپذیری خون، که منجر به خونریزی های شدید متعدد می شود، مشخص می شود.
این بر اساس ناهماهنگی عملکرد سیستم های انعقاد خون و ضد انعقاد است که مسئول هموستاز هستند. بنابراین، انعقاد داخل عروقی منتشر (DIC) اغلب به عنوان یک عارضه بارداری و زایمان، با غیرقابل مهار رخ می دهد. خونریزی رحم، صدمات گسترده، با کم خونی، هموبلاستوز، عفونت (به ویژه سپسیس) و مسمومیت، بیماری های خود ایمنی و شوک. لخته های خون، به ویژه اغلب در رگ های کوچک ریه ها، کلیه ها، کبد، غدد فوق کلیوی، غده هیپوفیز، مغز، دستگاه گوارش، پوست، با خونریزی های متعدد، دیستروفی و نکروز اندام ها و بافت ها (نکروز قشر کلیه ها، نکروز) ترکیب می شوند. و خونریزی در ریه ها، مغز مغز، غدد فوق کلیوی، غده هیپوفیز و غیره). بسیاری از اندام ها "شوک" می شوند، نارسایی حاد تک یا چند عضوی ایجاد می شود.
O سندرم ترومبوآمبولیکآنها می گویند در مواردی که یک ترومبوز یا بخشی از آن شکسته شود، به ترومبوآمبولی تبدیل می شود (نگاه کنید به. آمبولی)از طریق گردش خون سیستمیک در خون گردش می کند و با مسدود کردن مجرای شریان ها باعث ایجاد حملات قلبی متعدد می شود. ترومبوآمبولی اغلب تغییر می کند آمبولوتومبوز،آن ها لایه بندی یک لخته خون روی ترومبوآمبولی. منشا ترومبوآمبولی اغلب ترومب های روی لت های دریچه میترال یا آئورت (اندوکاردیت باکتریایی یا روماتیسمی - شکل 61)، ترومب های بین ترابکولار بطن چپ و زائده دهلیز چپ، ترومب های آنوریسم قلب (بیماری عروق کرونر) است. نقایص قلبی)، آئورت و شریان های بزرگ (آترواسکلروز). ترومبوآمبولی متعدد در چنین مواردی منجر به ایجاد حملات قلبی در کلیه ها، طحال، مغز، قلب و قانقاریای روده ها، اندام ها می شود. سندرم ترومبوآمبولیک اغلب در بیماری های قلبی عروقی، سرطانی، عفونی (سپسیس) رخ می دهد. دوره بعد از عمل، با مداخلات جراحی مختلف.
ترومبوآمبولی ریوی همراه با ایجاد انفارکتوس ریوی را نیز میتوان یکی از انواع سندرم ترومبوآمبولیک در نظر گرفت (نگاه کنید به. آمبولی).
خروجترومبوز متفاوت است. به نتایج مطلوب عبارتند از اتولیز آسپتیک ترومبوز،تحت تأثیر آنزیم های پروتئولیتیک لکوسیت ها ایجاد می شود. لخته های خون کوچک می توانند به طور کامل تحت اتولیز آسپتیک قرار گیرند. اغلب ترومب ها، به خصوص بزرگ، با بافت همبند جایگزین می شوند، به عنوان مثال. سازماندهی شده است. رشد درونی بافت همبند به ترومبوز در ناحیه سر از سمت انتیما رگ شروع می شود، سپس کل توده ترومبوز با بافت همبند جایگزین می شود، که در آن ترک ها یا کانال های پوشیده از اندوتلیوم ظاهر می شود. -صدا کرد فاضلاب ترومبوز (شکل 60 را ببینید). بعداً، کانال های پوشیده شده با اندوتلیوم به عروق حاوی خون تبدیل می شوند، در چنین مواردی از آنها صحبت می شود رگزایی ترومبوز عروق خونی ترومبوس اغلب باز بودن رگ های خونی را بازیابی می کند. با این حال، سازماندهی یک ترومبوز همیشه با فاضلاب و عروق آن ختم نمی شود. ممکن است کلسیفیکاسیون ترومبوز، سنگ شدن آن، گاهی اوقات سنگ در رگها ظاهر می شود - فلبولیت
به نامطلوب پیامدهای ترومبوز شامل جدا شدن ترومبوز یا بخشی از آن و تبدیل آن به ترومبوآمبولی،که منشا ترومبوآمبولی است. همجوشی سپتیک یک ترومبوز، که زمانی رخ می دهد که باکتری های پیوژنیک وارد توده ترومبوتیک می شوند، که منجر به آمبولی ترومبوباکتریایی عروق اندام ها و بافت های مختلف (با سپسیس) می شود.
ارزش ترومبوزبا توجه به سرعت توسعه، محلی سازی و شیوع آن و همچنین نتیجه تعیین می شود. در برخی موارد می توان در مورد آن صحبت کرد مطلوب معنای ترومبوز، به عنوان مثال، در ترومبوز آنوریسم، زمانی که ترومبوس دیواره آن را "تقویت" می کند. در اکثریت قریب به اتفاق موارد، ترومبوز - یک پدیده خطرناک از آنجا که انسداد لخته خون در شریان ها می تواند باعث حمله قلبی یا قانقاریا شود. در عین حال، لخته های خونی جداری که به آرامی تشکیل می شوند حتی در تنه های شریانی بزرگ ممکن است منجر به عواقب جدی نشود، زیرا در چنین مواردی گردش خون جانبی زمان توسعه دارد.
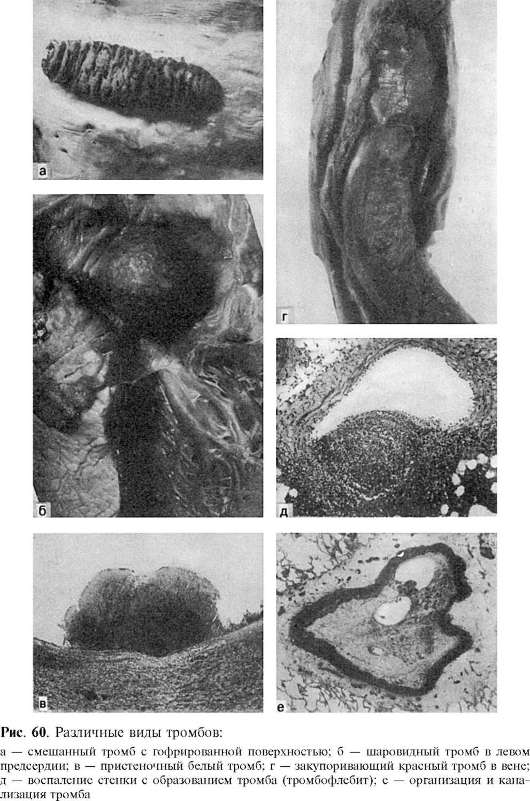
 برنج. 61.انواع آمبولی و آمبولی:
برنج. 61.انواع آمبولی و آمبولی:
الف - اندوکاردیت زگیل دریچه میترال - منبع ترومبوآمبولی گردش خون سیستمیک. ب - آمبولی ریه؛ حفره بطن راست و لومن شریان ریوی با توده های ترومبوآمبولیک پر شده است. ج - آمبولی چربی مویرگ های گلومرول کلیه (قطره های چربی با اسمیم سیاه رنگ می شوند). د - آمبولی چربی مویرگ های ریه در آزمایش (قطره های چربی با اسمیم سیاه رنگ می شوند). ه - آمبولی توسط بافت مخچه شریان کرونری قلب در نوزاد تازه متولد شده
آنها یک خطر بزرگ هستند ترومبوز پیشروندهو ترومبوز سپتیک
لخته شدن خون در آن لخته می شود رگهای بزرگ بسته به محلی بودن آنها تظاهرات مختلفی را ارائه می دهند. بنابراین، ترومبوز سینوس های وریدی سخت شامه به عنوان یک عارضه اوتیت میانی یا ماستوئیدیت می تواند منجر به تصادف عروق مغزی، ترومبوز ورید باب - به فشار خون پورتال و آسیت، ترومبوز ورید طحال - به اسپلنومگالی (ترومبوفلبیتی اسپلنومگالی) شود. با ترومبوز وریدهای کلیوی، در برخی موارد، سندرم نفروتیک یا انفارکتوس وریدی کلیه ایجاد می شود، با ترومبوفلبیت وریدهای کبدی - بیماری Budd-Chiari، و با ترومبوز وریدهای مزانتریک - گانگرن روده. یک تصویر بالینی مشخص توسط ترومبوفلبیت(فلبیت عارضه دار ترومبوز) وریدهای اندام تحتانی و فلبوترومبوز(ترومبوز وریدی) به منبع آمبولی ریه تبدیل می شود.
اهمیت بالینی ترومبوز و ترومبوآمبولی به این دلیل است که اغلب به عوارض کشنده بسیاری از بیماری ها تبدیل می شوند و در سال های اخیر فراوانی عوارض ترومبوآمبولی افزایش یافته است.
آمبولی
آمبولی(از یونانی. em-ballein- پرتاب به داخل) - گردش در خون (یا لنف) ذراتی که در شرایط عادی یافت نمی شوند و انسداد آنها در رگ های خونی. خود ذرات نامیده می شوند آمبولی(شکل 61 را ببینید). آمبولی به احتمال زیاد در امتداد حرکت می کند جریان خون در سه جهت: 1) از سیستم وریدی گردش خون سیستمیک و قلب راست به عروق گردش خون ریوی. اگر آمبولی، به عنوان مثال، در سیستم ورید اجوف تحتانی یا فوقانی وجود داشته باشد، آنها وارد ریه ها می شوند. 2) از نیمه چپ قلب، آئورت و شریان های بزرگ، و همچنین (به ندرت) از وریدهای ریوی در شریان های قلب، مغز، کلیه ها، طحال، روده ها، اندام ها و غیره. 3) از شاخه های سیستم پورتال به داخل سیاهرگ باب کبد. با این حال، کمتر آمبولی، به دلیل شدت آن، می تواند حرکت کند در برابر جریان خون، برای مثال، از طریق ورید اجوف تحتانی به داخل ورید کلیه، کبدی یا حتی فمورال فرود آید. این آمبولی نامیده می شود واپسگرادر صورت وجود نقص در سپتوم دهلیزی یا بین بطنی، آمبولی متناقض:آمبولی از وریدهای دایره بزرگ، با دور زدن ریه ها، وارد شریان ها می شود. آمبولی متناقض شامل میکروآمبولی عروقی از طریق آناستوموزهای شریانی وریدی است.
مکانیسم توسعهنمی توان آن را تنها به بسته شدن مکانیکی لومن رگ کاهش داد. در ایجاد آمبولی از اهمیت بالایی برخوردار است اسپاسم رفلکسهم خط عروقی اصلی و هم جانبی آن که باعث اختلالات شدید دیسیرکولاتوری می شود. اسپاسم شریان ها می تواند به رگ های جفت یا هر اندام دیگری گسترش یابد (به عنوان مثال، رفلکس کلیه در صورت آمبولی عروقی یکی از کلیه ها، رفلکس ریوی در صورت آمبولی ریوی).
بسته به طبیعت آمبولی که می تواند منفرد یا چندگانه باشد، انواع زیر را از آمبولی تشخیص می دهد: ترومبوآمبولی، چربی، هوا، گاز، بافت (سلولی)، میکروبی، آمبولی اجسام خارجی.
ترومبوآمبولی- رایج ترین نوع آمبولی (شکل 61 را ببینید). زمانی اتفاق میافتد که یک ترومبوز یا بخشی از آن پاره میشود و اندازه ترومبوآمبولی میتواند متفاوت باشد - از آنهایی که فقط در زیر میکروسکوپ تعیین میشوند تا طول چند سانتیمتر.
اگر ترومبوس وریدهای گردش خون سیستمیک یا حفره های نیمه راست قلب آمبولی شود، آنگاه به شاخه های شریان ریوی می افتند. ناشی می شود آمبولی ریه(شکل 61 را ببینید). ترومبوآمبولی شاخه های کوچک شریان ریوی معمولاً ایجاد می شود انفارکتوس هموراژیک ریه،و با ترومبوآمبولی شاخه های بزرگ رخ می دهد مرگ ناگهانی. گاهی اوقات مرگ ناگهانی زمانی رخ می دهد که ترومبوآمبولی در محل انشعاب تنه اصلی شریان ریوی پیدا شود. در پیدایش مرگ در آمبولی ریه، نه به عامل مکانیکی بسته شدن مجرای رگ، بلکه به رفلکس کرونری ریوی اهمیت داده می شود. در این مورد، اسپاسم درخت برونش، شاخه های شریان ریوی و عروق کرونر قلب وجود دارد.
منبع ترومبوآمبولی گردش خون سیستمیکهمانطور که قبلاً ذکر شد، ترومبهایی که بر روی کاسه دریچههای قلب چپ ایجاد میشوند، ترومبهایی که بین عضلات ترابکولار بطن چپ، در زائده دهلیز چپ یا در آنوریسم قلب، در آئورت و سایر شریانها قرار دارند، استفاده میشوند. در این موارد توسعه می یابد سندرم ترومبوآمبولیکبا حملات قلبی در بسیاری از اندام ها (نگاه کنید به. ترومبوز).
O آمبولی چربیمی گویند در مواردی که منشأ آن قطرات چربی است. به عنوان یک قاعده، اینها چربی های بدن هستند. قطرات چربی که وارد سیاهرگ ها می شوند مویرگ های ریه ها را محو می کنند یا با دور زدن ریه ها از طریق آناستوموزهای شریانی وریدی وارد مویرگ های گلومرول کلیه ها، مغز و سایر اندام ها می شوند (شکل 61 را ببینید). از نظر ماکروسکوپی، اندامها در طول آمبولی چربی تغییر نمیکنند، آمبولیهای چربی تنها در طول بررسی میکروسکوپی بخشهایی که مخصوص چربیها رنگآمیزی شدهاند (سودان III یا IV، اسید اسمیک و غیره) در مویرگها یافت میشوند.
آمبولی چربی معمولاً با له شدن تروماتیک بافت زیر جلدی، مغز استخوان (با شکستگی یا زخم گلوله استخوانهای بلند) ایجاد میشود. به ندرت زمانی اتفاق می افتد که به بیمار دارو یا مواد حاجب تهیه شده در روغن تزریق شود. اغلب اوقات، به عنوان مثال، با شکستگی استخوان های لوله ای بلند، آمبولی چربی از نظر بالینی ظاهر نمی شود، زیرا چربی امولسیون شده، صابونی شده و توسط لیپوفاژها در ریه ها جذب می شود (گاهی اوقات ذات الریه رخ می دهد). اگر 2/3 مویرگ های ریوی بسته شوند آمبولی چربی خطرناک می شود. سپس یک حاد نارسایی ریویو ایست قلبی
آمبولی کشنده مویرگ های مغز نیز می تواند کشنده باشد که منجر به بروز خونریزی های نقطه ای متعدد در بافت مغز می شود.
آمبولی هوازمانی اتفاق می افتد که هوا وارد جریان خون می شود. این یک نوع نادر از آمبولی است که زمانی رخ می دهد که وریدهای گردن زخمی می شوند، که با فشار منفی در آنها تسهیل می شود. با شکاف وریدهای سطح داخلی رحم پس از زایمان؛ اگر یک ریه اسکلروز آسیب دیده باشد که وریدهای آن فرو نمی ریزند. هنگام استفاده از پنوموتوراکس؛ با جراحی قلب باز؛ در صورت ورود تصادفی هوا همراه با مواد دارویی به داخل سیاهرگ. حباب های هوا که در خون به دام افتاده اند باعث آمبولی رگ های گردش خون ریوی می شوند و مرگ ناگهانی رخ می دهد. در این حالت هوا در حفره قلب راست جمع می شود و آن را کشیده می شود.
برای تشخیص آمبولی هوا در کالبد شکافی باید قلب سمت راست را بدون برداشتن آن و پس از پر کردن حفره پیراهن قلب با آب سوراخ کرد. آمبولی هوا با انتشار هوا از طریق سوراخ در محل سوراخ تشخیص داده می شود. خون در حفره قلب، به خصوص سمت راست، ظاهری کف آلود دارد، سیاهرگ ها حاوی حباب های هوا هستند.
آمبولی گازیآن ها انسداد رگ های خونی توسط حباب های گاز، در کارگران شاغل در کار کیسون، غواصان در موارد انتقال سریع از فشار اتمسفر بالا به حالت عادی رخ می دهد، به عنوان مثال. با رفع فشار سریع مشخص است که با افزایش فشار اتمسفر در خون، مقدار زیادی نیتروژن تجمع یافته و حل می شود که به بافت ها می رود. در خلال فشرده سازی سریع، نیتروژن آزاد شده از بافت ها زمان آزاد شدن توسط ریه ها را ندارد و به شکل حباب های گاز در خون تجمع می یابد. آمبولی های گازی مویرگ های سر را مسدود می کند و نخاع، کبد، کلیه ها و سایر اندام ها که با ظاهر شدن کانون های ایسکمی و نکروز در آنها (به ویژه کانون های مکرر نرم شدن در مغز و نخاع)، ایجاد خونریزی های متعدد و لخته شدن خون همراه است. این تغییرات مشخصه است بیماری رفع فشار تغییرات نزدیک به بیماری رفع فشار، که در خلبانان در هنگام صعود و فرود با سرعت بالا مشاهده می شود. گاهی اوقات آمبولی گازی به عنوان یک عارضه رخ می دهد گانگرن گازی (بی هوازی).
آمبولی بافتی (سلولی).در صورت تخریب بافت به دلیل تروما یا یک فرآیند پاتولوژیک که منجر به ورود قطعات بافتی (سلولها) به خون میشود (شکل 61 را ببینید). آمبولی می تواند بافت تومور یا مجموعه ای از سلول های تومور در طول پوسیدگی آن، قطعات دریچه قلب در صورت اندوکاردیت اولسراتیو، بافت مغز در صورت ضربه به سر باشد. آمبولی توسط بافت مغز عروق گردش خون کوچک و بزرگ در نوزادان با تروما هنگام تولد... آمبولی بافتی به عنوان آمبولی مایع آمنیوتیک در زنان پس از زایمان نیز شناخته می شود. اغلب، آمبولی بافتی (سلولی) در عروق دایره بزرگ، کمتر در عروق گردش خون ریوی مشاهده می شود. دسته خاصی از آمبولی بافتی آمبولی توسط سلول های بدخیم است
تومور، زیرا زمینه ساز متاستاز تومور هماتوژن است. متاستاز(از یونانی. متاستاز- حرکت) به انتقال آمبولی های خونی حاوی عناصری گفته می شود که قادر به رشد و نمو در محل انتقال هستند. تمرکز حاصل از این انتقال نامیده می شود متاستاز
آمبولی جسم خارجیهنگامی مشاهده می شود که قطعات گلوله و مین، گلوله و سایر اجسام به مجرای عروق بزرگ برخورد می کنند. با توجه به اینکه جرم چنین اجسام خارجی زیاد است، بخش های کوچکی از جریان خون را به عنوان مثال از ورید اجوف فوقانی به سمت قلب راست عبور می دهند. "آمبولی شدید"، به دلایل واضح، می تواند منجر به آمبولی رتروگراد شود، یعنی E. بر خلاف جریان خون، به عنوان مثال، از ورید اجوف فوقانی یا تحتانی به تنه وریدی زیرین فرود می آیند. آمبولی توسط اجسام خارجی شامل آمبولی با آهک و کریستال های کلسترول پلاک های آترواسکلروتیک است که در هنگام زخم شدن در مجرای رگ فرو می ریزند.
معنی.آمبولی بسیاری از بیماری ها را پیچیده می کند. فقط آمبولی گاز ماهیت و تظاهرات یک بیماری مستقل است - بیماری رفع فشار. با این حال، اهمیت آمبولی به عنوان یک عارضه مبهم است و با توجه به نوع آمبولی، شیوع آمبولی و محلی سازی آنها مشخص می شود. عوارض ترومبوآمبولی و مهمتر از همه آمبولی ریه که منجر به مرگ ناگهانی می شود از اهمیت بالینی بالایی برخوردار است. ترومبوآمبولی شریان های دایره بزرگ است دلیل مشترکتوسعه انفارکتوس مغزی، کلیه ها، طحال، گانگرن روده، اندام ها. اغلب در چنین مواردی، سندرم ترومبوآمبولیک رخ می دهد که درمان آن دشوار است. برای کلینیک، آمبولی باکتریایی به عنوان مکانیسمی برای گسترش عفونت چرکی و یکی از بارزترین تظاهرات سپسیس مهم نیست. همان را باید در مورد آمبولی سلول های تومور بدخیم به عنوان پایه متاستاز آنها گفت. اهمیت آمبولی هوا و چربی کم است، اما در برخی موارد می تواند کشنده باشد.
شوکه شدن
شوکه شدن(از فرانسوی. choc)- یک فرآیند پاتولوژیک حاد در حال توسعه، ناشی از عمل یک محرک فوق قوی و با نقض فعالیت سیستم عصبی مرکزی، متابولیسم و مهمتر از همه، تنظیم خودکار سیستم گردش خون، که منجر به تغییرات مخرب در اندام ها و بافت ها می شود. .
شوک با ریشه های مختلف بر اساس یک مکانیسم تک فازی پیچیده تکوین است. اما برای دوره اولیهشوک با علائم نسبتاً خاص به دلیل ویژگی های علت و پاتوژنز مشخص می شود.
بر این اساس، انواع شوک زیر مشخص می شود: 1) هیپوولمیک، که بر اساس کاهش حاد حجم خون (یا مایع) در گردش است. 2) تروماتیک، مکانیسم تحریک آن تکانه های آوران بیش از حد (عمدتا دردناک) است. 3) کاردیوژنیک، ناشی از کاهش سریع عملکرد انقباضی میوکارد و افزایش جریان تکانه های آوران (عمدتا "هیپوکسیک"). 4) سپتیک (سمی-عفونی) ناشی از اندوتوکسین های میکرو فلور بیماری زا.
در اواخر دوره شوک، ویژگی نسبی علائم ناشی از ویژگی های علت و پاتوژنز آن ناپدید می شود، تظاهرات بالینی و مورفولوژیکی آن تبدیل به کلیشه می شود.
برای تصویر مورفولوژیکی شوک با نقض انعقاد خون به شکل انعقاد داخل عروقی منتشر، دیاتز هموراژیک، خون جسد مایع مشخص می شود که می تواند مبنایی برای تشخیص شوک در کالبد شکافی باشد (Permyakov N.K.، 1979). از نظر میکروسکوپی، نقض همودینامیک و خواص رئولوژیکی خون با اسپاسم گسترده عروق، میکروترومبی در سیستم میکروسیرکولاسیون، علائم افزایش نفوذپذیری مویرگی، خونریزی نشان داده می شود. در اندام های داخلی، تعدادی از تغییرات کلی به شکل دیستروفی و نکروز ایجاد می شود که ناشی از اختلالات همودینامیک، هیپوکسی، اثر مخرب آمین های بیوژنیک، اندوتوکسین های میکرو فلور بیماری زا است. شدت این تغییرات تا حد زیادی امکان برگشت پذیری شوک را تعیین می کند.
تغییرات مورفولوژیکی شوک به دلیل تخصص ساختاری و عملکردی اندام و غلبه یکی از پیوندهای آن در پاتوژنز شوک - نوروفلکس، هیپوکسیک، سمی، می تواند دارای تعدادی ویژگی باشد.
با هدایت این ماده، اصطلاح "ارگان شوک" برای توصیف شوک استفاده شد.
V کلیه شوکقسمت های سنگین نفرون - لوله های پروگزیمال - دچار تغییرات شدید دیستروفیک و نکروز می شوند. نفروز نکروزان (گاهی اوقات نکروز متقارن قشر کلیه ها) ایجاد می شود که باعث نارسایی حاد کلیه در شوک می شود. V شوک کبدهپاتوسیت ها گلیکوژن را از دست می دهند، دچار دژنراسیون هیدروپیک می شوند، نکروز مرکز لوبولار کبد ایجاد می شود، علائم نارسایی ساختاری و عملکردی رتیکولواندوتلیوسیت های ستاره ای ظاهر می شود. همه این تغییرات احتمال ایجاد نارسایی حاد کبدی در شوک را تعیین می کند. در همان زمان، اغلب ترکیبی از نارسایی کلیه و کبد وجود دارد، سپس آنها در مورد صحبت می کنند سندرم کبدی
شوک ریهبا کانون های آتلکتازی، ادم هموراژیک سروزی همراه با از دست دادن فیبرین در لومن آلوئول ها، هموستاز و لخته شدن خون در عروق میکروسکولار مشخص می شود که باعث ایجاد نارسایی حاد تنفسی می شود.
ساختاری تغییرات میوکارد در شوکبا تغییرات دیستروفیک و نکروبیوتیک در کاردیومیست ها نشان داده می شود: ناپدید شدن گلیکوژن، ظاهر لیپیدها و انقباضات میوفیبریل ها. ظهور کانون های کوچک نکروز امکان پذیر است.
آسیب ساختاری مشخص در هنگام شوک نه تنها در اندام های شوک، بلکه در داخل نیز تشخیص داده می شود دستگاه گوارش، سیستم عصبی، غدد درون ریز و ایمنی.
اختلالات گردش خون لنفاوی
اختلالات گردش خون لنفاویبه شکل نارسایی آن آشکار می شود که اشکال آن می تواند متفاوت باشد.
سیستم لنفاوی برای حفظ تعادل متابولیک بین خون و بافت عمل می کند و با جذب آب و مواد با وزن مولکولی بالا (پروتئین ها، لیپیدهای امولسیون شده و غیره) از بافت ها عملکرد تخلیه را انجام می دهد.
بین نارسایی مکانیکی، دینامیکی و تحلیلی سیستم لنفاوی تمایز قائل شوید.
نقص مکانیکیدر ارتباط با تأثیر عواملی است که جریان لنف را مختل می کند و منجر به رکود آن می شود. این شامل فشرده سازی یا انسداد عروق لنفاوی، انسداد است گره های لنفاویبه عنوان مثال سلول های سرطانی، خارج شدن مجرای قفسه سینه یا غدد لنفاوی، نارسایی دریچه های عروق لنفاوی.
شکست دینامیکیبه دلیل افزایش فیلتراسیون در مویرگ ها ظاهر می شود. در این موارد، عروق لنفاوی قادر به خارج کردن مایع ادماتوز از بینابینی نیستند.
نارسایی جذبسیستم لنفاوی در نتیجه تغییر در خواص بیوشیمیایی و پراکنده پروتئین های بافت یا کاهش نفوذپذیری مویرگ های لنفاوی ایجاد می شود که منجر به رکود مایع در بافت ها می شود. در اکثریت قریب به اتفاق موارد، اشکال ترکیبی نارسایی گردش لنفاوی وجود دارد.
تظاهرات مورفولوژیکینارسایی سیستم لنفاوی، صرف نظر از شکل آن، مشخصه است (Zerbino D.D.، 1974). این موارد عبارتند از: رکود لنف و گسترش عروق لنفاوی. توسعه گردش لنفاوی جانبی و بازسازی مویرگ های لنفاوی و عروق خونی؛ تشکیل لنفانژکتازی؛ توسعه لنف ادم، استاز لنفاوی و تشکیل منعقد کننده های پروتئین (لخته شدن خون)؛ لنفوره (کیلوره)؛ تشکیل کیلوس آسیت، شیلوتوراکس. این تغییرات مورفولوژیکی منعکس کننده مراحل متوالی در ایجاد نارسایی لنفاوی است.
احتقان لنف و اتساع عروق لنفاوی- اولین تظاهرات اختلال درناژ لنفاوی، که در مواردی رخ می دهد که بیشتر مسیرهای لنفاوی منحرف مسدود شده است. رکود لنف منجر به گنجاندن واکنش های تطبیقی، توسعه می شود گردش لنفاوی جانبیدر این مورد، نه تنها استفاده از وثیقه های ذخیره رخ می دهد، بلکه نئوپلاسم مویرگ ها و عروق لنفاوی و بازسازی ساختار آنها نیز رخ می دهد. از آنجایی که قابلیت های پلاستیکی سیستم لنفاوی بسیار زیاد است، کمبود گردش لنفاوی را می توان برای مدت طولانی جبران کرد. با این حال، سازگاری سیستم لنفاوی در شرایط افزایش رکود لنفاوی در طول زمان ناکافی است. سپس بسیاری از مویرگ ها و رگ های خونی از لنف سرریز می شوند و به حفره های عریض با دیواره نازک تبدیل می شوند. (لنفانژکتازی).برآمدگی های متعدد دیوار در رگ های تخلیه ظاهر می شود - رگهای واریسیعروق لنفاوی.عدم جبران گردش خون لنفاوی شروع می شود که بیان آن ادم لنفوژن یا لنف ادم است.
لنف ادم(لنف یونانی. اودائو- ورم می کنم) در برخی موارد حاد (لنف ادم حاد) وجود دارد، اما بیشتر اوقات سیر مزمن دارد (لنف ادم مزمن). هر دو لنف ادم حاد و مزمن می توانند عمومی یا موضعی (منطقه ای) باشند.
لنف ادم عمومی حادنادر است، به عنوان مثال، در ترومبوز دو طرفه ورید ساب کلاوین. در این موارد، با افزایش فشار وریدی در ورید اجوف در مجرای قفسه سینه، استاز رتروگراد ایجاد می شود که تا مویرگ های لنفاوی گسترش می یابد. لنف ادم ژنرالیزه مزمن- یک پدیده طبیعی در استاز وریدی مزمن، به عنوان مثال. با نارسایی مزمن گردش خون، و بنابراین اهمیت بالینی زیادی دارد.
لنف ادم حاد موضعی (منطقه ای).با انسداد رگ های لنفاوی تخلیه (به عنوان مثال، آمبولی سرطان) یا فشرده سازی (بسته شدن در حین جراحی)، با لنفادنیت حاد، از بین رفتن غدد لنفاوی و عروق و غیره رخ می دهد. به محض ایجاد گردش خون جانبی لنفاوی ناپدید می شود. اهمیت بالینی مستقل است لنف ادم مزمن موضعی (منطقه ای)،که به مادرزادی و اکتسابی تقسیم می شود. مادرزادی معمولاً با هیپوپلازی یا آپلازی عروق لنفاوی اندام تحتانی همراه است. به دست آورد - در ارتباط با فشرده شدن (تومور) یا متروک شدن (التهاب مزمن، اسکلروز) عروق لنفاوی، با التهاب مزمن، اسکلروز یا برداشتن گروه بزرگی از غدد لنفاوی (به عنوان مثال، در طی یک عمل رادیکال برای برداشتن غده پستانی). ترومبوز وریدی، ترومبوفلبیت، تشکیل فیستول شریانی وریدی و غیره. احتقان مزمن لنفاوی منجر به هیپوکسی بافتی می شود و به همین دلیل است اسکلوژنیکعمل. در شرایط افزایش هیپوکسی، فعالیت کلاژن سازی فیبروبلاست ها و تکثیر آنها افزایش می یابد. منسوجات،
بیشتر اوقات پوست و بافت زیر جلدی اندام ها افزایش حجم پیدا می کند ، متراکم می شود ، شکل قبلی خود را از دست می دهد ، ظاهر ، تغییرات ایجاد می شود ، به نام فیل(شکل 62).
در پس زمینه لنف ادم ظاهر می شود استاز لنفاوی(لنفوستاز)، که می تواند از یک طرف منجر به تشکیل منعقد کننده های پروتئین در عروق لنفاوی شود - لخته شدن خون،و از طرف دیگر افزایش نفوذپذیری و حتی پارگی مویرگ ها و عروق لنفاوی که با توسعه همراه است. لنفوره(لنفوراژی). تمیز دادن لنفوره خارجی،هنگامی که لنف به محیط خارجی می رود، و لنفوره داخلی- با جریان لنف در بافت یا حفره بدن. ایجاد کیلوس آسیت و شیلوتوراکس با لنفوره داخلی همراه است.
آسیت شیلوس- تجمع
مایع شیلوس (لنف با محتوای چربی بالا) در حفره شکمی با رکود شدید لنف در اندام های شکمی یا با آسیب به عروق لنفاوی روده و مزانتر آن. مایع چیلوس مانند شیر سفید است.
شیلوتوراکس- تجمع مایع شیلوس در حفره پلوربه دلیل آسیب به مجرای قفسه سینه، انسداد توسط ترومبوز یا فشرده شدن توسط یک تومور.
پیامدها و اهمیتنارسایی سیستم لنفاوی در درجه اول با اختلالات متابولیسم بافت تعیین می شود، که منجر به نارسایی نه تنها لنفاوی، بلکه همچنین سیستم وریدی (استاز وریدی) می شود. در نتیجه این اختلالات، هیپوکسی بافتی رخ می دهد که هم تغییرات دیستروفیک و هم نکروبیوتیک در لنف ادم حاد و تغییرات آتروفیک و اسکلروتیک در احتقان مزمن لنفاوی عمدتاً با آن همراه است. هیپوکسی باعث می شود تغییرات در اندام ها و بافت ها در طول رکود لنف و خون اساساً کلیشه ای و بدون ابهام باشد. با توجه به وحدت ساختاری و عملکردی غدد لنفاوی و سیستم گردش خون، می توان تعدادی از مکانیسم های بیماری زایی مشترک و مرتبط را که این سیستم ها را در توسعه بسیاری از فرآیندهای پاتولوژیک متحد می کند، درک کرد.
 اختلال در محتوای مایع بافتی
اختلال در محتوای مایع بافتی
محتوای مایع بافت در درجه اول به وضعیت گردش خون و لنف و سطح نفوذپذیری بافت عروقی بستگی دارد. همچنین با وضعیت خون و لنف، سلول ها و ماده بین سلولی، جایی که مایع بافتی تجمع می یابد، تعیین می شود. محتوای مایع بافت توسط مکانیسم های عصبی-هومورال تنظیم می شود. در عین حال، اهمیت زیادی به آلدوسترون و هورمون ضد ادراری غده هیپوفیز داده می شود.
مایع بافتی از نظر پروتئین (تا 1٪) فقیر است و در سلول ها با کلوئیدهای پروتئینی و در بافت همبند - با پروتئین ها و گلیکوزآمینوگلیکان های ماده اصلی مرتبط است. جرم اصلی آن در ماده بین سلولی است. نقض محتوای مایع بافت در افزایش یا کاهش آن بیان می شود.
افزایش محتوای مایع بافتاین تخلف منجر به توسعه می شود ادمیا آبریزشدر همان زمان، در بافت ها یا در حفره های بدن تجمع می یابد مایع ادماتیکیا ترانسودات(از لات ترانس- در عرض، سودو، سوداتوم- عرق، تراوش). این مایع شفاف است، حاوی بیش از 2٪ پروتئین نیست و با کلوئیدهای پروتئینی پیوند ضعیفی دارد. تجمع مایع ادماتوز در بافت زیر جلدی نامیده می شود آنسارکاس(از یونانی. آنا- بیش از و سارکوس- گوشت)، در حفره پیراهن قلب - هیدروپریکارد،در حفره پلور - هیدروتوراکس،در حفره شکم - آسیت(از یونانی. آسکو- کیسه)، در حفره غشای واژن بیضه - هیدروسل
ظاهر.با ادم، ظاهر بافت ها و اندام ها مشخص است. ادم روی پوست در بافت همبند شل زیر جلدی، عمدتاً روی پوست پلک ها، زیر چشم ها، پشت دست ها، روی مچ پا ظاهر می شود و سپس به تدریج به کل بدن گسترش می یابد. پوست رنگ پریده می شود، گویی کشیده می شود، چین و چروک ها و چین ها صاف می شوند، با فشار، فرورفتگی هایی که برای مدت طولانی ناپدید نمی شوند، باقی می مانند. هنگامی که چنین پوستی بریده می شود، یک مایع شفاف آزاد می شود. بافت چربی زرد کم رنگ، براق و لزج می شود. ریه ها با ادم شدید، افزایش اندازه، قوام خمیری به دست می آید، مقدار زیادی مایع کف شفاف از سطح برش جریان می یابد. مغز بزرگ شده، فضاهای ساب عنکبوتیه و بطن ها متسع شده اند مایع شفاف... ماده مغز روی بریدگی می تابد، خونی که از مویرگ ها به دلیل ادم پریکاپیلاری جریان دارد، به سرعت در سطح برش پخش می شود. ادم مغزی اغلب با تورم همراه است که در برخی موارد غالب است. هنگامی که مغز متورم می شود، هیدراتاسیون شدید ماده آن (به ویژه سفید) وجود دارد، پیچش ها صاف می شوند، حفره های بطن ها کاهش می یابد. وقتی مغز بریده می شود، صفحه چاقو به سطح برش خورده می چسبد. افزایش فشار داخل مغزی و داخل جمجمه ای وجود دارد که منجر به فرو رفتن مخچه در سوراخ مگنوم می شود. کلیه با افزایش ادم، کپسول برداشته می شود
به راحتی قابل خواندن هستند، روی سطح و برش رنگ پریده هستند. غشاهای مخاطی متورم، شفاف، ژلاتینی.
آزمایش میکروسکوپی.مایع ادماتوز زیادی در ماده بینابینی وجود دارد، سلول ها، کلاژن، الیاف الاستیک و رتیکولار را هل می دهد، آنها را به فیبرهای نازک تر تقسیم می کند. سلول ها توسط مایع ادماتوز فشرده می شوند یا متورم می شوند، واکوئل ها در سیتوپلاسم و هسته آنها ظاهر می شوند، تغییرات نکروبیوتیک در سلول ها ظاهر می شود و می میرند. در حفره های سروزی، تورم مشاهده می شود، و سپس لایه برداری مزوتلیوم. گاهی اوقات به صورت لایه لایه می ریزد. اغلب، دیواره های مویرگ های لنفاوی متسع پاره می شود که منجر به لنفوراژی و مخلوط شدن لنف با مایع ادماتوز می شود. V ریه ها مایع ادماتوز در بافت بینابینی و سپس در آلوئول ها تجمع می یابد مغز - اطراف رگ های خونی و سلول ها (ادم اطراف عروقی و اطراف سلولی)؛ با تورم مغز، تخریب فیبرهای گلیال، تجزیه میلین، تورم آستروسیت ها مشاهده می شود. V کبد ادم مجاری پورتال و فضاهای پری سینوسی را درگیر می کند کلیه ها - بینابینی، در درجه اول مدولا.
مکانیسم توسعهدر میان عواملی که ایجاد ادم را تعیین می کند، فشار هیدرواستاتیک خون و فشار اسمزی کلوئیدی پلاسمای آن، نفوذپذیری دیواره مویرگی و احتباس الکترولیت ها و آب (یا لنف) نقش اصلی را ایفا می کند. اغلب یک عامل جایگزین یا تکمیل می شود.
در بالا بردنفشار هیدرواستاتیک در ریزرگ ها باعث افزایش فیلتراسیون مایع می شود که منجر به احتباس آن در بافت ها می شود. بوجود امدن مکانیکی،یا احتقانی، تورمکاهش در مقدار فشار کلوئیدی اسمزی پلاسما منجر به ایجاد ادم انکوتیکبا افزایش نفوذپذیری دیواره مویرگی، ادم در درجه اول با آسیب به غشاهای مویرگی همراه است که از دست دادن پروتئین های پلاسما و تجمع آنها در بافت ها را تعیین می کند. چنین ادمی نامیده می شود غشا زادر بسیاری از بیماری ها، نقش اصلی در ایجاد ادم با تاخیر فعال در بافت های الکترولیت ها، عمدتاً سدیم و آب، ایفا می شود. اغلب، ادم با رکود لنف رخ می دهد - ادم لنفاوی
عواملی که منجر به ایجاد ادم می شوند در بسیاری از بیماری ها ظاهر می شوند: بیماری های سیستم قلبی عروقی، بیماری های آلرژیک، برخی عفونت ها و مسمومیت ها، بیماری های کلیه، کبد، روده ها، آسیب شناسی بارداری. ادم با ترومبوز وریدی، احتقان لنفاوی، اختلالات تروفیسم عصبی، تروما، التهاب رخ می دهد.
طبقه بندی.بسته به بیماری یا فرآیند پاتولوژیکی که باعث ایجاد ادم شده است و به میزان کمتری به علت آن، انواع زیر از ادم متمایز می شود: احتقانی، قلبی، کلیوی، دیستروفیک، مارانتیک (کاهکتیک)، التهابی، آلرژیک، سمی، عصبی، پس از سانحه.
ادم احتقانیبا فلبوترومبوز، ترومبوفلبیت، فشرده سازی وریدها، با لنفوستاز رخ می دهد و معمولاً محدود و موضعی است.
شخصیت. آنها به دلیل احتقان وریدی طولانی مدت ایجاد می شوند که باعث افزایش فشار در وریدها، هیپوکسی بافتی می شود که منجر به آسیب به اندوتلیوم و غشای پایه مویرگ ها، افزایش نفوذپذیری مویرگی و خارج شدن قسمت مایع خون به داخل رگ ها می شود. بافت. تضعیف عملکرد سیستم لنفاوی به افزایش ادم کمک می کند.
ادم قلبیمشاهده شده با جبران بیماری قلبی، نه صرفا راکد. توزیع مجدد خون منجر به افزایش ترشح آلدوسترون و تخریب ناکافی آن در کبد در هنگام رکود می شود. آلدوسترونمی احتباس سدیم را تعیین می کند که به رشد ادم کمک می کند.
در حال توسعه ادم کلیههر دو عامل انکوتیک و احتباس سدیم مهم هستند، اما نقش هر دو در بیماری های کلیوی مختلف متفاوت است. در سندرم نفروتیک از هر پیدایش، که با از دست دادن مقادیر زیادی پروتئین در ادرار (پروتئینوری) و تخلیه آنها از پلاسمای خون (هیپوپروتئینمی) مشخص می شود، نقش اصلی در ایجاد ادم مربوط به کاهش فشار خون انکوتیک است. در گلومرولونفریت، احتباس سدیم و به میزان کمتر فشار انکوتیک اهمیت اولیه دارد. ادم کلیوی در درجه اول روی صورت ظاهر می شود - روی پلک ها، زیر چشم ها، سپس به دست ها و پاها گسترش می یابد.
ادم دیستروفیکبه دلیل محتوای ناکافی پروتئین در غذا ایجاد می شود. هیپوپروتئینمی حاصل منجر به کاهش فشار خون انکوتیک می شود. این نیز شامل می شود ادم مرانت (کاهکتیک). ادم التهابیمشاهده شده در اطراف کانون التهاب (به اصطلاح ادم پری فوکال)، به دلیل افزایش نفوذپذیری غشاهای مویرگی است. مکانیسم هم همین است آلرژیک، سمی، عصبیو ادم تروماتیک
بنابراین، ادم ناشی از دلایل مختلفبا بیماری ها و فرآیندهای پاتولوژیک مختلف، اغلب مکانیسم های مشترکی دارند.
خروجدر بسیاری از موارد، نتیجه: ممکن است مطلوب باشد - مایع ادماتوز حل می شود. با ادم طولانی مدت، هیپوکسی در بافت ها ایجاد می شود که منجر به دیستروفی و آتروفی سلول های پارانشیم و ایجاد اسکلروز می شود.
معنی ادم با علت، محلی سازی، شیوع آنها تعیین می شود. برای مثال ادم آلرژیک گذرا است. ادم قلبی و کلیوی برای مدت طولانی وجود دارد و نتیجه بیماری اغلب به آنها بستگی دارد. ادم مغز یا ریه اغلب علت مرگ است، افتادگی حفره ها منجر به اختلال در فعالیت اندام ها می شود.
در بافت های ادماتوز، التهاب، نکروز، زخم اغلب رخ می دهد که با اختلالات تروفیک، خود عفونت همراه است. به همین دلیل، ترانسودات در حفره های بدن می تواند مبنایی برای تشکیل یک مایع التهابی باشد، به عنوان مثال. وارد اگزودا شوید (به عنوان مثال، ایجاد پریتونیت در پس زمینه آسیت - آسیت-پریتونیت).
کاهش محتوای مایع بافت.این تخلف نامیده می شود کم آبی (کم آبی)یا اگزیکوزیس(از لات بیماری- خشک)، همراه با از دست دادن خون آب، یعنی. آنهیدرمی
ظاهرافراد مبتلا به اگزیکوز بسیار مشخص هستند: بینی نوک تیز، چشم های فرورفته، گونه ها، پوست چروکیده، شل، لاغری شدید. در این مورد، خون غلیظ و تیره می شود، سطح غشاهای سروزی - خشک یا پوشیده از یک توده چسبناک موکوس مانند. اندام ها کاهش می یابد، کپسول آنها چروک می شود. اگزیکوز با از دست دادن سریع مقدار زیادی مایع رخ می دهد که مشخصه وبا، اسهال طولانی مدت، سوء هاضمه است. گاهی کم آبی زمانی رخ می دهد که کمابه عنوان مثال، با آنسفالیت.
آسیب شناسی عمومی اختلالات گردش خون و CSF
سیستم گردش خون، اندامها و سیستمهای مختلف عملکردی را به منظور حفظ حیات بدن بهعنوان یک کل، هماهنگ و به هم پیوند میدهد. سیستم گردش خون این عملکرد هماهنگ کننده را در رابطه با هموستاز در اتحاد نزدیک انجام می دهد سیستم لنفاوی... تمام بافتهای بدن توسط مایع بافتی شسته میشوند که مواد مغذی و اکسیژن را از خون شریانی به آنها میرساند و محصولات متابولیسم بافت و دیاکسید کربن توسط سیاهرگها و عروق لنفاوی منتقل میشود. بنابراین، ترکیب مایع بینابینی به طور مداوم به روز می شود. سیستم گردش خون لنفاوی، از یک سو، یک سیستم زهکشی است که محصولات متابولیسم بافت را جذب و به داخل سیاهرگ ها می برد. از طرف دیگر، بخشی از سیستم خونی است که ارتباط نزدیکی با فرآیندهای متابولیک دارد.
بنابراین، گردش خون از نظر ساختاری و عملکردی با تخلیه لنفاوی مرتبط است. بنابراین، اختلالات گردش خون را نمی توان جدا از اختلالات گردش لنفاوی و وضعیت سیستم خون در نظر گرفت، که به نوبه خود با وضعیت مورفو-عملکردی اندام های خونساز همراه است. هر دو سیستم (گردش خون و لنفاوی) یک عملکرد تبادل-انتقال را انجام می دهند و یک هدف واحد را انجام می دهند - ارائه تبادل بین مویرگ ها در همه اندام ها و بافت ها در سطح عروق ریز.
اطمینان از جریان خون کافی فرآیند پیچیده ای است که به عملکرد مناسب قلب، یکپارچگی عروق و تعادل دقیق بین سیستم های انعقادی و ضد انعقاد خون بستگی دارد.
با توجه به شیوع و محلی شدن فرآیند، اختلالات گردش خون به کلی و موضعی تقسیم می شوند. اختلالات عمومی در سراسر بدن، کل سیستم گردش خون رخ می دهد و با اختلال در فعالیت قلب یا تغییر در حجم و خواص فیزیکوشیمیایی خون همراه است.
اختلالات موضعی گردش خون و لنف ناشی از آسیب ساختاری و عملکردی به بستر عروقی در هر یک از بخش های آن - در یک اندام، بخشی از یک اندام یا بخشی از بدن است.
تقسیم اختلالات گردش خون به کلی و محلی مشروط است و باید از جنبه وحدت دیالکتیکی محلی و عمومی فهمید. به عنوان مثال، کاهش فشار خون در آئورت با کم خونی حاد عمومی منجر به کاهش خون رسانی به قشر کلیه می شود که سیستم رنین-آنژیوتانسین را فعال می کند و به نوبه خود باعث افزایش فشار در همان آئورت می شود. در بیشتر موارد، اختلالات گردش خون موضعی نتیجه اختلالات گردش خون عمومی است. بنابراین، با احتقان وریدی عمومی، ترومبوز وریدی اندام تحتانی اغلب ایجاد می شود. به نوبه خود، اختلالات گردش خون موضعی می تواند علت اختلالات عمومی باشد. انفارکتوس میوکارد علت نارسایی قلبی است که بستر مورفولوژیکی آن مجموعه وریدی عمومی است. خونریزی به عنوان یک فرآیند موضعی می تواند علت کم خونی حاد عمومی باشد. از این قبیل نمونه ها زیاد است.
یک فرآیند پاتولوژیک کلی وجود ندارد که در آن اختلالات گردش خون یا پیامد یا نتیجه آن نباشد و یا از این روند حمایت و تضمین نکند. تقریباً تمام بیماری های شناخته شده با اختلالات جریان خون با شدت های مختلف همراه هستند. همه موارد فوق ارتباط این موضوع را تعیین می کند، زیرا دانش به دست آمده برای تسلط بر همه رشته های بالینی ضروری است.
هدف از آموزش این است که بتوان با علائم ماکرو و میکروسکوپی انواع مختلف اختلالات گردش خون عمومی و موضعی را شناسایی کرد، علل و مکانیسم ایجاد آنها را توضیح داد و آنها را ارزیابی کرد. نتیجه احتمالیو اهمیت این فرآیندها را برای بدن تعیین کنید.
چرا باید بتوانید:
تظاهرات ماکرو و میکروسکوپی ورید مشترک را تعیین کنید
مجموعه، دلایل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آن را توضیح دهد.
تعیین تظاهرات ماکرو و میکروسکوپی مجموعه شریانی عمومی، توضیح علل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آن.
تعیین تظاهرات ماکرو و میکروسکوپی کم خونی حاد و مزمن عمومی، توضیح علل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آنها.
تعیین تظاهرات ماکرو و میکروسکوپی ضخیم شدن و نازک شدن خون، توضیح علل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آنها.
تعیین تظاهرات ماکرو و میکروسکوپی شوک، توضیح علل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آن.
تعیین تظاهرات ماکرو و میکروسکوپی انعقاد داخل عروقی منتشر (DIC)، توضیح علل، مکانیسم توسعه، نتیجه و ارزیابی اهمیت آن.
اختلالات عمومی گردش خون
اختلالات رایج گردش خون عبارتند از:
مجموعه شریانی عمومی؛
احتقان وریدی عمومی؛
کم خونی عمومی - حاد و مزمن؛
غلیظ شدن خون؛
رقیق شدن خون؛
انعقاد داخل عروقی منتشر (انعقاد داخل عروقی منتشر).
کل خون کامل شریانی
(هیپرمی جهانی آرتریوزا)
پرخونی عمومی شریانی یا پرخونی شریانی، افزایش تعداد گلبول های خون (گلبول های قرمز) است که گاهی اوقات
همراه با افزایش حجم خون در گردش. این روند نسبتاً نادر است: هنگام صعود به ارتفاع (در بین کوهنوردان)، در میان ساکنان مناطق کوهستانی، در افراد مبتلا به آسیب شناسی ریه، و همچنین در نوزادان پس از بستن بند ناف. از نظر بالینی، قرمزی پوست و غشاهای مخاطی، افزایش فشار خون وجود دارد. در عمل، بیشترین اهمیت فراوانی شریانی عمومی در بیماری واکز (پلی سیتمی ورا) است - بیماری که در آن تولید بیش از حد واقعی گلبول های قرمز وجود دارد.
خون وریدهای عمومی
(هیپرمی یونیورسالیس ونوزا)
پرده وریدی عمومی یکی از شایع ترین انواع اختلالات گردش خون عمومی است و تظاهرات بالینی و مورفولوژیکی نارسایی قلبی یا ریوی قلب است.
ماهیت پاتوفیزیولوژیکی و پاتومورفولوژیکی احتقان وریدی عمومی شامل توزیع مجدد حجم خون در گردش عمومی با تجمع آن در قسمت وریدی گردش خون سیستمیک (وریدهای توخالی و گاهی اوقات در عروق ریه) و کاهش شریانی است. بخش
در مکانیسم ایجاد (یعنی در پاتوژنز) احتقان وریدی عمومی، سه عامل اصلی زیر نقش دارند:
نارسایی قلبی که به آن نارسایی قلبی گفته می شود، علل آن می تواند موارد زیر باشد:
نقایص اکتسابی و مادرزادی قلب؛
بیماری التهابی قلب (پریکاردیت، میوکاردیت، اندوکاردیت)؛
کاردیواسکلروز با علل مختلف (آترواسکلروتیک، پس از انفارکتوس و غیره)؛
انفارکتوس میوکارد و غیره
بیماری های ریوی همراه با کاهش حجم رگ های گردش خون ریوی:
آمفیزم ریه؛
پنومونی مزمن غیر اختصاصی؛
پنوموسکلروز با علل مختلف؛
پنوموکونیوز (بیماری های ریوی گرد و غبار) و غیره
آسیب به قفسه سینه، جنب و دیافراگم، همراه با اختلال در عملکرد مکش قفسه سینه:
پلورز (از جمله چسب)؛
پنوموتوراکس؛
تغییر شکل قفسه سینه و ستون فقرات.
احتقان وریدی عمومی می تواند در دوره بالینی حاد و مزمن باشد.
توده ورید عمومی حاد تظاهر سندرم نارسایی حاد قلبی و هیپوکسی (خفگی) است. می تواند ناشی از:
انفارکتوس میوکارد؛
میوکاردیت حاد؛
پلورزی اگزوداتیو حاد با تجمع بیش از حد پلورال افیوژن، فشرده سازی ریه ها.
ایستادن زیاد دیافراگم (با پریتونیت)، محدود کردن تنفس.
آمبولی ریه؛
پنوموتوراکس؛
انواع آسفیکسی
در نتیجه هیپوکسی، سد هیستوهماتوژن آسیب می بیند و نفوذپذیری مویرگی به شدت افزایش می یابد. در بافت ها استاز وریدی، اشباع پلاسما (پلاسموراژ)، ادم، استاز در مویرگ ها و خونریزی های دیاپدی متعدد مشاهده می شود. تغییرات دیستروفیک و نکروز در اندام های پارانشیمی ظاهر می شود. مشخص ترین تغییرات مورفولوژیکی در توده وریدی حاد عمومی در ریه ها و در کبد ایجاد می شود.
علت احتقان وریدی ریه ها نارسایی قلبی بطن چپ است. احتقان حاد وریدی باعث گشاد شدن مویرگ های آلوئولی می شود که از نظر بالینی با خارج شدن مایع به داخل آلوئول ها (ادم ریوی) همراه است. خونریزی داخل آلوئولی نیز ممکن است رخ دهد. در کالبد شکافی، مقدار زیادی مایع مایل به صورتی متمایل به قرمز، ریز و کفی درشت از سطح برش ریه جاری می شود.
نارسایی قلب بطن راست باعث رکود در گردش خون سیستمیک می شود. در همان زمان، در کبد، گسترش وریدهای کبدی مرکزی و رکود در سینوسوئیدها در قسمت مرکزی لوبول کبدی وجود دارد. این نواحی مرکزی قرمز راکد با بافت نرمال و کم رنگ تر در نواحی محیطی متناوب می شوند و الگوی عجیبی را ایجاد می کنند که یادآور جوز هندی است (به نام جوز هندی).
در کبد، به دلیل ویژگی های معماری لوبول کبدی و گردش خون آن، با توده وریدی حاد، خونریزی های مرکز لوبولار و نکروز ظاهر می شود.
توده وریدی عمومی مزمن در سندرم نارسایی قلبی مزمن (قلبی عروقی) یا ریوی ایجاد می شود. علل آن نقایص قلبی، بیماری ایسکمیک مزمن، میوکاردیت مزمن، کاردیومیوپاتی، آمفیزم ریوی، پنوموسکلروزیس با منشاء مختلف (اشکال سیروزی سل ریوی، ذات الریه مزمن، پنوموکونیوز)، انحنای ستون فقرات (قوز یا گیبوسیس در انواع مختلف کایفوزیس) است. ، لوردوز)، آلودگی یا محو شدن حفره های پلور با چسبندگی با پلوریت چسبنده و غیره.
تظاهرات بالینی و مورفولوژیکی احتقان وریدی عمومی مزمن.
در معاینه خارجی بیمار، چه با احتقان وریدی عمومی حاد و چه مزمن، رنگ سیانوتیک پوست (سیانوز) توجه را به خود جلب می کند، زیرا وریدهای پوست و بافت زیر جلدی گشاد شده و مملو از خون هستند. از طریق لایه شفاف اپیدرم، رنگ قرمز تیره خون وریدی رنگ مایل به آبی پیدا می کند. در انسان، بیشترین حجم خون در بافت زیر جلدی و سیاهرگ های اندام تحتانی رسوب می کند.
پوست، به خصوص اندام تحتانی، سرد می شود، سیانوز یا سیانوز به وضوح روی صورت در ناحیه بینی، لاله گوش، لب ها و همچنین در دست ها و پاها قابل مشاهده است: در ناحیه ناخن. تخت، نوک انگشتان سیانوز قسمت های بیرون زده بدن آکروسیانوز نامیده می شود.
ادم بیان شده (ادم) درم و بافت زیر جلدی به دلیل این واقعیت است که عروق لنفاوی نیز متسع و پر از لنف هستند. مایع ادماتیک ترانسودات (ترانسوداسیون - تراوش) نامیده می شود و حاوی مقدار کمی الکترولیت، کمتر از 2٪ پروتئین و سلول های خون و لنفاوی جدا شده است. در حفره های سروزی، تجمع بیش از حد مایع مشاهده می شود که به آن ادم حفره یا قطرات حفره ها می گویند. به افتادگی حفره شکم آسیت می گویند. افتادگی حفره های پلور - هیدروتوراکس، قطرات حفره پیراهن پریکارد - هیدروپریکارد.
ادم بافت چربی زیر جلدی کل بدن در ترکیب با قطرات حفره ها آنسارکا نامیده می شود.
سروز، مننژها و غشاهای مخاطی سیانوتیک هستند.
اندامها و بافتهای دارای توده وریدی حجمشان افزایش مییابد، به دلیل افزایش محتوای هموگلوبین کاهشیافته، سیانوتیک و به دلیل اختلال گردش خون لنفاوی و ادم متراکم میشوند و بعداً به دلیل تکثیر بافت همبند.
کبد و ریه ها در صورت گرفتگی وریدی عمومی ظاهر خاصی دارند.کبد در احتقان وریدی مزمن بزرگ، متراکم، لبه های آن گرد، سطح برش رنگارنگ، خاکستری مایل به زرد با لکه های قرمز تیره ("جوز هندی") است. دلیل چنین الگوی کبد چیست؟
اجازه دهید ابتدا برخی از داده های آناتومیکی در مورد سیستم وریدی کبد را یادآوری کنیم. کبد دارای دو سیستم وریدی است. یکی از ادوکتورها ورید باب است که خون را از اندام های جفت نشده حفره شکمی جمع آوری می کند. به موازات آن، خون شریانی از طریق شریان کبدی وارد کبد می شود. هر دو شریان و ورید، به همراه مجرای صفراوی بین لوبول های کبد، "سه گانه" معروف را تشکیل می دهند. در داخل لوبول، شاخه های وریدها و شریان ها با هم ادغام می شوند و یک رگ کوچک واحد را تشکیل می دهند - سینوسوئیدهای داخل سپتال (داخل لوبولار). بخش های انتهایی این سینوس ها وریدهای مرکزی را در مرکز لوبول ها تشکیل می دهند - این شروع سیستم وریدی وابران کبد است. خون از وریدهای مرکزی به وریدهای جمع کننده کبد و سپس به ورید اجوف تحتانی هدایت می شود.
با احتقان وریدی عمومی، احتقان وریدی در حال توسعه در ورید اجوف تحتانی به ترتیب ابتدا به وریدهای کبدی، سپس به وریدهای جمع کننده و مرکزی و تا حدی به سینوسوئیدهای لوبول کبدی گسترش می یابد. انبساط بیشتر مشاهده نمی شود، زیرا در شاخه های مویرگی شریان کبدی که به سینوس ها می ریزد، فشار همیشه بیشتر از سینوس ها است. بخشهای مرکزی لوبولها با خون کامل نه تنها از نظر میکروسکوپی، بلکه از نظر ماکروسکوپی نیز قابل مشاهده هستند. بخش های مرکزی لوبول روی برش کبد قرمز تیره ("جگر جوز هندی") به نظر می رسد. در حاشیه لوبولها، سلولهای کبدی در حالت دیستروفی، اغلب چرب هستند، که رنگ خاکستری مایل به زرد بافت کبد را توضیح میدهد (چنین کبدی قبلاً "کبد چرب جوز هندی" نامیده میشد). همانطور که توده وریدی در مرکز لوبول ها رشد می کند، خونریزی ظاهر می شود، سلول های کبدی در اینجا علاوه بر دیستروفی، نکروز و آتروفی دچار می شوند. سلول های کبدی در حاشیه لوبول ها هیپرتروفی جبرانی هستند. گرسنگی طولانی مدت اکسیژن همراه با پرخونی وریدی منجر به درشت شدن و تکثیر بافت همبند در اندام و تشکیل فیبروز احتقانی پیشرونده (اسکلروز، سیروز) کبد می شود. به این سیروز مسقطی، قلبی نیز گفته می شود، زیرا معمولاً در نارسایی مزمن قلبی رخ می دهد.
توجه داشته باشید که در تمام اندام های داخلی در هنگام استاز وریدی در نتیجه گرسنگی اکسیژن، درشت شدن، ضخیم شدن رشته های کلاژن استروما رخ می دهد و پدیده ای ایجاد می شود که معمولا به آن سفتی راکد یا سفتی سیانوتیک یک اندام می گویند، به عنوان مثال، سفتی سیانوتیک طحال، سفتی سیانوتیک کلیه ها.
در ریه ها با استاز وریدی طولانی مدت، به اصطلاح فشردگی قهوه ای ریه ها ایجاد می شود. این نتیجه نارسایی مزمن بطن چپ قلب است. هیپوکسی مشاهده شده با استاز وریدی، فشار خون بالادر داخل عروق منجر به نقض نفوذپذیری مویرگ ها و ونول ها می شود. گلبول های قرمز همراه با پلاسما وارد لومن آلوئول ها و سپتوم های بین آلوئولی می شوند، یعنی خونریزی های دیاپدی متعددی مشاهده می شود. در آلوئول ها و سپتوم های بین آلوئولی، گلبول های قرمز متلاشی شده و قطعات آنها توسط ماکروفاژها گرفته می شود. این سلول های مملو از هموسیدرین - سیدروبلاست ها و سیدروفاژها - به ریه ها رنگ قهوه ای می دهند. آنها سلول های "بیماری قلبی" نامیده می شوند. نام آنها به این دلیل است که احتقان در ریه ها اغلب با بیماری میترال مشاهده می شود.
علاوه بر این، در ریه ها، به دلیل هیپوکسی، بافت همبند در سپتوم بین آلوئولار رشد می کند.
بنابراین، با احتقان وریدی مزمن ریه ها، دو نوع تغییر ایجاد می شود:
پرفشاری احتقانی و فشار خون بالا در گردش خون ریوی، منجر به هیپوکسی و افزایش نفوذپذیری عروق، خونریزی دیاپدتیک، ایجاد هموسیدروز ریوی می شود.
تکثیر بافت همبند، یعنی اسکلروز.
ریه ها بزرگ، قهوه ای، متراکم می شوند - تراکم قهوه ای (یا استحکام) ریه ها.
خروج احتقان وریدی عمومی یک فرآیند برگشت پذیر است، مشروط بر اینکه علت آن به موقع از بین برود. به موقع یعنی چه؟ یعنی هنگام استفاده اقدامات درمانی(درمانی، جراحی، شکل گیری یک سبک زندگی منطقی و غیره) می توان فعالیت قلبی طبیعی را قبل از ایجاد فرآیندهای دیستروفی، آتروفیک و اسکلروتیک غیرقابل برگشت در اندام ها بازیابی کرد.
حالت حفظ طولانی مدت هیپوکسی بافتی همراه با توده وریدی عمومی مزمن منجر به تغییرات شدید و اغلب غیرقابل برگشت در اندام ها و بافت ها می شود. علاوه بر پلاسموراژ، ادم، استاز، خونریزی، دیستروفی و نکروز، تغییرات آتروفیک و اسکلروتیک در اندام ها ایجاد می شود. تغییرات اسکلروتیک، یعنی تکثیر بافت همبند، با این واقعیت مرتبط است که هیپوکسی مزمن باعث تحریک سنتز کلاژن توسط فیبروبلاست ها می شود. پارانشیم اندام آتروفی می شود و با بافت همبند جایگزین می شود، فشرده سازی راکد (استقامت) اندام ها و بافت ها ایجاد می شود.
معنی. مجموعه وریدی عمومی قطعاً ارزش منفی دارد، زیرا عملکرد اندام ها در شرایط گرسنگی طولانی مدت اکسیژن کاهش می یابد. این همیشه نشانگر ضعیف شدن کار قلب است.
بیماران بر اثر نارسایی قلبی جان خود را از دست می دهند.
به طور کلی خون پایین
(کم خونی جهانی)
بسته به علت و پاتوژنز، موارد زیر وجود دارد:
کم خونی حاد عمومی؛
کم خونی مزمن عمومی
خون کم حاد عمومی
(کم خونی جهانی حاد)
این وضعیتی است که با از دست دادن سریع خون، یعنی کاهش حجم خون در گردش (BCC) در گردش عمومی در مدت زمان کوتاهی ایجاد می شود.
علل کم خونی حاد عمومی: صدمات مختلف با آسیب به اندام ها، بافت ها و رگ های خونی.
پارگی خودبخودی رگ یا قلب بزرگ با تغییر پاتولوژیک (پارگی آنوریسم آئورت در سیفلیس، آترواسکلروز).
پارگی اندام تغییر یافته از نظر پاتولوژیک (پارگی لوله فالوپ در حاملگی خارج از رحم، پارگی طحال عفونی در مالاریا، تب عودکننده، از دست دادن خون گسترده در سل ریوی، زخم معده، سرطان با موقعیت های مختلف).
تظاهرات بالینی کم خونی حاد عمومی: رنگ پریدگی پوست و غشاهای مخاطی، سرگیجه، اغلب غش یا از دست دادن هوشیاری، نبض ضعیف مکرر، پایین بودن فشار خون... بیماران اغلب به دلیل کم خونی حاد جان خود را از دست می دهند. چرا مریض ها می میرند؟ به دلیل شوک هیپوولمیک.
تظاهرات پاتومورفولوژیک کم خونی حاد عمومی: در طی کالبد شکافی یک متوفی از کم خونی حاد عمومی، توجه به رنگ پریدگی شدید پوست، غشاهای مخاطی قابل مشاهده، غشاهای سروزی، بافت جلب می شود. اعضای داخلی... حفره های قلب و عروق بزرگ خالی است، طحال کوچک، چروکیده است. نشانه نسبتاً مشخص این روند خونریزی های نقطه ای و نقطه ای در زیر اندوکارد بطن چپ قلب (نقاط میناکوف) است.
نتیجه به دو شرایط بستگی دارد:
از مقدار خون از دست رفته؛
از میزان از دست دادن خون - با چه سرعتی از دست دادن خون رخ داده است.
اصولاً در صورتی که فرد خون زیادی از دست نداده باشد و خیلی سریع نباشد (یا اگر خون از دست رفته به اندازه کافی سریع و در حجم مورد نیاز با تزریق جت خون و جایگزین های خون جبران شده باشد) این یک فرآیند برگشت پذیر است. مکانیسم های جبرانی وارد عمل می شوند: خون از انبارهای خون به رگ های محیطی پرتاب می شود. تون عروق تغییر می کند - دیواره عروقی منقبض می شود. و به لطف این دو شرایط، بدن فشار خون را سازگار با زندگی حفظ می کند. با گذشت زمان، اندام های خونساز به طور فعال شروع به کار می کنند و نه تنها حجم خون، بلکه سلول های خون نیز دوباره پر می شود. اگر از دست دادن خون به سرعت ایجاد شود، مکانیسم های جبرانی زمان روشن شدن نداشته باشند، فشار خون و فشار خون روی دیواره های قلب به شدت کاهش می یابد، گیرنده ها تحریک نمی شوند و ایست قلبی رفلکس رخ می دهد.
معنی. خطر اصلی کم خونی حاد عمومی، اختلال همودینامیک است. اقدامات پزشک باید در جهت بازگرداندن حجم خون باشد.
خون کم مزمن عمومی
(کم خونی جهانی مزمن)
کم خونی مزمن عمومی یا کم خونی، کاهش تعداد گلبول های قرمز خون و/یا محتوای هموگلوبین در یک واحد حجمی خون است. حجم کل خون در گردش در بدن تغییر نمی کند. در پاتوژنز کم خونی مزمن عمومی، دو عامل مهم هستند:
اختلال در عملکرد اندام های خونساز؛
افزایش همولیز گلبول های قرمز
علل کم خونی مزمن عمومی:
بیماری های خود اندام های خونساز (هموبلاستوز، کم خونی)؛
بیماری های عفونی مزمن (سل، سیفلیس)؛
مسمومیت اگزوژن (مسمومیت با سرب، آرسنیک و فرآورده های آن، بنزن، مونوکسید کربن و غیره)؛
مسمومیت درون زا (مسمومیت با محصولات متابولیسم نیتروژن - با بیماری کلیوی، اسیدهای صفراوی با زردی انسدادی، سموم درون زا با تومورهای بدخیمو غیره.)؛
ناشتا (کامل یا جزئی)، کمبود ویتامین؛
از دست دادن خون کوچک، اما اغلب مکرر (با زخم معده و زخم اثنی عشر، سل ریوی، رحم و خونریزی هموروئیدی).
تظاهرات بالینی کم خونی مزمن عمومی: رنگ پریدگی، خستگی آسان، ضعف، کاهش عملکرد، سرگیجه، غش. در آزمایش خون - کاهش تعداد گلبول های قرمز و کاهش محتوای هموگلوبین.
تظاهرات پاتولوژیک کم خونی مزمن عمومی: رنگ پریدگی پوست، غشاهای مخاطی، اندام های داخلی. تغییرات دیستروفیک در اندام های پارانشیمی (به ویژه دژنراسیون چربی).
با افزایش همولیز گلبول های قرمز، هموسیدروز عمومی ایجاد می شود. در نتیجه هیپوکسی، خونریزی دیاپدتیک ممکن است رخ دهد.
نتیجه و معنا. در اصل، روند برگشت پذیر است. اما اگر علت از بین نرود و روند پیشرفت کند، می تواند منجر به مرگ شود. مرگ به دلیل اختلالات متابولیکی برگشت ناپذیر مرتبط با گرسنگی اکسیژن رخ می دهد.
ضخامت خون
(آنهیدرمی، inspisatio sanguinis)
غلیظ شدن خون عبارت است از کاهش خون در یک جزء مایع، یعنی کاهش محتوای آب و برخی الکترولیت ها در خون محیطی. در نتیجه خون غلیظ می شود، ویسکوزیته آن افزایش می یابد، خواص رئولوژیکی خون تغییر می کند و تعداد سلول ها در واحد حجم نسبتاً افزایش می یابد.
ضخیم شدن خون زمانی ایجاد می شود که مقدار زیادی مایع از بین برود.
علل غلیظ شدن خون:
اسهال و استفراغ مداوم (وبا، اشکال شدید اسهال خونی، سالمونلوز).
سوختگی های معمولی درجه دو، هنگامی که توده ای از مایع به تاول های سوختگی می رود.
مسمومیت با عوامل جنگ شیمیایی خفه کننده (CWA)، زمانی که یک فرد مسموم شده با گاز دچار بیماری شدید می شود. سوختگی شیمیاییریه ها و بافت ریه تا 10 لیتر مایع جمع می کنند - ادم ریوی سمی.
آسیب شناسی ایتروژنیک - دیورز اجباری ناکافی در صورت مسمومیت برای دفع محصولات سمی در ادرار در مواردی که این درمان به طور غیرقابل کنترل انجام می شود (بدون در نظر گرفتن نسبت حجم مایع ورودی و خروجی).
تظاهرات پاتولوژیک ضخیم شدن خون: خون غلیظ، چسبناک، تیره است، لخته های خون در رگ ها تشکیل می شود. به خصوص تغییرات قابل توجهی در ریز عروق با تشکیل لخته های خونی کوچک و پدیده لجن (چسباندن گلبول های قرمز به شکل ستون های سکه ای، چسباندن آنها به دیواره مویرگی) مشاهده می شود.
نتیجه و معنا. این روند زمانی برگشت پذیر است که علت از بین برود و مهمتر از همه، با درمان مناسب، ترکیب خون را می توان بازسازی کرد - نتیجه مطلوب است. در موارد دیگر غلیظ شدن خون با اختلالات متابولیک، افزایش اصطکاک خون در برابر دیواره رگ ها، افزایش ویسکوزیته همراه است و این امر مانع از کار قلب می شود و می تواند منجر به ایجاد نارسایی حاد قلبی شود. ضخیم شدن خون به ایجاد ترومبوز کمک می کند.
رقیق شدگی خون
رقیق شدن خون یا هیدرمی، افزایش میزان آب در خون محیطی فرد است. به ندرت در موارد زیر مشاهده می شود: بیماری کلیوی، هنگامی که فشار اسمزی، انکوتیک، تعادل پروتئین مختل می شود - مایع در خون حفظ می شود.
با همگرایی سریع ادم - هیپرولمی؛
هنگام بازپرداخت BCC با پلاسما و جایگزین های خون پس از از دست دادن خون.
در برخی موارد احیا و مراقبت های ویژه، اگر پزشکان به منظور سم زدایی و/یا بازیابی پارامترهای همودینامیک، مقدار زیادی مایع را به صورت داخل وریدی تزریق کنند. هیپرهیدراتاسیون (آب زیاد) و هیپرولمی، یعنی افزایش BCC وجود دارد. یکی از مظاهر آن رقیق شدن خون است.
مقدار رقیق شدن خون منفی است. می تواند با افزایش حجم خون در گردش همراه باشد که کار قلب را دشوار می کند و نارسایی قلبی ایجاد می شود. گاهی اوقات مایع تزریق شده در خون باقی نمی ماند و سپس ادم ریوی و مغزی ایجاد می شود که می تواند عامل مرگ باشد.
شوک یک وضعیت بالینی است که با کاهش اثربخشی همراه است برون ده قلبی، نقض خودتنظیمی سیستم میکروسیرکولاتوری و با کاهش عمومی در خون رسانی به بافت ها مشخص می شود که منجر به تغییرات مخرب در اندام های داخلی می شود.
بر اساس ویژگی های علت و پاتوژنز، انواع شوک زیر متمایز می شود: هیپوولمیک، نوروژنیک، سپتیک، قلب و آنافیلاکتیک.
شوک هیپوولمیک این نوع شوک بر اساس موارد زیر است: کاهش حجم خون در نتیجه خونریزی (چه خارجی و چه داخلی).
از دست دادن بیش از حد مایعات (کم آبی)، مانند اسهال، استفراغ، سوختگی، تعریق زیاد
اتساع عروق محیطی اتساع عمومی عروق کوچک منجر به رسوب بیش از حد خون در عروق محیطی می شود. در نتیجه، کاهش حجم موثر خون وجود دارد که با کاهش برون ده قلبی (نارسایی گردش خون محیطی) همراه است. اتساع عروق محیطی می تواند تحت تأثیر عوامل متابولیک، سمی یا هومورال رخ دهد.
شوک عصبی غش معمولی ناشی از اشکال شوک عصبی؛ این وضعیت خود به خود از بین می رود، زیرا زمانی که فرد در حالت خوابیده روی زمین می افتد، بازگشت وریدی به قلب افزایش می یابد و در نتیجه برون ده قلبی بازیابی می شود. شوک تروماتیک را می توان نوعی از این نوع شوک دانست که لحظه آغازین آن تکانه های آوران بیش از حد (عمدتاً دردناک) است. در برخی موارد، می توان با بیهوشی ناکافی یا آسیب به نخاع و اعصاب محیطی مشاهده کرد.
شوک سپتیک. در شوک سپتیک، اندوتوکسین باکتریایی در گردش (لیپوپلی ساکارید) به گیرنده های CD14 ماکروفاژها متصل می شود که منجر به آزادسازی گسترده سیتوکین ها، به ویژه TNF (فاکتور نکروز تومور) می شود که تظاهرات اصلی آن تغییر در نفوذپذیری عروق و انعقاد خون داخل عروقی است. در شوک سپتیک، سندرم DIC بیشتر مشخص است، زیرا اندوتوکسین های باکتریایی تأثیر مستقیمی بر سیستم انعقاد خون دارند. در نتیجه شوک سپتیک با موارد زیر مشخص می شود: نکروز غده هیپوفیز قدامی، نکروز و خونریزی در غدد فوق کلیوی (سندرم فریدریکسن-واترهاوس)، نکروز قشر کلیه ها.
شوک آنافیلاکتیک در قلب توسعه است شوک آنافیلاکتیکبه دلیل تثبیت IgE روی بازوفیل های خون و بازوفیل های بافت، حساسیت از نوع reaginic (1) وجود دارد. هنگامی که آنتی ژن مجددا وارد می شود، یک واکنش آنتی ژن / آنتی بادی در سطح این سلول ها ایجاد می شود که منجر به آزاد شدن گسترده مواد فعال بیولوژیکی در بافت ها می شود (مواد فعال بیولوژیکی - هیستامین، برادی کینین و لکوترین ها) که در طی دگرانولاسیون آزاد می شوند. بازوفیل های بافتی و بازوفیل های خون و باعث انبساط پری مویرگ ها و "زهکشی" خون به داخل سیستم میکروسیرکولاتوری می شود. کاهش فشار خون منجر به گنجاندن مکانیسم های جبرانی - کاتکول آمین ها می شود که برای تقویت فعالیت انقباضی قلب (افزایش حجم دقیقه) و ایجاد اسپاسم شریان ها طراحی شده اند و در نتیجه از ترمیم فشار خون اطمینان حاصل می کنند. با این حال، در شوک آنافیلاکتیک، "طوفان کاتکول آمین" معمولاً بی اثر است زیرا انتشار قبلی هیستامین باعث انسداد می شود؟ و - گیرنده ها. انتشار گسترده هیستامین همچنین باعث ایجاد اسپاسم عضلات صاف برونش ها (برونکواسپاسم) و روده ها می شود تا تصویری از انسداد حاد روده ایجاد شود.
شوک قلبیشوک قلبی با کاهش شدید برون ده قلبی در نتیجه آسیب اولیه قلب و کاهش شدید انقباض بطنی رخ می دهد، به عنوان مثال، در انفارکتوس حاد میوکارد، میوکاردیت حاد، انواع خاصی از آریتمی ها، سوراخ شدن حاد دریچه، تجمع سریع مایع در اگزوداتیو. پریکاردیت یکی از انواع شوک قلبییک شوک انسدادی است که در آن جریان خون به قلب یا عروق بزرگ ریوی مسدود می شود. این امر با آمبولی بزرگ ریه یا ترومبوز بزرگ دهلیز چپ که دهانه دریچه میترال را می بندد مشاهده می شود. نقض شدید پر شدن بطن، که هنگام فشرده شدن قلب (تامپوناد) با خروج خون (با پارگی قلب) یا مایع التهابی (افیوژن پریکارد) مشاهده می شود.
برنج. 1. علل و مکانیسم های ایجاد شوک
نکته 1: در شوک ناشی از کاهش اولیه برون ده قلبی، فشار در ورید ژوگولار افزایش می یابد. در شوک که به دلیل کاهش بازگشت وریدی ایجاد می شود، فشار در ورید ژوگولار کاهش می یابد.
نکته 2: کاهش جریان خون منجر به کاهش بیشتر جریان خون می شود. یک دایره باطل رخ می دهد (به عنوان مثال، لجن گلبول های قرمز، ایسکمی میوکارد، شوک ریه، ایسکمی روده). این منجر به شوک برگشت ناپذیر می شود.
نکته 3: هیپوکسی عمومی بافت منجر به اسیدوز پیشرونده می شود.
تغییرات بالینی و مورفولوژیکی در شوک
هر نوع شوک بر اساس یک مکانیسم تک فازی پیچیده تکوین است. برای دوره اولیه شوک، به دلیل ویژگی های علت و پاتوژنز، علائم نسبتاً خاصی مشخص است. در اواخر دوره شوک، ویژگی نسبی علائم ناشی از ویژگی های علت و پاتوژنز آن ناپدید می شود، تظاهرات بالینی و مورفولوژیکی آن تبدیل به کلیشه می شود.
سه مرحله ایجاد شوک وجود دارد:
مرحله جبران: در پاسخ به کاهش برون ده قلب، سیستم عصبی سمپاتیک فعال می شود که منجر به افزایش ضربان قلب (تاکی کاردی) و انقباض عروق محیطی و در نتیجه حفظ فشار خون در اندام های حیاتی (مغز و میوکارد) می شود. . اولین شواهد بالینی یک نبض شوک (رشته ای) با دامنه کم است. انقباض عروق محیطی در بافت هایی که کمتر حیاتی هستند بارزتر است. پوست سرد می شود و عرق لطیف ظاهر می شود که یکی دیگر از تظاهرات بالینی اولیه شوک است. انقباض عروق در شریان های کلیوی باعث کاهش فشار و سرعت فیلتراسیون گلومرولی می شود که منجر به کاهش تولید ادرار می شود. الیگوری (مقدار کمی ادرار) یک مکانیسم جبرانی است که هدف آن حفظ مایعات در بدن است. اصطلاح اورمی پره کلیوی برای اشاره به حالت اولیگوری استفاده می شود که در اثر همه نوع علل خارج کلیوی ایجاد می شود. آسیب کلیه در این مرحله رخ نمی دهد و با افزایش برون ده قلبی، وضعیت به سرعت بهبود می یابد.
مرحله نقض جریان خون در بافت ها: انقباض عروق بیش از حد طولانی مدت منجر به اختلال در فرآیندهای متابولیک در بافت ها و کاهش اکسیژن رسانی آنها می شود که مستلزم انتقال به گلیکولیز بی هوازی با تجمع اسید لاکتیک در بافت ها و ایجاد اسیدوز است. و همچنین پدیده لجن (افزایش تجمع گلبول های خون). در این حالت مانعی برای جریان خون در مویرگ ها ایجاد می شود. در اختلالات شدید جریان خون در بافت ها، نکروز سلولی رخ می دهد که اغلب در اپیتلیوم لوله های کلیوی مشاهده می شود.
مرحله جبران: با پیشرفت شوک، جبران خسارت رخ می دهد. انقباض عروق محیطی رفلکس با اتساع عروق جایگزین می شود، احتمالاً در نتیجه افزایش هیپوکسی مویرگی و اسیدوز. اتساع عمومی عروق و استاز (قطع جریان خون) رخ می دهد که منجر به کاهش تدریجی فشار خون (هیپوتانسیون) می شود تا زمانی که خون رسانی به مغز و میوکارد به سطح بحرانی برسد. هیپوکسی مغز منجر به اختلال حاد فعالیت آن می شود (از دست دادن هوشیاری، ادم، تغییرات دژنراتیو و مرگ نورون ها). هیپوکسی میوکارد منجر به کاهش بیشتر برون ده قلبی و مرگ سریع می شود.
تغییرات مورفولوژیکی در اندام های داخلی در شوک
در کالبد شکافی، توجه به توزیع مجدد خون با تجمع آشکار آن در عروق ریز عروق جلب می شود. حفره های قلب و عروق بزرگ خالی است، در بقیه خون در حالت مایع است. اتساع ونول ها، ادم کم و بیش منتشر (ادم)، خونریزی های متعدد، میکروسکوپی - چسبندگی گلبول های قرمز در مویرگ ها، میکروترومبی ها (پدیده لجن، انعقاد داخل عروقی منتشر) مشاهده می شود. در میان سایر صدمات، باید به کانون های متعدد نکروز در اندام های داخلی اشاره کرد، جایی که آنها به طور انتخابی در اطراف مویرگ های سینوسی قرار دارند که معمولاً برای خون قابل عبور هستند. برخی از ویژگی های تصویر مورفولوژیکی مشاهده شده در شوک در اندام های داخلی باعث استفاده از اصطلاح "ارگان شوک" شد.
در کلیه شوکاز نظر ماکروسکوپی، لایه قشری در مقایسه با اهرام، که در نتیجه تجمع رنگدانه هموگلوبینوژنیک و توده های تیز ناحیه juxtaglomerular به دلیل شانت خون، دارای رنگ قرمز مایل به قهوه ای هستند، در حجم افزایش یافته است، رنگ پریده، ادماتیک است. از نظر میکروسکوپی، کم خونی قشر، نکروز حاد اپیتلیوم لوله های پیچ خورده با پارگی غشای پایه لوله ها و ادم بینابینی آشکار می شود. در مجرای لولهها، قالبهای پروتئینی، رنگدانههای هموگلوبینوژن، سلولهای اپیتلیال پوسیده پوستهشده قابل مشاهده هستند. این ضایعات ماهیتی سگمنتال و کانونی دارند، یعنی فقط قسمتی از توبول تحت تأثیر قرار می گیرد، به عنوان مثال، قسمت انتهایی و نه همه نفرون ها، بلکه گروه های فردی آنها. ساختار گلومرول کلیه ها، به عنوان یک قاعده، حفظ می شود، مگر در مواردی که نکروز قشر متقارن ایجاد می شود. این نفروپاتی لوله ای حاد با ایجاد نارسایی حاد کلیه همراه است. اما با درمان به موقع و فشرده، یک نتیجه مطلوب به دلیل بازسازی اپیتلیوم تخریب شده امکان پذیر است.
V شوک ریه (سندرم دیسترس تنفسی [RDS])گردش خون ناهموار، پدیده سندرم DIC همراه با لجن گلبول های قرمز و میکروترومب ها، نکروز کوچک متعدد، ادم آلوئولی و بینابینی، خونریزی های کانونی، آلوئولیت سروزی و هموراژیک، تشکیل غشاهای هیالین مانند (فیبرین). با یک فرآیند طولانی، وضوح همیشه از طریق پنومونی کانونی انجام می شود.
V کبد: سلولهای کبدی گلیکوژن را از دست میدهند (سبک، از نظر نوری خالی، رنگ را برای چربی و گلیکوژن درک نمیکنند)، دچار دیستروفی هیدروپیک میشوند، نکروز بدون اکسیژن در ناحیه مرکزی لوبول کبدی (نکروز مرکز لوبولار) رخ میدهد. در بخش ماکروسکوپی، کبد شبیه یک تراشه سنگ مرمر زرد است.
تغییرات میوکارددر شوک، آنها با تغییرات دیستروفیک در کاردیومیوسیت ها با ناپدید شدن گلیکوژن در سیتوپلاسم آنها و ظاهر شدن لیپیدها، انقباضات میوفیبریل ها نشان داده می شوند. ظهور کانون های کوچک نکروز، عمدتاً در زیر اندوکارد، امکان پذیر است.
V معده و رودهزیاد خونریزی های جزئیدر لایه مخاطی در ترکیب با زخم - آنها را "زخم استرس" می نامند. نکروز ایسکمیک روده مهم است زیرا اغلب با ترشح اندوتوکسین های باکتریایی تشدید می شود (به دلیل ورود میکروارگانیسم ها از روده به جریان خون، جایی که آنها از بین می روند. سیستم ایمنی بدنو سیستم مکمل)، که وضعیت را بیشتر بدتر می کند.
علیرغم اصالت، تغییرات مورفولوژیکی توصیف شده در اندام های داخلی به طور مطلق برای شوک خاص نیست.
پیش آگهی شوک به عوامل مختلفی بستگی دارد که مهمترین آنها علت اصلی آن است. وقتی بتوان علت را از بین برد (مثلاً با هیپوولمی، مایع یا خون تزریق میشود)، بیشتر بیماران زنده میمانند، حتی اگر در شرایط جدی باشند. در بیماران در حال نقاهت، سلولهای نکروزه (مثلاً سلولهای توبول کلیوی و سلولهای اپیتلیال آلوئولی) معمولاً بازسازی میشوند و این بافتها عملکرد طبیعی خود را باز میگردانند. در صورتی که علت شوک از بین نرود (مثلاً با انفارکتوس وسیع میوکارد) و شروع دیرهنگام درمان، زمانی که آسیب بافتی برگشت ناپذیر قبلاً رخ داده باشد، ممکن است بمیرند.
سندرم انعقاد خون داخل عروقی منتشر
(سندرم DIC، سندرم ترومبوهموراژیک، انعقاد مصرفی)
سندرم انعقاد داخل عروقی منتشر با تشکیل گسترده لختههای خونی کوچک (فیبرین، اریتروسیتیک، هیالین) در ریز عروق کل بدن، همراه با انعقاد ناپذیری خون، که منجر به خونریزیهای شدید متعدد میشود، مشخص میشود. این یک عارضه جدی و اغلب کشنده از بیماری های متعدد است و نیاز دارد تشخیص زودهنگامو درمان این بر اساس ناهماهنگی عملکرد سیستم های انعقاد خون و ضد انعقاد است که مسئول هموستاز هستند.
در بسیاری از موارد، علت انعقاد داخل عروقی منتشر ناشناخته است. شایع ترین علل انعقاد داخل عروقی منتشر عبارتند از:
بیماری های عفونی:
باکتریمی گرم منفی و گرم مثبت
سپسیس مننگوکوکی
عفونت قارچی منتشر
ریکتزیوز
ویرمی شدید (به عنوان مثال، تب خونریزی دهنده)
مالاریا پلاسمودیوم فالسیپاروم
عفونت های نوزادی یا داخل رحمی
بیماری های زنان و زایمان:
آمبولی مایع آمنیوتیک
مرگ داخل رحمی جنین
جدا شدن جفت
بیماری های کبدی:
نکروز گسترده کبد
سیروز کبدی
تومورهای بدخیم
لوسمی پرومیلوسیتیک حاد
متاستاز سرطان، شایع ترین آدنوکارسینوم
واسکولیت عروق کوچک (به عنوان مثال، با ایجاد حساسیت بیش از حد سیتوتوکسیک و انواع ایمونوکمپلکس (II و III))
ترومای گسترده
تب
گرمازدگی
جراحی بای پس قلبی ریوی
گزش مار
شوک شدید
همولیز داخل عروقی
لخته های خون متعدد در عروق کوچک در سندرم DIC منجر به اختلال در پرفیوژن بافتی با تجمع اسید لاکتیک در آنها و ایجاد ایسکمی آنها و همچنین ایجاد ریزانفارکتوس در تعداد زیادی از اندام ها می شود. لخته های خون به ویژه در رگ های کوچک ریه ها، کلیه ها، کبد، غدد فوق کلیوی، غده هیپوفیز، مغز، دستگاه گوارش، پوست شایع است و همراه با خونریزی های متعدد، دیستروفی و نکروز اندام ها و بافت ها (نکروز قشر کلیه ها، نکروز و خونریزی در ریه ها، مغز و غیره). لازم است بدانید که در برخی موارد در حین کالبد شکافی، به دلیل عملکرد موازی و غالب سیستم فیبرینولیتیک، ممکن است میکروترومبی تشخیص داده نشود (به اصطلاح فیبرینولیز).
لازم به ذکر است که ترومبوز منتشر نیز با ایجاد انعقاد منجر به مصرف فاکتورهای انعقادی خون می شود.
مصرف. در این مورد، ترومبوسیتوپنی مشاهده می شود، که همراه با کاهش فیبرینوژن و سایر عوامل انعقادی، منجر به ایجاد خونریزی پاتولوژیک می شود. این تمایل به خونریزی با فعال شدن بیش از حد سیستم فیبرینولیتیک (فعال شدن فاکتور XII هاگمن، که مسیر انعقاد داخلی خون را تحریک می کند و منجر به تبدیل پلاسمینوژن به پلاسمین می شود) تشدید می شود. محصولات تجزیه فیبرین ناشی از عمل پلاسمین بر روی فیبرین نیز دارند
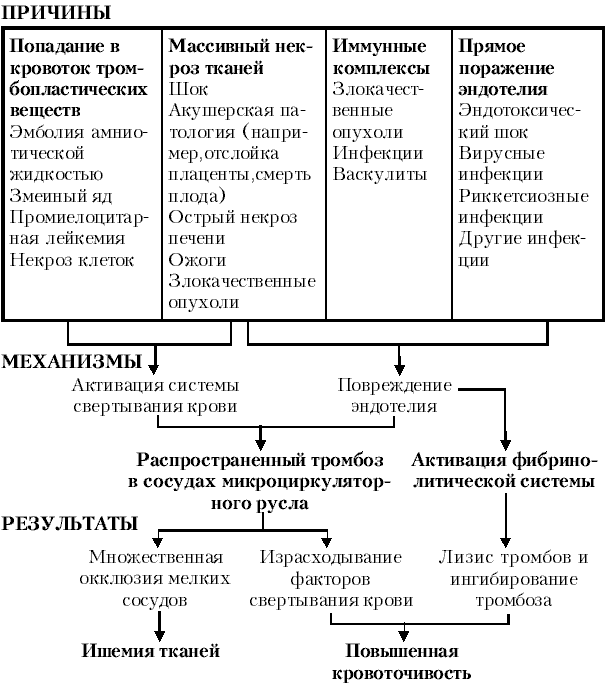
برنج. 2. علل و مکانیسم های ایجاد انعقاد داخل عروقی منتشر
تفاوت اصلی بین انعقاد داخل عروقی منتشر و ترومبوز موضعی این است که در انعقاد داخل عروقی و فیبرینولیز منتشر، هم سیستم انعقادی و هم سیستم فیبرینولیز به طور همزمان فعال می شوند، در حالی که در ترومبوز این تغییرات فقط به صورت موضعی مشاهده می شود. در برخی موارد، با سندرم DIC، ترومبوز غالب است، که منجر به ایسکمی بافتی می شود، در برخی دیگر - فیبرینولیز، که منجر به ظهور خونریزی می شود.
معنی - نارسایی حاد چند عضوی ایجاد می شود که علت مرگ بیماران است.
پیش آگهی با تشخیص به موقع و شروع درمان تعیین می شود که شامل تجویز هپارین برای مهار تشکیل لخته های خون و تجویز پلاکت ها و پلاسما برای بازگرداندن فاکتورهای انعقادی مصرف شده است. نظارت بر سطوح محصولات تجزیه فیبرین، فیبرینوژن و شمارش پلاکت ها برای تشخیص و نظارت بر اثربخشی درمان استفاده می شود.
آثاری وجود دارد که نشان دهنده کارایی بالای درمان سندرم DIC با تزریق خون فیبرینولیز (جسد) خون است.
اختلالات گردش خون موضعی
طبقه بندی
اختلالات گردش خون موضعی عبارتند از:
مجموعه شریانی؛
احتقان وریدی؛
استاز خون؛
خونریزی و خونریزی؛
ایسکمی (کم خونی موضعی)؛
خون کامل شریانی محلی
(هیپرمی آرتریوزا موضعی)
توده شریانی موضعی (پرخونی شریانی) افزایش جریان خون شریانی به اندام یا بافت است.
پرخونی فیزیولوژیکی و پاتولوژیک را تشخیص دهید.
نمونه ای از پرخونی فیزیولوژیکی شریانی می تواند رنگ شرم بر روی صورت، نواحی صورتی مایل به قرمز پوست در محل تحریک حرارتی یا مکانیکی آن باشد.
بر اساس علت و مکانیسم توسعه، انواع زیر از هیپرمی شریانی پاتولوژیک متمایز می شود:
پرخونی آنژیونورتیک در اختلالات وازوموتور ناشی از تحریک اعصاب گشادکننده عروق یا فلج اعصاب منقبض کننده عروق، تحریک عقده های سمپاتیک مشاهده می شود. نمونه ای از این اختلالات، لوپوس اریتماتوز حاد است که در بسیاری از عفونت های حاد، نواحی پرخونی به صورت پروانه ای دراز کشیده به صورت متقارن یا اریتم صورت و ملتحمه چشم ظاهر می شود. پرخونی آنژیونورتیک شامل پرخونی اندام ها با آسیب شبکه عصبی مربوطه، پرخونی نیمی از صورت همراه با نورالژی همراه با تحریک عصب سه قلو و غیره است.
پرخونی آنژیونورتیک با تسریع جریان خون نه تنها در عملکرد طبیعی، بلکه در باز کردن مویرگ های ذخیره مشخص می شود. پوست و غشاهای مخاطی قرمز، کمی متورم، گرم یا داغ در لمس می شوند. معمولا این پرخونی به سرعت از بین می رود و اثری از خود باقی نمی گذارد.
پرخونی جانبی زمانی رخ می دهد که شریان اصلی، به عنوان مثال، توسط پلاک آترواسکلروتیک بسته شود. خون جاری در امتداد وثیقه ها هجوم می آورد که در همان زمان گسترش می یابد. از اهمیت زیادی در ایجاد پرخونی شریانی جانبی، همه چیزهای دیگر برابر هستند، میزان بسته شدن رگ بزرگ و سطح فشار شریانی است. تنگی و حتی بسته شدن عروق بزرگ، زمانی که در طول سال ها ایجاد می شوند، ممکن است با عواقب شدید همراه نباشد. این به دلیل این واقعیت است که وثیقه ها در سیستم شریانی به موازات افزایش مانع جریان خون در امتداد تنه اصلی ایجاد می شوند.
گاهی اوقات، به عنوان مثال، در آترواسکلروز، بسته شدن هر دو شریان کرونری قلب با علائم واضح نارسایی قلبی همراه نیست، زیرا گردش خون جانبی در اینجا به دلیل شریان های مدیاستن، بین دنده ای، پریکارد و برونش ایجاد می شود.
آگاهی از قابلیت های آناتومیکی گردش خون جانبی به جراحان اجازه می دهد تا با موفقیت عملیات بستن شریان های فمورال، پوپلیتئال و کاروتید را بدون ایجاد عوارض شدید به شکل نکروز اندام های مربوطه انجام دهند.
پرخونی پس از کم خونی (هیپرمی پس از کم خونی) زمانی ایجاد می شود که یک عامل (به عنوان مثال، تورم، تجمع مایع در حفره ها) که باعث کم خونی موضعی (ایسکمی) می شود به سرعت حذف شود. رگهای بافتی که قبلاً تخلیه شدهاند به شدت منبسط میشوند و از خون سرریز میشوند. خطر چنین پرخونی شریانی در این واقعیت نهفته است که رگ های بیش از حد پر شده، به ویژه در افراد مسن، می تواند پاره شود و منجر به خونریزی و خونریزی شود. علاوه بر این، در ارتباط با توزیع مجدد شدید خون، کم خونی سایر اندام ها، به عنوان مثال، مغز، قابل مشاهده است که در کلینیک با توسعه غش همراه است. بنابراین، دستکاری هایی مانند برداشتن مایع از قفسه سینه و حفره های شکمی به آرامی انجام می شود.
هیپرمی خلاء (از لاتین vacuus - خالی) به دلیل کاهش فشار هوا ایجاد می شود. نمونه ای از این موارد پرخونی پوست تحت تأثیر فنجان های طبی است.
پرخونی التهابی یکی از علائم بالینی مهم هر التهاب است.
پرخونی بر اساس شانت شریانی وریدی زمانی رخ می دهد که در هنگام ضربه، آناستوموز بین شریان و ورید ایجاد شود و خون شریانی به داخل ورید می رود. خطر این پرخونی با احتمال پارگی چنین آناستوموز و ایجاد خونریزی تعیین می شود.
ارزش هیپرمی شریانی پاتولوژیک عمدتاً بر اساس نوع آن تعیین می شود.
خون وریدی موضعی
(hyperaemia venosa localis)
احتقان وریدی موضعی (پرخونی وریدی) زمانی ایجاد می شود که خروج خون وریدی از یک عضو یا بخشی از بدن مختل شود. بر اساس علت و مکانیسم توسعه، آنها تشخیص می دهند: پرخونی انسدادی وریدی ناشی از انسداد مجرای ورید توسط ترومبوز، آمبولی (ترومبوفلبیت محو کننده وریدهای کبدی - بیماری هیاری، که در آن، مانند احتقان وریدی عمومی، کبد جوز هندی ایجاد می شود، و در دوره مزمن - سیروز کبدی مسقطی؛ سفتی سیانوتیک کلیه ها با ترومبوز ورید کلیوی).
پرخونی وریدی فشاری، مشاهده شده زمانی که ورید از خارج توسط ادم التهابی، تومور، لیگاتور، بافت همبند در حال رشد فشرده می شود.
پرخونی وریدی جانبی، که می توان آن را هنگامی مشاهده کرد که یک تنه بزرگ ورید اصلی بسته شود، به عنوان مثال، پورتوکاوال آناستوموز با مشکل در خروج خون از طریق ورید پورتال (ترومبوز ورید پورتال، سیروز کبدی).
بازآرایی مورفولوژیکی وثیقه های وریدی از همان اصل شریانی پیروی می کند، با این تفاوت ماکروسکوپی، با این حال، این است که عروق وریدی در حال گسترش به شکل مارپیچ و ندولر هستند.
چنین تغییراتی را واریس می نامند و در آن مشاهده می شود اندام های تحتانی، در طناب اسپرماتیک (واریکوسل)، در رباط های پهن رحم، در مجرای ادرار، در مقعد و قسمت مجاور رکتوم - به اصطلاح هموروئید. در دیواره قدامی شکم، رگ های سرریز از خون وریدی ظاهری دارند که در ادبیات به آن "سر چتر دریایی" می گویند. وریدهای جانبی پر از خون به شدت منبسط می شوند و دیواره آنها نازک تر می شود. این می تواند علت خونریزی خطرناک باشد (به عنوان مثال، خونریزی شدید از بواسیر بیرون زده به مجرای راست روده، خونریزی از وریدهای متسع و نازک مری همراه با سیروز کبدی). با وریدهای واریسی اندام تحتانی (عمدتا v. Saphena magna et parva و موارد جانبی آنها، و همچنین رگهای پوستی کوچک)، سیانوز، ادم، فرآیندهای آتروفیک برجسته مشاهده می شود: پوست و بافت زیر جلدی، به ویژه یک سوم پایین ساق پا. ، بسیار لاغر می شوند و زخم های ساق پا به سختی بهبود می یابند ("زخم ساق پا").
خروج احتقان وریدی موضعی یک فرآیند برگشت پذیر است اگر علت آن به سرعت برطرف شود.
اهمیت اختلالات خروج وریدی با وجود این واقعیت که اختلالات خروج وریدی بسیار شایع تر از انسداد شریانی است، اهمیت بالینی آنها تا حدودی کمتر است. این عمدتا به دلیل تعداد بیشتر عروق جانبی در سیستم وریدی نسبت به سیستم شریانی است.
اختلالات خروج وریدی هنگامی که یک سیاهرگ بسیار بزرگ آسیب دیده است (به عنوان مثال ورید اجوف فوقانی) یا اگر گردش خون جانبی کافی در این ناحیه وجود نداشته باشد (مثلاً با انسداد ورید مرکزی شبکیه، ساژیتال فوقانی) باعث تغییرات قابل توجهی در بافت ها می شود. سینوس، سینوس کاورنو، ورید کلیوی). هنگامی که زهکشی وریدی جانبی وجود داشته باشد، اما ضعیف باشد، مانند ورید فمورال، بسته شدن لومن آن می تواند باعث ادم متوسط به دلیل افزایش فشار هیدرواستاتیک در انتهای وریدی مویرگ شود. در پلتورای شدید وریدی، فشار هیدرواستاتیک ممکن است به حدی افزایش یابد که باعث پارگی مویرگ ها و خونریزی شود، مانند پلتورای وریدی و خونریزی در بافت های چشم در صورت انسداد سینوس غار. در موارد شدید، انسداد وریدها می تواند منجر به انفارکتوس وریدی شود. بنابراین، ارزش توده وریدی منفی است، زیرا خونریزی های دیاپدی در اندام ها ایجاد می شود، و اغلب خونریزی، تغییرات دیستروفیک، آتروفیک و اسکلروتیک، گاهی اوقات با نکروز بافتی همراه است.
استاز (از لاتین stasis - ایستادن) کاهش سرعت، تا توقف کامل، جریان خون در عروق میکروواسکولار، عمدتا در مویرگ ها است.
استاز خون ممکن است با احتقان وریدی (استاز احتقانی) یا ایسکمی (استاز ایسکمیک) پیش از آن باشد. با این حال، می تواند بدون اختلالات گردش خون ذکر شده قبلی، تحت تأثیر علل درونی و برون زا، در نتیجه عمل عفونت ها (به عنوان مثال، مالاریا، تیفوس)، عوامل شیمیایی و فیزیکی مختلف بر روی بافت (درجه حرارت بالا) رخ دهد. ، سرماخوردگی) منجر به اختلال در عصب عروقی، با بیماری های عفونی-آلرژیک و خودایمنی (بیماری های روماتیسمی) و غیره می شود.
استاز خون با توقف خون در مویرگ ها و ونول ها با انبساط لومن و چسبندگی گلبول های قرمز به ستون های همگن مشخص می شود - این امر استاز را از پرخونی وریدی متمایز می کند. همولیز و لخته شدن خون رخ نمی دهد.
استاز را باید از پدیده لجن متمایز کرد. لجن پدیده ای از چسبندگی گلبول های قرمز نه تنها در مویرگ ها، بلکه در عروق با اندازه های مختلف از جمله سیاهرگ ها و شریان ها است. این سندرم تجمع داخل عروقی گلبول های قرمز نیز نامیده می شود و با انواع عفونت ها، مسمومیت های ناشی از افزایش چسبندگی گلبول های قرمز، تغییر در شارژ آنها مشاهده می شود. در کلینیک، پدیده لجن با افزایش ESR منعکس می شود.
به عنوان یک فرآیند موضعی (منطقه ای)، لجن در وریدهای ریوی ایجاد می شود، به عنوان مثال، با اصطلاح شوک ریه، یا نارسایی حاد تنفسی در بزرگسالان (سندرم زجر تنفسی).
با منشأهای مختلف هیپوکسی، اسپاسم وریدها، به اصطلاح "بحران وریدی" به گفته ریکر، قابل مشاهده است. این می تواند باعث لکوستاز شود - تجمع گرانولوسیت ها در داخل بستر عروقی: در وریدها، مویرگ ها. لکوستاز در شوک غیرمعمول نیست و با لوکودیاپدزیس همراه است.
خروج استاز یک پدیده برگشت پذیر است. استاز با تغییرات دژنراتیو در اندام هایی که در آن مشاهده می شود همراه است. استاز برگشت ناپذیر منجر به نکروز می شود.
اهمیت بالینی استاز با فراوانی این پدیده تعیین می شود. استاز و شرایط پرستاتیک در بحرانهای آنژینوروتیک (فشار خون بالا، آترواسکلروز)، در اشکال حاد التهاب، در شوک، در بیماریهای ویروسی مانند آنفولانزا، سرخک مشاهده میشود. قشر مغز حساس ترین به اختلالات گردش خون و هیپوکسی است. استاز می تواند منجر به ایجاد انفارکتوس های کوچک شود. ایستایی گسترده در کانون های التهاب، خطر نکروز بافتی را به همراه دارد که می تواند مسیر را به طور اساسی تغییر دهد. فرآیند التهابی... به عنوان مثال، با ذات الریه، این می تواند منجر به خفگی و ایجاد قانقاریا، یعنی نکروز شود.
از نقطه نظر بیولوژیکی کلی، استاز جبران سازوکارهای تطبیقی زیربنایی تنظیم گردش خون محیطی و گردش خون در اندام ها است.
خون ریزی
خونریزی (هموراژی) - آزاد شدن خون از مجرای یک رگ یا حفره قلب. اگر خون به محیط ریخته شود، در مورد خونریزی خارجی صحبت می کنند، اگر در حفره بدن بدن - در مورد خونریزی داخلی صحبت می کنند.
نمونه هایی از خونریزی خارجی عبارتند از هموپتیز (هموپتوئه)، خونریزی بینی (اپیستاکسی)، استفراغ خون (هماتومز)، خون در مدفوع (ملنا)، خونریزی از رحم (متروراژی). در خونریزی داخلی، خون می تواند در حفره پریکارد (هموپریکاردیوم)، پلور (هموتوراکس)، حفره شکمی (هموپریتونئوم) تجمع یابد.
خروج خون به خارج از بستر عروقی با تجمع آن در بافت به عنوان خونریزی نامیده می شود. خونریزی از نوع خصوصی است
خون ریزی.
علل خونریزی (خونریزی) می تواند پارگی، خوردگی و افزایش نفوذپذیری دیواره عروق باشد.
خونریزی در نتیجه پارگی دیواره رگ یا قلب - خونریزی از طریق رکسین - همراه با نکروز، التهاب یا اسکلروز دیواره عروق یا قلب رخ می دهد. این نوع خونریزی، به عنوان مثال، با پارگی قلب به دلیل میومالاسی در انفارکتوس میوکارد (بیماری ایسکمیک حاد قلب)، پارگی آئورت همراه با نکروز غشای میانی آن (مدیونکروز)، با التهاب پوشش میانی آن رخ می دهد. آئورت (مزائورتیت) با سیفلیس. اغلب پارگی آنوریسم قلب، آئورت و شریان های مغزی، شریان های ریوی با واسکولیت با علل مختلف، فشار خون بالا، آترواسکلروز و غیره وجود دارد.
خونریزی در نتیجه فرسایش دیواره عروق - خونریزی از طریق دیابروزین - یا خونریزی خورنده، زمانی رخ می دهد که دیواره عروق توسط شیره معده در انتهای زخم خورده شود، نکروز کازئوز در دیواره حفره همراه با سل، سرطان، ترشح چرکی همراه با آبسه، بلغم. خونریزی خورنده نیز در طول حاملگی خارج رحمی (لوله ای) ایجاد می شود، زمانی که پرزهای کوریونی رشد می کنند و دیواره لوله کوفالوپی و عروق آن را خورده می کنند.
خونریزی به دلیل افزایش نفوذپذیری دیواره عروق (بدون نقض قابل مشاهده یکپارچگی آن) - خونریزی در هر دیاپدزین - به دلایل بسیاری از شریان ها، مویرگ ها و وریدها ناشی می شود. خونریزی های دیاپدی در واسکولیت های سیستمیک، بیماری های عفونی و عفونی- آلرژیک، در بیماری های سیستم خونی (هموبلاستوز و کم خونی)، انعقاد، کمبود ویتامین، در برخی مسمومیت ها، مصرف بیش از حد داروهای ضد انعقاد و غیره رخ می دهد.
خونریزی های ماکروسکوپی متمایز می شوند:
نقطه - پتشی و اکیموز؛
کبودی - خونریزی مسطح در پوست و غشاهای مخاطی؛
هماتوم - تجمع خون در بافت با نقض یکپارچگی آن و تشکیل حفره.
انفیلتراسیون هموراژیک - اشباع خون بافت بدون برهم زدن یکپارچگی آن.
خروج جذب کامل خون مطلوب ترین نتیجه خونریزی و خونریزی است. سازمان - جایگزینی خون خروجی با بافت همبند. کپسولاسیون رشد بافت همبند در اطراف خون خروجی با تشکیل یک کپسول است. سنگسازی رسوب نمکهای Ca2 + در خون است. الحاق عفونت و چروک یک نتیجه نامطلوب است.
معنای خونریزی و خونریزی با نوع آن مشخص می شود، یعنی خون از کجا می آید: از شریان، ورید، مویرگ ها. محلی سازی، یعنی جایی که خون ریخته می شود، میزان خون از دست رفته، میزان از دست دادن خون، وضعیت بدن. پارگی آئورت، آنوریسم آن منجر به از دست دادن سریع مقدار زیادی خون و در اکثریت قریب به اتفاق موارد به مرگ ناشی از کم خونی حاد عمومی می شود. خونریزی طولانی مدت و مکرر (به عنوان مثال، با زخم معده و زخم اثنی عشر، هموروئید) می تواند منجر به کم خونی مزمن شود. به خصوص خطرناک، اغلب کشنده، خونریزی مغزی است، به عنوان مثال، با پارگی آنوریسم شریان مغز، سکته هموراژیک در فشار خون بالا. اغلب کشنده خونریزی در ریه ها همراه با ساییدگی رگ در دیواره حفره سل یا در یک تومور متلاشی می شود. در عین حال، خونریزی های شدید در بافت چربی زیر جلدی و ماهیچه ها ممکن است هیچ خطری برای زندگی نداشته باشند.
ترومبوز (از یونانی ترومبوز) - در داخل بدن انعقاد خون در مجرای رگ، در حفره های قلب، یا از دست دادن توده های متراکم از خون.
لخته خون حاصل ترومبوز نامیده می شود.
انعقاد خون پس از مرگ در عروق خونی مشاهده می شود (لخته شدن خون پس از مرگ). و توده های متراکم خونی که در همان زمان ریخته شده اند، لخته خون پس از مرگ نامیده می شوند.
علاوه بر این، لخته شدن خون در بافت ها در هنگام خونریزی از یک رگ آسیب دیده رخ می دهد و یک مکانیسم هموستاتیک طبیعی است که هدف آن متوقف کردن خونریزی زمانی است که یک رگ آسیب دیده است.
بر اساس مفهوم مدرن، فرآیند انعقاد خون به شکل یک واکنش آبشاری ("نظریه آبشار") - فعال شدن متوالی پروتئین های پیش ساز، یا عوامل انعقادی در خون یا بافت ها اتفاق می افتد (این نظریه به تفصیل در توضیح داده شده است. سخنرانی گروه فیزیولوژی پاتولوژیک).
علاوه بر سیستم انعقادی، یک سیستم ضد انعقاد نیز وجود دارد که تنظیم سیستم هموستاز - حالت مایع خون در بستر عروقی را در شرایط عادی تضمین می کند. بر این اساس، ترومبوز تظاهر اختلال در تنظیم سیستم هموستاتیک است.
ترومبوز با انعقاد خون متفاوت است، اما این تفاوت تا حدودی خودسرانه است، زیرا در هر دو مورد یک واکنش انعقاد خون آبشاری ایجاد می شود. یک ترومبوز همیشه به اندوتلیوم متصل است و از لایههایی از پلاکتها، رشتههای فیبرین و سلولهای خونی به هم پیوسته تشکیل شده است و لخته خون حاوی رشتههای فیبرین با جهتگیری تصادفی است که پلاکتها و گلبولهای قرمز بین آنها قرار دارند.
هموستاز طبیعی
در حالت طبیعی، تعادل ظریف و پویا بین تشکیل لخته خون و انحلال آن (فیبرینولیز) وجود دارد.
هنگامی که یک رگ آسیب می بیند (شایع ترین عامل منجر به تشکیل ترومبوز)، آسیب به اندوتلیوم رخ می دهد که با تشکیل پلاک هموستاتیک پلاکتی و فعال شدن سیستم های انعقادی و فیبرینولیز همراه است (شکل 3).
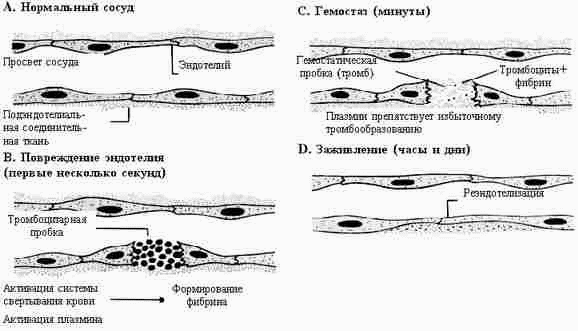
برنج. 3. مکانیسم هموستاز طبیعی
پاسخ: در یک رگ سالم و سالم، بافت همبند ساب اندوتلیال، به ویژه کلاژن و الاستین، از جریان خون جدا می شود.
س: در چند ثانیه اول پس از آسیب، پلاکت ها به بافت ساب اندوتلیال می چسبند و جمع می شوند. آسیب اندوتلیال همچنین منجر به فعال شدن فاکتور Hageman (عامل XII) می شود که منجر به فعال شدن مسیر انعقاد داخلی خون می شود. آزاد شدن ترومبوپلاستین های بافتی مسیر خارجی را نیز فعال می کند.
ج: هموستاز در عرض چند دقیقه رخ می دهد. فیبرین و پلاکت ها یک پلاگ هموستاتیک (ترومبوز) تشکیل می دهند. پلاسمین (فیبرینولیزین) از لخته شدن خون اضافی جلوگیری می کند.
د: جمع شدن لخته، سازماندهی و فیبروز در طول بهبودی رخ می دهد.
آخرین مرحله، اندوتلیالیزاسیون مجدد است.
تشکیل پلاک هموستاتیک پلاکت: آسیب به اندوتلیوم عروقی باعث قرار گرفتن در معرض کلاژن ساب اندوتلیال می شود که اثر ترومبوژنیک قوی بر پلاکت ها دارد و منجر به چسبندگی پلاکت ها در محل آسیب می شود. پلاکت ها محکم به اندوتلیوم آسیب دیده و به یکدیگر متصل می شوند و یک پلاگ هموستاتیک را تشکیل می دهند که آغاز روند تشکیل ترومبوز است. تجمع پلاکت ها به نوبه خود منجر به دگرانولاسیون آنها می شود، در حالی که سروتونین، ADP، ATP و مواد ترومبوپلاستیک آزاد می شوند. ADP که یک عامل تجمع پلاکتی قوی است، باعث تجمع بیشتر پلاکت ها می شود. در ترومبوز، لایههای پلاکتها با فیبرین متناوب میشوند و با بررسی میکروسکوپی به صورت خطوط رنگ پریده آشکار میشوند (خطوط Zahn)
انعقاد خون: فعال شدن فاکتور Hageman (فاکتور XII در آبشار انعقاد خون) با فعال کردن آبشار انعقادی داخلی منجر به تشکیل فیبرین می شود. ترومبوپلاستین های بافتی که در اثر آسیب آزاد می شوند، آبشار انعقاد خون خارجی را فعال می کنند که منجر به تشکیل فیبرین می شود. فاکتور سیزدهم بر روی فیبرین اثر می گذارد و باعث ایجاد یک پلیمر فیبریلار نامحلول می شود که همراه با پلاگ پلاکت، هموستاز نهایی را فراهم می کند. در معاینه میکروسکوپی، فیبرین دارای ساختار شبکه ای فیبریلار است که رنگ آمیزی شده است رنگ صورتی، با توده های رنگ پریده آمورف متناوب پلاکت ها.
اختلالات هموستاز
تعادل طبیعی که بین تشکیل لخته و فیبرینولیز وجود دارد، تشکیل لخته ای با اندازه مطلوب را تضمین می کند که برای توقف خونریزی از رگ کافی است. فعالیت فیبرینولیتیک از تشکیل بیش از حد ترومبوز جلوگیری می کند. نقض این تعادل در برخی موارد منجر به تشکیل بیش از حد ترومبوز می شود، در برخی دیگر - به خونریزی.
تشکیل بیش از حد ترومبوز منجر به باریک شدن مجرای رگ یا انسداد آن (بسته شدن کامل) می شود. این معمولاً در نتیجه قرار گرفتن در معرض عوامل محلی رخ می دهد که فعالیت سیستم فیبرینولیتیک را سرکوب می کند، که معمولاً از تشکیل بیش از حد ترومبوز جلوگیری می کند.
برعکس، کاهش لخته شدن خون منجر به خونریزی بیش از حد می شود و در اختلالات مختلف که مستلزم افزایش خونریزی است مشاهده می شود: با کاهش تعداد پلاکت ها در خون، کمبود فاکتورهای انعقادی و افزایش فعالیت فیبرینولیتیک.
عوامل موثر بر تشکیل ترومبوز:
آسیب به اندوتلیوم عروقی، که هم چسبندگی پلاکت ها و هم فعال شدن آبشار انعقاد خون را تحریک می کند، عامل اصلی تشکیل ترومبوز در بستر شریانی است. هنگامی که یک لخته خون در وریدها و ریز عروق تشکیل می شود، آسیب اندوتلیال نقش کمتری ایفا می کند.
تغییرات در جریان خون، مانند کاهش جریان خون و جریان خون آشفته؛
تغییرات در خواص فیزیکوشیمیایی خون (ضخیم شدن خون، افزایش ویسکوزیته خون، افزایش سطح فیبرینوژن و تعداد پلاکت ها) از عوامل مهم تر در ترومبوز وریدی هستند.
دلایل ترومبوز:
بیماری های سیستم قلبی عروقی
تومورهای بدخیم
عفونت ها
دوره بعد از عمل
مکانیسم های تشکیل ترومبوز:
لخته شدن خون - انعقاد
چسبندگی پلاکت - تجمع
پیوند گلبول های قرمز - آگلوتیناسیون
رسوب پروتئین پلاسما - رسوب
مورفولوژی و انواع لخته های خون. ترومبوز دستهای از خون است که در محل آسیب به دیواره رگ خونی چسبیده است، معمولاً قوام متراکم دارد، خشک است، به راحتی خرد میشود، لایه لایه، با سطحی موجدار یا ناهموار. در کالبد شکافی، باید از انعقاد خون پس از مرگ متمایز شود، که اغلب شکل رگ را تکرار می کند، با دیواره آن مرتبط نیست، مرطوب، الاستیک، همگن، با سطح صاف است.
بسته به ساختار و ظاهر، آنها متمایز می شوند:
لخته خون سفید؛
لخته خون قرمز؛
لخته خون مخلوط؛
ترومبوز هیالین
ترومبوس سفید متشکل از پلاکتها، فیبرین و لکوسیتها با تعداد کمی گلبول قرمز است که به آرامی و بیشتر در بستر شریانی، جایی که سرعت جریان خون بالا مشاهده میشود، تشکیل میشود.
لخته قرمز خون از پلاکت ها، فیبرین و تعداد زیادی گلبول قرمز تشکیل شده است که در شبکه فیبرین به دام افتاده اند. لختههای خون قرمز معمولاً در سیستم وریدی تشکیل میشوند، جایی که جریان آهسته خون جذب گلبولهای قرمز را تشویق میکند.
ترومبوز مخلوط اغلب رخ می دهد، دارای ساختار لایه ای است، حاوی عناصر خونی است که مشخصه ترومبوس سفید و قرمز است. لخته های خونی لایه ای بیشتر در وریدها، در حفره آنوریسم آئورت و قلب ایجاد می شوند. در یک ترومبوز مختلط، موارد زیر وجود دارد: سر (ساختار یک ترومبوز سفید دارد) - این وسیع ترین قسمت آن است.
بدن (در واقع لخته خون مخلوط)؛
دم (دارای ساختار یک لخته خون قرمز).
سر به محلی از اندوتلیوم تخریب شده متصل است که ترومبوز را از لخته شدن خون پس از مرگ متمایز می کند.
ترومبوز هیالین نوع خاصی از لخته خون است. از گلبول های قرمز همولیز شده، پلاکت ها و پروتئین های پلاسما در حال رسوب تشکیل شده است و عملاً عاری از فیبرین است. توده های حاصل شبیه هیالین هستند. این لخته های خون در رگ های ریز عروق یافت می شوند. گاهی اوقات ترومبوس ها یافت می شوند که تقریباً به طور کامل از پلاکت ها تشکیل شده اند. آنها معمولاً در بیمارانی که تحت درمان با هپارین قرار می گیرند ایجاد می شوند (اثر ضد انعقادی آن از تشکیل فیبرین جلوگیری می کند).
در رابطه با لومن رگ، موارد زیر وجود دارد:
ترومب پاریتال (بیشتر لومن آزاد است)؛
انسداد یا انسداد ترومبوز (لومن رگ تقریباً به طور کامل بسته است).
محلی سازی لخته های خون
ترومبوز شریانی: لخته شدن خون در شریان ها بسیار کمتر از وریدها است و معمولاً پس از آسیب به اندوتلیوم و تغییر موضعی در جریان خون (جریان خون آشفته) مانند تصلب شرایین ایجاد می شود.
در بین شریان های با کالیبر بزرگ و متوسط، بیشتر تحت تأثیر قرار می گیرند آئورت، شریان های کاروتید، شریان های دایره ویلیس، عروق کرونر قلب، عروق روده و اندام.
به طور معمول، ترومبوز شریانی یک عارضه آرتریت است، به عنوان مثال، در پری آرتریت ندوزا، آرتریت سلول غول پیکر، ترومبانگیت انسدادی و پورپورای شونلین-هنوخ و سایر بیماری های روماتیسمی.
در بیماری فشار خون، عروق با کالیبر متوسط و بزرگ بیشتر تحت تأثیر قرار می گیرند.
ترومبوز قلب: در شرایط زیر لخته های خون در حفره های قلب تشکیل می شوند:
التهاب دریچه های قلب منجر به آسیب اندوتلیال، جریان خون آشفته موضعی و رسوب پلاکت ها و فیبرین روی دریچه ها می شود.
لخته های خون کوچک را زگیل (روماتیسم) و لخته های بزرگ را پوشش گیاهی می نامند.
پوشش های گیاهی می توانند بسیار بزرگ و شل و در حال فرو ریختن باشند (مثلاً با اندوکاردیت عفونی). قطعات یک ترومبوز اغلب پاره شده و توسط جریان خون به شکل آمبولی حمل می شوند.
آسیب به اندوکارد جداری. آسیب اندوکارد می تواند با انفارکتوس میوکارد و تشکیل آنوریسم بطنی رخ دهد.
لختههای خونی که روی دیوارههای اتاقک تشکیل میشوند اغلب بزرگ هستند و همچنین میتوانند فرو ریخته و آمبولی ایجاد کنند.
جریان خون آشفته و استاز در دهلیزها. لخته های خون اغلب در حفره دهلیزی تشکیل می شوند که جریان خون آشفته یا استاز خون رخ می دهد، مانند تنگی میترال و فیبریلاسیون دهلیزی. لختههای خون میتوانند آنقدر بزرگ (کروبی) باشند که جریان خون را از طریق دهانه دهلیزی مسدود کنند.
ترومبوز وریدی:
ترومبوفلبیت با ترومبوفلبیت، ترومبوز وریدی برای بار دوم رخ می دهد، در نتیجه التهاب حاد وریدها. ترومبوفلبیت یک اتفاق رایج با زخم ها یا زخم های عفونی است. وریدهای سطحی اندام ها بیشتر تحت تأثیر قرار می گیرند. سیاهرگ آسیب دیده تمام علائم التهاب حاد (درد، قرمزی، گرمی، تورم) را دارد. این نوع لخته خون تمایل دارد به طور محکم به دیواره رگ بچسبد. آمبولی به ندرت از آن تشکیل می شود.
گاهی اوقات ترومبوفلبیت در وریدهای سطحی متعدد پاها (ترومبوفلبیت مهاجرتی) در بیماران مبتلا به نئوپلاسم های بدخیم، اغلب در سرطان معده و پانکراس (علامت تروسو) ایجاد می شود، زیرا موسین ها و سایر مواد تشکیل شده توسط سلول های تومور دارای فعالیت ترومبوپلاستین مانند هستند.
فلبوترومبوز یک ترومبوز وریدی است که در غیاب علائم واضح التهاب رخ می دهد. فلبوترومبوز عمدتاً در وریدهای عمقی پاها رخ می دهد (ترومبوز ورید عمقی). به ندرت وریدهای شبکه وریدی لگن تحت تأثیر قرار می گیرند. ترومبوز ورید عمقی یک اتفاق رایج است و از اهمیت پزشکی بالایی برخوردار است، زیرا لختههای خونی بزرگی که در این وریدها ایجاد میشوند، به طور شل به دیواره عروق متصل میشوند و اغلب به راحتی از بین میروند. آنها همراه با جریان خون به قلب و ریه ها مهاجرت می کنند و مجرای شریان های ریوی را می بندند (ترومبوآمبولی تنه ریوی و شاخه های آن).
علل فلبوترومبوز: عوامل ایجاد کننده فلبوترومبوز ورید عمقی به طور کلی برای ترومبوز معمولی هستند، اما آسیب اندوتلیال معمولاً ضعیف بیان می شود و تشخیص آن دشوار است. مهمترین عامل ایجاد کننده فلبوترومبوز کاهش جریان خون است. در شبکه وریدی ساق، جریان خون به طور معمول با انقباض عضلات پا (پمپ عضلانی) حفظ می شود. ایجاد رکود خون و ایجاد ترومبوز با بی حرکتی طولانی مدت در بستر، نارسایی قلبی تسهیل می شود. عامل دوم - افزایش ظرفیت چسبندگی و تجمع پلاکت ها و همچنین تسریع لخته شدن خون به دلیل افزایش سطح برخی از عوامل انعقادی (فیبرینوژن، فاکتورهای VII و VIII) - در دوره پس از عمل و پس از زایمان رخ می دهد. با استفاده از داروهای ضد بارداری خوراکی، به ویژه با دوزهای بالای استروژن، در بیماران سرطانی. گاهی اوقات چندین عامل می توانند با هم کار کنند.
تظاهرات بالینی: ترومبوز ورید عمقی پاها ممکن است خفیف یا بدون علامت باشد. معاینه بیمار تورم متوسط مچ پا و درد در داخل را نشان می دهد عضلات ساق پابا خم شدن کف پا (علامت هومن). در اکثر بیماران آمبولی ریه- اولین تظاهرات بالینی فلبوترومبوز. ترومبوز ورید عمقی را می توان با فلبوگرافی، سونوگرافی، روش های رادیولوژیکی، اندازه گیری مقایسه ای پاها با یک نوار سانتی متر تشخیص داد.
نتیجه ترومبوز
تشکیل لخته های خون پاسخی را از بدن برای از بین بردن لخته و بازگرداندن جریان خون به رگ خونی آسیب دیده آغاز می کند.
مکانیسم های مختلفی برای این کار وجود دارد:
لیز ترومبوس (فیبرینولیز)، که منجر به تخریب کامل ترومبوز می شود، یک نتیجه مطلوب ایده آل است، اما بسیار نادر است. فیبرین که لخته را تشکیل می دهد توسط پلاسمین از بین می رود که با فعال شدن آبشار انعقاد داخلی خون (یعنی سیستم فیبرینولیتیک همزمان با سیستم انعقادی فعال می شود) توسط فاکتور Hageman (فاکتور XII) فعال می شود. ترومبوز). فیبرینولیز از تشکیل فیبرین اضافی و تجزیه لخته های خون کوچک جلوگیری می کند. فیبرینولیز در شکستن لختههای خون بزرگ موجود در شریانها، سیاهرگها یا قلب مؤثر نیست. مواد خاصی مانند استرپتوکیناز و فعالکنندههای پلاسمینوژن بافتی که سیستم فیبرینولیتیک را فعال میکنند، هنگامی که بلافاصله پس از ترومبوز استفاده میشوند، مهارکنندههای مؤثر تشکیل ترومبوز هستند و باعث لیز ترومبوز و بازیابی جریان خون میشوند. آنها با موفقیت در درمان انفارکتوس حاد میوکارد، ترومبوز ورید عمقی و ترومبوز شریان محیطی حاد استفاده می شوند. سازماندهی و کانالیزاسیون مجدد معمولاً در لخته های خونی بزرگ رخ می دهد. لیز آهسته و فاگوسیتوز یک ترومبوز با تکثیر بافت همبند و کلاژن سازی (سازماندهی) همراه است. ترک ها می توانند در ترومبوس ایجاد شوند - کانال های عروقی که با اندوتلیوم پوشانده شده اند (کانالیزاسیون مجدد)، به طوری که جریان خون می تواند تا حدودی بازیابی شود. کانالیزاسیون مجدد آهسته است و طی چند هفته انجام می شود، و اگرچه از تظاهرات حاد ترومبوز جلوگیری نمی کند، اما می تواند در درازمدت پرفیوژن بافتی را کمی بهبود بخشد. سنگ شدن ترومبوس یک نتیجه نسبتا مطلوب است که با رسوب نمک های کلسیم در ترومبوس مشخص می شود. در رگ ها، این روند گاهی اوقات تلفظ می شود و منجر به تشکیل سنگ های سیاهرگی (فلبولیت) می شود. فروپاشی سپتیک یک ترومبوز یک نتیجه نامطلوب است که زمانی رخ می دهد که ترومبوز از خون یا دیواره رگ عفونی شود.
ارزش ترومبوز بر اساس میزان توسعه، محلی سازی، شیوع و پیامد آن تعیین می شود.
در برخی موارد، می توانیم در مورد ارزش مثبت ترومبوز صحبت کنیم، به عنوان مثال، با آنوریسم آئورت، زمانی که سازماندهی ترومبوز منجر به تقویت دیواره عروق نازک شده می شود.
در بیشتر موارد، ترومبوز یک پدیده خطرناک است. در شریان ها، انسداد لخته خون می تواند باعث حمله قلبی یا قانقاریا شود. لختههای خون جداری در شریانها خطر کمتری دارند، بهویژه اگر به آهستگی ایجاد شوند، زیرا در این مدت میتوانند وثیقههایی ایجاد شوند که خون لازم را فراهم میکنند.
لخته شدن خون در وریدها باعث احتقان وریدی موضعی می شود و در کلینیک بسته به محل، تظاهرات مختلفی را نشان می دهد. به عنوان مثال، ترومبوز سینوسی سخت شامه منجر به تصادف عروق مغزی کشنده، ترومبوز ورید باب - به فشار خون باب، ترومبوز ورید طحال - به اسپلنومگالی می شود. با ترومبوز وریدهای کلیوی، در برخی موارد، سندرم نفروتیک یا انفارکتوس وریدی کلیه ایجاد می شود، با ترومبوفلبیت وریدهای کبدی، بیماری هیاری.
اهمیت بالینی ترومبوهای وریدهای گردش خون سیستمیک در این واقعیت نهفته است که آنها به عنوان منبع آمبولی ریه عمل می کنند و بنابراین عوارض کشنده بسیاری از بیماری ها هستند.
آمبولی عبارت است از انتقال ذرات خارجی توسط جریان خون و انسداد مجرای عروق توسط آنها. خود ذرات آمبولی نامیده می شوند. اغلب آمبولی ها قطعات جداگانه ای از لخته های خون هستند که توسط جریان خون حمل می شوند (ترومبوآمبولی).
بسته به جهت حرکت آمبولی، موارد زیر وجود دارد:
آمبولی ارتوگراد (حرکت آمبولی در طول جریان خون)؛
آمبولی رتروگراد (حرکت آمبولی در برابر جریان خون توسط گرانش)؛
آمبولی متناقض (در صورت وجود نقص در سپتوم بین دهلیزی یا بین بطنی، آمبولی از وریدهای دایره بزرگ، با دور زدن ریه ها، وارد شریان ها می شود).
پاتوژنز آمبولی نمی توان آن را تنها به بسته شدن مکانیکی لومن رگ کاهش داد. در ایجاد آمبولی، اسپاسم رفلکس هر دو خط عروقی اصلی و جانبی آن اهمیت زیادی دارد که باعث اختلالات شدید دیسیرکولاتوری می شود. اسپاسم شریان ها می تواند به رگ های جفت یا هر اندام دیگری سرایت کند (به عنوان مثال، رفلکس کلیه-کلیه در صورت آمبولی عروقی یکی از کلیه ها، رفلکس ریوی کرونری در صورت آمبولی ریوی).
محل آمبولی بستگی به محل بروز و اندازه آمبولی دارد. تشکیل آمبولی در وریدهای گردش خون سیستمیک. آمبولی هایی که در وریدهای گردش خون سیستمیک (در نتیجه ترومبوز وریدی) یا در سمت راست قلب (مثلاً با اندوکاردیت عفونی دریچه تریکوسپید) تشکیل می شوند، شریان های دایره کوچک را مسدود می کنند، مگر اینکه چنین باشند. کوچک (به عنوان مثال، قطرات چربی، تومورهای سلولی) که می توانند از مویرگ ریوی عبور کنند. محل انسداد در عروق ریوی به اندازه آمبولی بستگی دارد. به ندرت، آمبولی که در وریدهای دایره بزرگ رخ می دهد، می تواند از نقصی در سپتوم دهلیزی یا بین بطنی عبور کند (در نتیجه دایره کوچک را دور می زند) و باعث آمبولی در شریان های گردش خون سیستمیک (آمبولی متناقض) شود.
آمبولی هایی که در شاخه های ورید باب ایجاد می شوند باعث اختلالات گردش خون در کبد می شوند.
تشکیل آمبولی در قلب و شریان های گردش خون سیستمیک:
آمبولی هایی که در سمت چپ قلب و شریان های گردش خون سیستمیک ایجاد می شوند (در نتیجه ترومبوز قلب یا شریان ها) باعث آمبولی در قسمت های انتهایی دایره سیستمیک می شوند، یعنی. در مغز، قلب، کلیه ها، اندام ها، روده ها و غیره.
ترومبوآمبولی: جدا شدن قطعه ای از ترومبوز و انتقال آن توسط جریان خون شایع ترین علت آمبولی است.
آمبولی ریه (PE)
علل و شیوع: جدی ترین عارضه ترومبوآمبولی آمبولی ریه است که می تواند باعث مرگ ناگهانی شود.
تقریباً 600000 بیمار سالانه به آمبولی ریه در ایالات متحده مبتلا می شوند. تقریباً 100000 نفر از آنها می میرند. در بیش از 90 درصد موارد آمبولی در وریدهای عمقی پاها (فلبوترومبوز) رخ می دهد. به ندرت منبع لخته خون شبکه وریدی لگن است. آمبولی ریه بیشتر در شرایط زیر که مستعد فلبوترومبوز هستند دیده می شود:
1) در حدود 30-50 درصد بیماران پس از مداخلات جراحیدر اوایل دوره پس از عمل، ترومبوز ورید عمقی ایجاد می شود. با این حال، علائم آمبولی ریه تنها در بخش کوچکی از این بیماران رخ می دهد.
2) اوایل دوره پس از زایمان؛
3) بی حرکتی طولانی مدت در رختخواب.
4) نارسایی قلبی؛
5) استفاده از داروهای ضد بارداری خوراکی.
تظاهرات بالینی و اهمیت PE: اندازه آمبولی مهم ترین عامل تعیین کننده درجه تظاهرات بالینی آمبولی ریه و اهمیت آن است. آمبولی بزرگ: آمبولی های بزرگ (چند سانتی متر طول و قطری شبیه به ورید فمورال) می توانند در خروجی بطن راست یا در تنه ریوی متوقف شوند، جایی که گردش خون را مسدود کرده و در نتیجه رفلکس ریوی باعث مرگ ناگهانی می شوند. انسداد با آمبولی شاخههای بزرگ شریان ریوی نیز میتواند باعث مرگ ناگهانی در نتیجه انقباض عروقی شدید تمام عروق گردش خون ریوی شود که به صورت انعکاسی در پاسخ به ظهور ترومبوآمبولی در رگ یا اسپاسم همه برونشها رخ میدهد. آمبولی با اندازه متوسط: افراد سالمشریان برونش پارانشیم ریه را تامین می کند و عملکرد شریان ریوی عمدتاً تبادل گاز است (نه اکسیژن رسانی بافت موضعی).
بنابراین، آمبولی ریوی با اندازه متوسط منجر به ایجاد ناحیهای از ریه میشود که تهویه میشود، اما در تبادل گاز دخالت نمیکند. این باعث اختلال در تبادل گاز و هیپوکسمی می شود، اما انفارکتوس ریه همیشه ایجاد نمی شود. اغلب، حمله قلبی در بیماران مبتلا به نارسایی مزمن قلب بطن چپ (در پس زمینه احتقان وریدی مزمن) یا مبتلا به ریه ایجاد می شود. بیماری های عروقیکه علاوه بر این، خون رسانی از طریق شریان های برونش را مختل کرده و در نتیجه ریه اکسیژن دریافت می کند و مواد مغذیعمدتا از عروق ریوی. در این بیماران، اختلال در جریان خون در شریان ریوی منجر به انفارکتوس ریوی می شود.
آمبولی کوچک: شاخه های کوچک شریان ریوی را مسدود می کند و بسته به شیوع آمبولی ممکن است بدون علائم بالینی ادامه یابد. در بیشتر موارد، آمبولی ها تحت تأثیر فیبرینولیز تجزیه می شوند. اگر آمبولی های کوچک متعدد در گردش خون ریوی به مدت طولانی وارد شود، خطر ابتلا به فشار خون ریوی وجود دارد.
ترومبوآمبولی عروق گردش خون سیستمیک
دلایل: ترومبوآمبولی در رگ های گردش خون سیستمیک زمانی رخ می دهد که آمبولی در نیمه چپ قلب یا یک شریان بزرگ ایجاد شود. ترومبوآمبولی عروق گردش خون سیستمیک معمولاً رخ می دهد:
در بیمارانی که از اندوکاردیت عفونی با پوشش های ترومبوتیک روی دریچه های میترال و آئورت رنج می برند.
در بیمارانی که دچار انفارکتوس میوکارد بطن چپ با ترومبوز جداری شده اند.
در بیماران مبتلا به روماتیسم و بیماری عروق کرونر با آریتمی شدید قلبی (فیبریلاسیون دهلیزی، فیبریلاسیون دهلیزی)، که منجر به تشکیل لخته خون در حفره قلب، اغلب در دهلیز چپ می شود.
در بیماران مبتلا به آنوریسم آئورت و بطن چپ، که در آن ترومب های جداری اغلب تشکیل می شود. ترومبوآمبولی از هر یک از این مکان ها به شریان های اندام های مختلف منتقل می شود. به دلیل آناتومی آئورت، آمبولیهای قلبی بیشتر از سایر شریانهای دایره بزرگ تمایل دارند به اندامهای تحتانی یا شریان کاروتید داخلی راست حمله کنند.
تظاهرات بالینی و اهمیت ترومبوآمبولی گردش خون سیستمیک با اندازه رگ آسیب دیده، توسعه گردش خون جانبی و حساسیت بافت به ایسکمی تعیین می شود. انفارکتوس مغز، قلب، کلیه ها و طحال ممکن است رخ دهد. حمله قلبی در روده ها و اندام های تحتانی تنها با انسداد شریان های بزرگ یا با آسیب به گردش خون جانبی ایجاد می شود.
آمبولی هوا: آمبولی هوا زمانی رخ می دهد که مقدار کافی هوا (تقریباً 150 میلی لیتر) وارد جریان خون شده باشد.
جراحی یا ضربه به ورید ژوگولار داخلی. در صورت آسیب به ورید ژوگولار داخلی، فشار منفی به داخل قفسه سینهمنجر به مکش هوا به داخل آن می شود. هنگامی که سایر وریدها آسیب می بینند این اتفاق نمی افتد، زیرا آنها توسط دریچه هایی از فشار منفی در حفره قفسه سینه جدا می شوند.
زایمان و سقط جنین. به ندرت، آمبولی هوا می تواند در هنگام زایمان یا سقط جنین رخ دهد، زمانی که هوا می تواند در طی انقباضات رحمی به سینوس های وریدی جفت پاره شود.
آمبولی با انتقال خون، انفوزیون داخل وریدی (قطرهانداز)، مطالعات آنژیوگرافی با کنتراست اشعه ایکس. آمبولی هوا تنها زمانی رخ می دهد که تکنیک دستکاری نقض شود.
با تهویه مکانیکی ناکافی در شرایط اکسیژن رسانی هیپرباریک.
تظاهرات بالینی هنگامی که هوا وارد جریان خون می شود، از بطن راست عبور می کند، جایی که یک مخلوط کف آلود ظاهر می شود که جریان خون را به شدت مختل می کند، بسته شدن 2/3 مویرگ های ریه با هوا باعث مرگ می شود.
آمبولی گاز نیتروژن (سندرم رفع فشار).
علل سندرم رفع فشار در غواصان در هنگام صعود سریع از اعماق زیاد، در خلبانان و فضانوردان هنگامی که کابین کم فشار است مشاهده می شود. استنشاق هوا با فشار زیاد زیر آب، افزایش حجم هوا، عمدتاً اکسیژن و نیتروژن، در خون حل می شود و بر این اساس، به بافت ها نفوذ می کند.
در خلال فشردگی سریع، گازهایی که در بافت ها هستند از حالت محلول به حالت گازی عبور می کنند. اکسیژن به سرعت توسط خون جذب می شود، اما نیتروژن نمی تواند به سرعت جذب شود و حباب هایی در بافت ها و خون ایجاد می کند که به عنوان آمبولی عمل می کنند.
تظاهرات بالینی و اهمیت. پلاکت ها به حباب های نیتروژن در جریان خون می چسبند و مکانیسم انعقاد خون را فعال می کنند. ترومبوز داخل عروقی منتشر شده، وضعیت ایسکمیک بافت ها را بدتر می کند که در اثر انسداد مویرگ ها توسط حباب های گاز ایجاد می شود. در موارد شدید، با حل شدن نیتروژن در بافت های غنی از لیپید، نکروز بافت مغز رخ می دهد و منجر به مرگ می شود. در موارد کمتر شدید، ماهیچه ها و اعصابی که آنها را عصب دهی می کنند در درجه اول تحت تأثیر قرار می گیرند. این باعث اسپاسم شدید عضلانی با درد شدید می شود. آمبولی گاز با نیتروژن در ریه ها علت نارسایی تنفسی است و با ادم آلوئولی و خونریزی همراه است.
آمبولی چربی
علل آمبولی چربی زمانی رخ می دهد که قطرات چربی وارد جریان خون شوند. شکستگی استخوان های بزرگ (مانند استخوان ران) ذرات مغز استخوان زرد را وارد جریان خون می کند. به ندرت، آمبولی چربی منجر به آسیب گسترده به بافت چربی زیر جلدی می شود. علیرغم این واقعیت که قطرات چربی در جریان خون در 90٪ بیماران با شکستگی شدید تشخیص داده می شود، علائم بالینی آمبولی چربی بسیار کمتر است.
اگرچه مکانیسم ورود قطرات چربی به جریان خون هنگام پاره شدن سلول های چربی ساده به نظر می رسد، مکانیسم های متعدد دیگری وجود دارد که به تظاهرات بالینیآمبولی چربی مشخص شد که قطرات چربی در جریان خون می توانند اندازه آنها افزایش یابد. این واقعیت را توضیح می دهد که ذرات کوچک چربی که آزادانه از مویرگ های ریوی عبور می کنند می توانند باعث آمبولی در مویرگ های گردش خون سیستمیک شوند. فرض بر این است که آزاد شدن کاتکول آمین ها در نتیجه تروما منجر به بسیج اسیدهای چرب آزاد می شود که به دلیل آن افزایش تدریجی قطرات چربی وجود دارد. چسبندگی پلاکت ها به ذرات چربی منجر به افزایش بیشتر اندازه آنها می شود که همچنین منجر به ترومبوز می شود. هنگامی که این فرآیند به صورت عمومی رخ می دهد، معادل سندرم انعقاد داخل عروقی منتشر است.
تظاهرات بالینی و اهمیت. قطرات چربی در گردش
ابتدا وارد شبکه مویرگی ریه ها می شود. ذرات چربی بزرگ (بیش از 20 میکرومتر) در ریه ها باقی می مانند و باعث ناراحتی تنفسی (تنگی نفس و متابولیسم گاز) می شوند. گلبول های چربی کوچکتر از مویرگ های ریه عبور کرده و وارد گردش خون سیستمیک می شوند. تظاهرات بالینی معمول آمبولی چربی: ظهور بثورات هموراژیک روی پوست و ظهور اختلالات عصبی منتشر حاد. هنگامی که اختلالات تنفسی، اختلالات مغزی و بثورات هموراژیک در روزهای 1-3 پس از آسیب ظاهر می شوند، باید احتمال ایجاد آمبولی چربی را در نظر گرفت. تشخیص را می توان با تشخیص قطرات چربی در ادرار و خلط تایید کرد. تقریباً 10 درصد از بیماران مبتلا به علائم بالینیآمبولی چربی می میرند در طول کالبد شکافی، قطرات چربی را می توان در بسیاری از اندام ها یافت که نیاز به رنگ آمیزی خاصی از داروهای چربی دارد.
آمبولی مغز استخوان: قطعات مغز استخوان حاوی چربی ها و سلول های خونساز می توانند پس از آسیب مغز استخوان تروماتیک وارد جریان خون شوند و می توانند در شریان های ریوی بیمارانی که در حین احیا دچار شکستگی دنده می شوند، پیدا شوند. آمبولی مغز استخوان اهمیت بالینی ندارد.
آمبولی آتروماتوز (آمبولی کلسترول): هنگامی که پلاکهای آتروماتوز بزرگ زخم میکنند، ورود کلسترول و سایر مواد آتروماتوز به جریان خون بسیار رایج است. آمبولی در شریان های کوچک گردش خون سیستمیک، اغلب در مغز مشاهده می شود، که منجر به ظاهر گذرا می شود. حملات ایسکمیک، با توسعه گذرا علائم عصبی مربوط به اختلالات حادگردش خون مغزی
آمبولی با مایع آمنیوتیک: محتویات کیسه آمنیوتیک به ندرت می تواند (1: 80000 تولد) از طریق پارگی های رحم در حین انقباض میومتر در حین زایمان به سینوس های وریدی آن نفوذ کند. اگرچه نادر است، اما آمبولی مایع آمنیوتیک با میزان مرگ و میر بالایی همراه است و علت اصلی مرگ مادران در ایالات متحده است (تقریباً 80٪).
مایع آمنیوتیک حاوی مقدار زیادی مواد ترومبوپلاستیک است که منجر به ایجاد انعقاد داخل عروقی منتشر (DIC) می شود. مایع آمنیوتیک همچنین حاوی اپیتلیوم کراتینه کننده جنین (لایه برداری از پوست)، موهای جنین، چربی جنین، مخاط و مکونیوم است. همه این مواد می توانند باعث آمبولی ریه شوند و تشخیص آنها در کالبد شکافی تشخیص آمبولی مایع آمنیوتیک را تایید می کند. زنان در حال زایمان معمولاً به دلیل خونریزی ناشی از فیبرینولیز به دلیل "انعقاد مصرف" با DIC می میرند.
آمبولی تومور: سلول های سرطانی که رگ های خونی را از بین می برند، اغلب وارد جریان خون می شوند. این فرآیند زمینه ساز متاستاز (از متاستاز یونانی - حرکت) تومورهای بدخیم است. معمولاً این سلولهای منفرد یا گروههای کوچک سلولی آنقدر کوچک هستند که نمیتوانند در گردش خون در اندامها اختلال ایجاد کنند. با این حال، گاهی اوقات قطعات بزرگ تومور می توانند آمبولی های بزرگ (چند سانتی متری) (آمبولی بافتی) ایجاد کنند، به عنوان مثال، در سرطان کلیه، ورید اجوف تحتانی و در سرطان کبد، وریدهای کبدی را تحت تأثیر قرار می دهد.
اغلب، آمبولی های باکتریایی در طی تجزیه سپتیک لخته خون تشکیل می شوند. در محل انسداد رگ، آبسه های متاستاتیک ایجاد می شود: پیش آمبولی عروق گردش خون ریوی - در ریه ها، با آمبولی عروق گردش خون سیستمیک - در کلیه ها، طحال، قلب و سایر اندام ها. .
آمبولی توسط اجسام خارجی زمانی رخ می دهد که گلوله ها، قطعات پوسته و سایر اجسام به مجرای عروق بزرگ برخورد کنند. جرم چنین اجسامی زیاد است، بنابراین بخشهای کوچکی از مسیر خون را عبور میدهند، مثلاً از ورید اجوف فوقانی به سمت قلب راست. بیشتر اوقات، چنین اجسامی در برابر جریان خون در عروق فرو می روند (آمبولی رتروگراد).
معنی. معنای آمبولی مبهم است و با توجه به نوع آمبولی، شیوع آمبولی و محلی شدن آنها مشخص می شود. عوارض ترومبوآمبولی و به ویژه آمبولی ریه که منجر به مرگ ناگهانی می شود از اهمیت بالینی بالایی برخوردار است. ترومبوآمبولی شریان های گردش خون سیستمیک علت شایع انفارکتوس مغز، کلیه ها، طحال، قانقاریا روده، اندام ها است. برای کلینیک، آمبولی باکتریایی به عنوان مکانیسم انتشار اهمیت کمتری ندارد عفونت چرکیو یکی از بارزترین تظاهرات سپسیس است.
خون موضعی یا ایسکمی
کم خونی یا ایسکمی (از یونانی Ischo - مانع کردن، تاخیر) - کاهش یا توقف جریان خون شریانی به اندام، بافت یا بخشی از بدن.
بسته به علل و شرایط وقوع، انواع زیر از کم خونی متمایز می شود:
آنژیو اسپاستیک؛
انسدادی؛
فشرده سازی؛
ایسکمی در نتیجه توزیع مجدد خون.
ایسکمی آنژیو اسپاستیک به دلیل اسپاسم عروق در اثر عمل محرک های مختلف رخ می دهد. آنژیواسپاسم با هر آسیبی (خانگی، عملی، شلیک گلوله) مشاهده می شود، به خصوص اگر همراه با احساس درد، ترس باشد. شرایط کم خونی می تواند در مناطق دورافتاده یک اندام یا اندام ها و بافت ها رخ دهد، به عنوان مثال، نکروز قشر پس از ضربه کلیه ها با آسیب محدود به آنها، شرایط آنوریک در حین عمل بر روی مثانه، تشکیل زخم های حاد معده و اثنی عشر همراه با جراحات. سیستم عصبی مرکزی، سوختگی. آنژیواسپاسم ممکن است با تجویز داروها (مثلاً آدرنالین) رخ دهد.
فرآیندهای آنژیو اسپاستیک می توانند آلرژیک باشند. جنسون و اسمیت (1956) با تجویز مکرر سرم اسب به سگ منجر به انفارکتوس روده شد. حملات قلبی با از بین بردن اولیه گانگلیون های سیستم عصبی خودمختار یا با تجویز داخل وریدی کورتیزون ایجاد نشد. در انسان، حملات قلبی نیز می تواند با کم خونی آنژیو اسپاستیک همراه باشد، و نه به دلیل بسته شدن مکانیکی رگ های خونی، به عنوان مثال، ایسکمی غیر انسدادی روده در بحران فشار خون بالا. ایسکمی آنژیو اسپاستیک نیز با تأثیرات عاطفی منفی ظاهر می شود ("آنژیواسپاسم احساسات بدون واکنش").
ایسکمی انسدادی در نتیجه انسداد مجرای شریان ها رخ می دهد و اغلب با ترومبوز یا آمبولی شریان ها و همچنین با تکثیر بافت همبند در لومن شریان همراه با التهاب دیواره آن (محو کننده) همراه است. اندارتریت) یا باریک شدن مجرای شریان توسط پلاک آترواسکلروتیک. اغلب، ایسکمی انسدادی با آنژیو اسپاستیک ترکیب می شود.
ایسکمی فشاری در نتیجه فشردگی شریان هنگام اعمال تورنیکه، هنگام بستن شریان ها در حین عمل با بستن، و همچنین هنگامی که آنها توسط یک افیوژن التهابی (اگزودا)، تومور، اسکار یا اندام بزرگ شده فشرده می شوند، مشاهده می شود.
ایسکمی ناشی از توزیع مجدد خون (سندرم سرقت). به عنوان مثال، ایسکمی مغزی پس از برداشتن سریع مایع آسیتی از حفره شکمی، جایی که توده زیادی از خون به سرعت جاری می شود.
تغییرات مورفولوژیکی در اندام ها و بافت ها در همه انواع ایسکمی، به هر طریقی، با هیپوکسی یا آنکسی، یعنی با گرسنگی اکسیژن همراه است. بسته به علت کم خونی، ناگهانی بودن آن، مدت و درجه کاهش جریان خون شریانی، ایسکمی حاد و مزمن تشخیص داده می شود.
ایسکمی حاد قطع کامل و ناگهانی جریان خون شریانی به اندام یا بافت است. از نظر میکروسکوپی، در بافت ها، گلیکوژن از بین می رود، فعالیت آنزیم های ردوکس کاهش می یابد و میتوکندری ها از بین می روند. از نظر ماکروسکوپی، چنین ناحیه ای یا کل اندامی رنگ پریده و کسل کننده است. هنگام درمان با نمک های تترازولیوم، که تعیین هیستوشیمیایی درجه فعالیت دهیدروژناز را ممکن می کند، مناطق ایسکمیک بدون رنگ باقی می مانند (فعالیت آنزیم کاهش یافته یا وجود ندارد)، در حالی که مناطق بافت مجاور خاکستری یا سیاه می شوند (سطح فعالیت دهیدروژناز بالا است). . ایسکمی حادباید به عنوان یک وضعیت پیش نکروز (پیش انفارکتوس) در نظر گرفته شود.
ایسکمی مزمن - کاهش طولانی و تدریجی جریان خون شریانی منجر به ایجاد آتروفی سلول های پارانشیمی و اسکلروز استرومایی در نتیجه افزایش فعالیت سنتز کلاژن فیبروبلاست ها می شود. به عنوان مثال، توسعه کاردیواسکلروز در مزمن بیماری ایسکمیکقلبها.
بنابراین، نتیجه ایسکمی ممکن است بازگشت به حالت عادی، آتروفی بافتی یا نکروز باشد. پیامد و اهمیت ایسکمی متفاوت است و به شدت ایسکمی و مدت آن بستگی دارد. علاوه بر این، آنها به عوامل زیر بستگی دارند:
توسعه وثیقه در بافت هایی که شبکه جانبی عروق شریانی به خوبی توسعه یافته است، جریان خون به طور قابل توجهی در صورت مسدود شدن یک شریان کاهش نمی یابد، به عنوان مثال، زمانی که شریان رادیال مسدود می شود، ایسکمی در بازو مشاهده نمی شود، زیرا گردش خون جانبی در امتداد شریان اولنار وجود دارد. اختلال در گردش خون را جبران می کند. در بافت هایی که هیچ وثیقه ای ندارند، انسداد شاخه های انتهایی شریان های تامین کننده بافت منجر به قطع کامل جریان خون و سکته می شود، مثلاً با انسداد شریان مرکزی شبکیه یا شریان مغزی میانی. اگر شدت گردش خون جانبی متوسط باشد، نتیجه انسداد شریان به عوامل دیگری بستگی دارد که در زیر توضیح داده شده است.
شرایط شریان های جانبی. تنگ شدن عروق گردش وثیقهاثربخشی آن را کاهش می دهد؛ به عنوان مثال، هنگامی که شریان کاروتید داخلی در سنین جوانی مسدود می شود، جریان خون معمولاً با افزایش آن در رگ های جانبی دایره ویلیس جبران می شود. با این حال، در سنین بالا، با تنگ شدن آترواسکلروتیک این شریان های جانبی، ایسکمی مغزی اغلب زمانی رخ می دهد که یکی از شریان های کاروتید داخلی مسدود شود. تغییرات ایسکمیک در بافت هایی که معمولاً گردش خون جانبی کافی در آنها وجود دارد (مثلاً در روده ها و اندام ها)، اغلب در بیماران مسن به عنوان نتیجه مستقیم آترواسکلروز گسترده در سنین بالا ایجاد می شود.
اثربخشی عملکرد سیستم قلبی عروقی. برای توسعه جریان خون جانبی، کار موثر قلب و فشار خون بالا لازم است تا خون از طریق شریان های جانبی نسبتاً باریک جریان یابد.
نرخ وقوع موانع انسداد ناگهانی شریان باعث تغییرات ایسکمیک شدیدتر از انسداد تدریجی می شود زیرا زمان کمتری برای رشد عروق جانبی وجود دارد. به عنوان مثال، انسداد ناگهانی یک شریان کرونر در ابتدا طبیعی منجر به انفارکتوس میوکارد می شود. انسداد تدریجی همان شریان باعث آسیب کمتر ایسکمیک به میوکارد می شود (تغییرات دژنراتیو و آتروفی کاردیومیوسیت ها، کاردیواسکلروز) زیرا عروق جانبی زمان بیشتری برای رشد دارند.
حساسیت بافت به ایسکمی. بافت ها از نظر توانایی مقاومت در برابر ایسکمی متفاوت هستند. مغز بسیار حساس است و انفارکتوس در عرض چند دقیقه پس از انسداد شریان رخ می دهد. در مقابل، ماهیچههای اسکلتی، استخوانها و برخی بافتهای دیگر میتوانند چندین ساعت قبل از اینکه دچار اختلال شوند، ایسکمی را تحمل کنند. این با ویژگی های متابولیسم تعیین می شود - غلبه گلیکولیز یا فسفوریلاسیون اکسیداتیو در بافت ها. جراحی فوری برای انسداد شریان بازویی یا فمورال می تواند از نکروز گسترده اندام جلوگیری کند.
سطح متابولیک بافت خنک شدن (هیپوترمی) به دلیل کاهش کلی نیاز متابولیک بافت ها، سرعت شروع آسیب ایسکمیک را کاهش می دهد. این پدیده در برخی از عمل های جراحی و هنگام انتقال اعضا برای پیوند استفاده می شود.
حمله قلبی (از زبان Lat. Infarcire - پر کردن، پر کردن) ناحیه مرده اندام یا بافتی است که در نتیجه قطع ناگهانی جریان خون (ایسکمی) از گردش خون خارج می شود. حمله قلبی نوعی انعقاد عروقی (ایسکمیک) یا نکروز برخوردی... این شایع ترین نوع نکروز است.
هم سلول های پارانشیمی و هم بافت بینابینی دچار نکروز می شوند. اغلب، حمله قلبی با ترومبوز یا آمبولی، اسپاسم، فشرده سازی عروق شریانی رخ می دهد. به ندرت، نقض خروج وریدی می تواند علت حمله قلبی باشد.
دلایل ایجاد حمله قلبی:
ایسکمی حاد به دلیل اسپاسم طولانی مدت، ترومبوز یا آمبولی، فشرده سازی شریان.
تنش عملکردی یک اندام در شرایط کمبود خون. نارسایی آناستوموزها و وثیقه ها که بستگی به درجه دارد
آسیب به دیواره شریان ها و باریک شدن لومن آنها (آترواسکلروز، اندارتریت محو کننده)، از درجه اختلالات گردش خون (به عنوان مثال، استاز وریدی) و از سطح خاموش شدن شریان توسط ترومبوس یا آمبولی.
بنابراین، حملات قلبی معمولا با آن دسته از بیماری ها رخ می دهد که با تغییرات شدید در دیواره رگ ها و اختلالات گردش خون عمومی مشخص می شود. این:
بیماری های روماتیسمی؛
نقص قلبی؛
آترواسکلروز؛
بیماری هایپرتونیک؛
اندوکاردیت باکتریایی (عفونی).
ایجاد انفارکتوس وریدی در ترومبوز وریدی در شرایط توده احتقانی با نارسایی آناستوموزها و وثیقه ها همراه است. برای وقوع حمله قلبی، وضعیت متابولیسم بافت نیز از اهمیت بالایی برخوردار است، یعنی. زمینه متابولیک که در آن انفارکتوس ایسکمیک ایجاد می شود. متابولیسم اندام ها و بافت هایی که در آنها حمله قلبی رخ می دهد معمولاً به دلیل هیپوکسی ناشی از اختلالات گردش خون عمومی مختل می شود. تنها انسداد عروق اصلی بزرگ می تواند بدون اختلالات گردش خون قبلی و اختلالات متابولیک در بافت منجر به نکروز شود.
مورفولوژی حملات قلبی
تصویر ماکروسکوپی از حملات قلبی. شکل، اندازه، رنگ و قوام حمله قلبی ممکن است متفاوت باشد.
شکل حمله قلبی. معمولا حملات قلبی گوه ای شکل هستند. در این حالت، قسمت نوک تیز گوه رو به دروازه اندام است و قسمت وسیعتر به سمت اطراف میرود، مثلاً زیر کپسول اندام، زیر صفاق (سکتههای طحال)، زیر پلور (سکتههای ریوی). )، و غیره. شکل مشخصه حملات قلبی در کلیه ها، طحال، ریه ها با ماهیت آنژیو آرشیتکتونیکی این اندام ها تعیین می شود - نوع اصلی (دوگانه متقارن) انشعاب شریانی. کمتر دچار حملات قلبی می شوند شکل نامنظم... چنین انفارکتوس هایی در قلب، مغز، روده ها مشاهده می شود، زیرا در این اندام ها نه نوع اصلی، بلکه شل یا مختلط انشعاب شریانی غالب است.
بزرگی حملات قلبی. حمله قلبی می تواند بیشتر یا تمام اندام را بپوشاند (انفارکتوس جزئی یا کلی) یا فقط در زیر میکروسکوپ قابل تشخیص است (میکرو انفارکتوس).
رنگ و قوام حملات قلبی. اگر انفارکتوس به صورت نکروز انعقادی ایجاد شود، بافت در ناحیه نکروز متراکم تر می شود، به رنگ خشک، سفید متمایل به زرد می شود (سکته قلبی، کلیه، طحال). اگر حمله قلبی به صورت نکروز برخوردی ایجاد شود، بافت مرده نرم و مایع می شود (سکته مغزی یا کانون نرم شدن خاکستری).
بسته به مکانیسم توسعه و ظاهر، آنها متمایز می شوند:
حمله قلبی سفید (ایسکمیک)؛
حمله قلبی قرمز (هموراژیک)؛
حمله قلبی سفید با تاج هموراژیک.
انفارکتوس سفید (ایسکمیک) در نتیجه قطع کامل جریان خون شریانی به اندام ها، به عنوان مثال، در قلب، کلیه ها، طحال و مغز بالای دایره ویلیس رخ می دهد. معمولاً در مناطقی با یک سیستم جریان خون (نوع اصلی انشعاب شریانی) رخ می دهد که در آن گردش خون جانبی ضعیف است. به دلیل خروج وریدی بدون مزاحمت از بافت ایسکمیک و به دلیل اسپاسم قسمت انتهایی عروق پس از قطع جریان خون، رنگ پریدگی این حملات قلبی مشاهده می شود. انفارکتوس سفید (ایسکمیک) ناحیه ای است که به وضوح از بافت های اطراف محدود شده است، به رنگ سفید مایل به زرد، بدون ساختار.
یک انفارکتوس سفید با یک تاج هموراژیک با یک ناحیه سفید مایل به زرد نشان داده می شود، اما این ناحیه توسط یک منطقه خونریزی احاطه شده است. در نتیجه این واقعیت ایجاد می شود که وازواسپاسم در امتداد حاشیه انفارکتوس با گسترش پارتیک آنها و ایجاد خونریزی جایگزین می شود. چنین حمله قلبی می تواند در کلیه ها، میوکارد رخ دهد.
انفارکتوس قرمز (هموراژیک) با این واقعیت مشخص می شود که ناحیه نکروز از خون اشباع شده است، قرمز تیره و به خوبی مشخص شده است. انفارکتوس به دلیل آزاد شدن خون از رگ های نکروزه عروق ریز در ناحیه انفارکتوس قرمز می شود. برای ایجاد حمله قلبی قرمز، ویژگیهای آنژیوآرشکتتونیک اندام مهم است - دو یا چند سیستم جریان خون، ایجاد وثیقه: در ریهها - وجود آناستوموز بین شریانهای برونش و ریوی، در روده - فراوانی آناستوموزها بین شاخه های شریان های مزانتریک، در مغز در ناحیه دایره ویلیسین آناستوموز بین شاخه های کاروتید و شریان های بازیلار.
انفارکتوس قرمز همچنین می تواند در بافت زمانی رخ دهد که یک ترومب انسدادی حل شود یا تکه تکه شود (پوسیدگی)، که جریان خون شریانی را در ناحیه انفارکتوس بازیابی می کند.
انفارکتوس هموراژیک در کلیه و قلب نادر است. یک پیش نیاز برای چنین خیساندن خونریزی دهنده، استاز وریدی است.
انفارکتوس وریدی زمانی رخ می دهد که کل سیستم تخلیه وریدی بافت مسدود شده باشد (به عنوان مثال، ترومبوز سینوس ساژیتال فوقانی، ترومبوز ورید کلیه، ترومبوز ورید مزانتریک فوقانی). در این حالت، ادم شدید، احتقان، خونریزی و افزایش تدریجی فشار هیدرواستاتیک در بافت ها رخ می دهد. با افزایش شدید فشار هیدرواستاتیک، جریان خون شریانی به بافت دشوار می شود که منجر به ایسکمی و حمله قلبی می شود. انفارکتوس وریدی همیشه خونریزی دهنده است.
انواع خاصی از انفارکتوس وریدی زمانی رخ می دهد که انفارکتوس رخ می دهد (مثلاً وقتی فتق در سوراخ فتق شکسته می شود منجر به انفارکتوس محتویات کیسه فتق می شود) و پیچ خوردگی وریدها (مثلاً پیچ خوردگی). طناب اسپرماتیکمنجر به انفارکتوس هموراژیک بیضه می شود).
بین حملات قلبی آسپتیک و سپتیک تمایز قائل شوید. بیشتر سکته های قلبی اندام های داخلی که با محیط خارجی در تماس نیستند، آسپتیک هستند. انفارکتوس سپتیک زمانی رخ می دهد که یک عفونت باکتریایی ثانویه وارد بافت نکروز شود. انفارکتوس سپتیک زمانی رخ می دهد که:
1) وجود میکروارگانیسم ها در ترومبوس یا آمبولی انسدادی، به عنوان مثال، در آمبولی در اندوکاردیت باکتریایی (سپتیک). 2) ایجاد حمله قلبی در بافت (به عنوان مثال، در روده)، که در آن فلور باکتریایی به طور معمول وجود دارد. انفارکتوس سپتیک با التهاب چرکی شدید مشخص می شود که اغلب منجر به تشکیل آبسه در محل ناحیه انفارکتوس می شود. وجود فلور باکتریایی موجود در اندام های در تماس با محیط خارجی می تواند منجر به تبدیل حملات قلبی در آنها به قانقاریا شود (به عنوان مثال، در روده ها، ریه ها).
از نظر میکروسکوپی، ناحیه مرده با از بین رفتن ساختار، خطوط سلولی و ناپدید شدن هسته ها مشخص می شود.
بیشترین اهمیت بالینی حملات قلبی (میوکارد)، مغز، روده ها، ریه ها، کلیه ها، طحال است.
در قلب، انفارکتوس معمولاً سفید با تاج هموراژیک است، شکلی نامنظم دارد، بیشتر در بطن چپ و سپتوم بین بطنی رخ میدهد، به ندرت در بطن راست و دهلیز. مرگ می تواند در زیر اندوکارد (انفارکتوس زیر قلب)، اپی کارد (انفارکتوس زیر قلب)، در ضخامت میوکارد (داخل ترمورال) قرار گیرد یا کل ضخامت میوکارد را پوشش دهد. سکته مغزی). در ناحیه انفارکتوس، روکش های ترومبوتیک اغلب روی اندوکارد و روکش های فیبرینی روی پریکارد تشکیل می شود که با ایجاد التهاب واکنشی در اطراف محل های نکروز همراه است. اغلب، انفارکتوس میوکارد در پس زمینه آترواسکلروز و فشار خون بالا با اضافه شدن اسپاسم یا ترومبوز شریان ها رخ می دهد که یک شکل حاد از بیماری عروق کرونر قلب است.
در مغز بالای دایره ویلیس، یک انفارکتوس سفید رخ می دهد که به سرعت نرم می شود (مرکز نرم شدن خاکستری مغز). اگر حمله قلبی در پس زمینه اختلالات قابل توجه گردش خون، استاز وریدی ایجاد شود، کانون نکروز مغز از خون اشباع شده و قرمز می شود (تمرکز نرم شدن قرمز مغز). در ناحیه ساقه مغز، زیر دایره ویلیس، حمله قلبی قرمز نیز ایجاد می شود. حمله قلبی معمولاً در گره های زیر قشری موضعی می شود و مسیرهای مغز را از بین می برد که با فلج ظاهر می شود. انفارکتوس مغزی، مانند انفارکتوس میوکارد، اغلب در پس زمینه آترواسکلروز و فشار خون بالا رخ می دهد و یکی از تظاهرات بیماری های عروق مغزی است.
در ریه ها، در اکثریت قریب به اتفاق موارد، انفارکتوس هموراژیک تشکیل می شود. علت آن اغلب ترومبوآمبولی است، کمتر - ترومبوز همراه با واسکولیت. محل انفارکتوس به خوبی مشخص شده است، شکل مخروطی دارد که قاعده آن به سمت پلور است. پوشش های فیبرین (جنب واکنشی) روی پلور در ناحیه انفارکتوس ظاهر می شود. در نوک مخروط، رو به ریشه ریه، ترومبوس یا آمبولی در شاخه شریان ریوی اغلب دیده می شود. بافت مرده متراکم، دانهدار، به رنگ قرمز تیره است. انفارکتوس ریوی هموراژیک معمولاً در پس زمینه استاز وریدی رخ می دهد و توسعه آن تا حد زیادی با ویژگی های آنژیوآرشکتتونیک ریه ها ، وجود آناستوموز بین سیستم شریان های ریوی و برونش تعیین می شود. در شرایط توده احتقانی و بسته شدن مجرای شاخه شریان ریوی، خون از شریان برونش وارد ناحیه نکروز بافت ریه می شود که مویرگ ها را پاره می کند و به لومن آلوئول ها می ریزد. التهاب بافت ریه (پنومونی حوالی انفارکتوس) اغلب حول یک حمله قلبی ایجاد می شود. انفارکتوس هموراژیک شدید ریه می تواند باعث زردی فوق کبدی شود.
حملات قلبی سفید در ریه ها بسیار نادر است. این بیماری با اسکلروز و از بین رفتن لومن شریان های برونش رخ می دهد.
در کلیه ها، انفارکتوس معمولاً سفید با یک تاج هموراژیک است، ناحیه مخروطی شکل نکروز یا قشر یا کل ضخامت پارانشیم را می پوشاند. هنگامی که تنه شریانی اصلی بسته می شود، انفارکتوس کلی یا ساب کل ایجاد می شود. نکروز متقارن قشر کلیه که منجر به ایجاد نارسایی حاد کلیه می شود، نوعی حمله قلبی است. ایجاد انفارکتوس ایسکمیک کلیه معمولاً با ترومبوآمبولی همراه است، کمتر با ترومبوز شاخه های شریان کلیوی در روماتیسم، اندوکاردیت باکتریایی، فشار خون بالا، بیماری عروق کرونر قلب. به ندرت، با ترومبوز سیاهرگ کلیوی، انفارکتوس وریدی کلیه رخ می دهد.
در طحال، انفارکتوس های سفید، اغلب با التهاب فیبرینی واکنشی کپسول و ایجاد چسبندگی های بعدی با دیافراگم، برگ جداری صفاق، و حلقه های روده رخ می دهد. حملات قلبی ایسکمیکطحال همراه با ترومبوز و آمبولی. با ترومبوز ورید طحال، گاهی اوقات، بسیار نادر، انفارکتوس وریدی تشکیل می شود.
در روده، انفارکتوس های هموراژیک و همیشه تحت تجزیه سپتیک قرار می گیرند که منجر به سوراخ شدن دیواره روده و ایجاد پریتونیت می شود.
علت، اغلب، ولولوس، انواژیناسیون روده، فتق خفه شده، کمتر - آترواسکلروز با افزودن ترومبوز است.
نتیجه حمله قلبی
حمله قلبی یک آسیب غیر قابل برگشت بافتی است که با نکروز سلول های پارانشیمی و بافت همبند مشخص می شود. نکروز باعث ایجاد یک واکنش التهابی حاد در بافت های اطراف با استاز و مهاجرت نوتروفیل ها می شود. آنزیم های لیزوزومی نوتروفیل ها باعث لیز بافت مرده در ناحیه انفارکتوس (هترولیز) می شوند. سپس توده های مایع شده توسط ماکروفاژها فاگوسیتوز می شوند. سلول های التهاب حاد با لنفوسیت ها و آکروفاژها جایگزین می شوند. لنفوسیت ها و پلاسماسل ها احتمالاً در پاسخ ایمنی به آنتی ژن های سلولی درون زا آزاد شده در طی نکروز نقش دارند. سیتوکین های آزاد شده توسط سلول های التهاب مزمن تا حدی مسئول تحریک فیبروز و عروق مجدد هستند. متعاقباً تشکیل بافت گرانولاسیون رخ می دهد. در نهایت، تشکیل اسکار رخ می دهد. به دلیل انقباض، اسکار حاصل از نظر حجم کمتر از ناحیه انفارکتوس اولیه است.
سیر انفارکتوس مغزی با آنچه در بالا توضیح داده شد متفاوت است. سلول های نکروزه به دلیل آزاد شدن آنزیم های خود (اتولیز) تحت مایع سازی (تقابل) قرار می گیرند. نوتروفیل ها کمتر از انفارکتوس سایر بافت ها یافت می شوند. سلول های مغز مایع شده توسط ماکروفاژهای ویژه (میکروگلیا) فاگوسیتوز می شوند که به عنوان سلول های بزرگ با سیتوپلاسم دانه ای کم رنگ و کفی (توپ های چربی-گرانولار) تعریف می شوند. ناحیه انفارکتوس به یک حفره پر از مایع تبدیل می شود که توسط دیواره هایی که توسط تکثیر واکنشی آستروسیت ها تشکیل شده است (فرآیندی به نام گلیوز که مشابه فیبروز است) محدود می شود.
سرعت پیشرفت حمله قلبی و زمان لازم برای بهبودی نهایی با توجه به اندازه ضایعه متفاوت است. یک حمله قلبی کوچک ممکن است در عرض 12 هفته بهبود یابد، در حالی که یک ناحیه بزرگتر ممکن است 68 هفته یا بیشتر طول بکشد تا بهبود یابد. تغییرات ماکرو و میکروسکوپی در ناحیه انفارکتوس تخمین سن انفارکتوس را امکان پذیر می کند، که در طی کالبد شکافی برای تعیین توالی وقایع منجر به مرگ مهم است.
به ندرت، کانون های کوچک نکروز ایسکمیک ممکن است تحت اتولیز آسپتیک و به دنبال آن بازسازی کامل قرار گیرند. شایع ترین نتیجه نسبتا مطلوب حمله قلبی که به عنوان نکروز خشک ایجاد می شود، سازماندهی و تشکیل اسکار آن است. سازماندهی حمله قلبی می تواند منجر به تحجر آن شود. گاهی اوقات وقتی نوبت به سازماندهی انفارکتوس هموراژیک می رسد، هموسیدروز رخ می دهد. یک کیست در محل حمله قلبی تشکیل می شود که به عنوان نکروز برخوردی، برای مثال، در مغز ایجاد می شود.
پیامدهای نامطلوب حمله قلبی: 1) ذوب چرکی آن، که معمولاً با آمبولی ترومبوباکتری در سپسیس یا عمل یک عفونت ثانویه (روده ها، ریه ها) همراه است. 2) در قلب - میومالسی و پارگی واقعی قلب با ایجاد هموتامپوناد حفره پریکارد.
معنی حمله قلبی این بر اساس موضع، اندازه و نتیجه حمله قلبی تعیین می شود، اما همیشه برای بدن بسیار بالا است، در درجه اول به این دلیل که حمله قلبی یک نکروز ایسکمیک است، یعنی بخشی از یک عضو از عملکرد خارج می شود. توجه به این نکته ضروری است که حمله قلبی یکی از شایع ترین و وحشتناک ترین عوارض تعدادی از بیماری های قلبی عروقی است. اینها اول از همه آترواسکلروز و فشار خون بالا هستند.
همچنین لازم به ذکر است که حملات قلبی در آترواسکلروز و فشار خون بالا اغلب در اندام های حیاتی - قلب و مغز ایجاد می شود و این امر درصد بالایی از موارد مرگ و ناتوانی ناگهانی را تعیین می کند. اهمیت پزشکی و اجتماعی انفارکتوس میوکارد و عواقب آن باعث شد تا آن را به عنوان تظاهرات یک بیماری مستقل - بیماری ایسکمیک حاد قلب تشخیص دهیم.
اختلالات گردش خون لنفاوی
اختلالات گردش خون لنفاوی از نظر بالینی و مورفولوژیکی عمدتاً به شکل خروج ناکافی لنفاوی ظاهر می شود که اشکال آن می تواند متفاوت باشد.
اولین تظاهرات نقض خروج لنفاوی احتقان لنفاوی و گسترش عروق لنفاوی است. پاسخ جبرانی-تطبیقی در پاسخ به احتقان لنفاوی، ایجاد ضایعات و بازسازی عروق لنفاوی است که به حفرههای دیواره نازک گسترده (لنفانژکتازی) تبدیل میشوند. برآمدگی های متعدد دیوار در آنها ظاهر می شود - گسترش واریسی عروق لنفاوی.
یکی از تظاهرات عدم جبران گردش خون لنفاوی ادم لنفاوی یا لنف ادم است.
لنف ادم می تواند باشد:
محلی (منطقه ای)؛
هر دو لنف ادم عمومی و موضعی می توانند حاد و مزمن در طول دوره باشند.
لنف ادم حاد ژنرالیزه نادر است، مانند ترومبوز دو طرفه ورید ساب کلاوین. در این موارد، با افزایش فشار وریدی در ورید اجوف در مجرای قفسه سینه، رکود رتروگراد ایجاد می شود که تا مویرگ ها گسترش می یابد. تغییرات دیستروفیک در بافت ها تا نکروز سلولی ایجاد می شود.
لنف ادم عمومی مزمن با احتقان وریدی عمومی مزمن مشاهده می شود. علاوه بر دیستروفی، تغییرات آتروفیک و اسکلروتیک ناشی از هیپوکسی مزمن بافتی، در اندامها و بافتها منجر به توسعه میشود.
لنف ادم موضعی حاد زمانی رخ می دهد که انسداد عروق لنفاوی تخلیه (به عنوان مثال آمبولی تومور)، فشرده شدن یا بستن غدد لنفاوی و عروق در حین جراحی و غیره رخ می دهد. به محض ایجاد گردش خون جانبی می تواند خود به خود ناپدید شود.
لنف ادم موضعی مزمن مادرزادی و اکتسابی است. مادرزادی با هیپوپلازی (کمبود) یا آپلازی (فقدان مادرزادی، توسعه نیافتگی) غدد لنفاوی و عروق اندام تحتانی همراه است. لنف ادم موضعی مزمن اکتسابی به دلیل فشرده شدن (تورم) یا متروک شدن عروق لنفاوی (التهاب مزمن، اسکلروز، یا برداشتن جراحی غدد لنفاوی، به عنوان مثال، در سرطان سینه)، همراه با ترومبوز ورید ایجاد می شود. احتقان مزمن لنفاوی منجر به هیپوکسی بافتی می شود و بنابراین اثر فیبروزی دارد. در کلینیک تغییراتی در اندام ها ایجاد می شود که به آن فیل می گویند.
در پس زمینه لنف ادم، استاز لنفاوی (لنفوستاز)، ترومب های پروتئینی ایجاد می شود که با افزایش نفوذپذیری و حتی پارگی مویرگ های لنفاوی و لنفوره توجیه می شود.
ایجاد کیلوس آسیت و شیلوتوراکس با لنفوره داخلی همراه است.
آسیت شیلوس تجمع مایع شیلوس (لنف با محتوای چربی بالا) در حفره شکم با رکود شدید لنف در اندام ها یا با آسیب به عروق لنفاوی روده و مزانتر آن است. مایع چیلوس مانند شیر سفید است.
شیلوتوراکس تجمع مایع شیلوس در حفره پلور به دلیل آسیب به مجرای قفسه سینه در حین جراحی یا با تجویز داروها، انسداد توسط ترومبوز یا فشرده شدن توسط تومور است.
اهمیت نارسایی سیستم لنفاوی، اول از همه، با اختلالات متابولیسم بافت تعیین می شود، که نارسایی نه تنها لنفاوی، بلکه سیستم وریدی (استاز وریدی) نیز منجر به آن می شود.
هیپوکسی در حال توسعه، در اصل، تغییرات کلیشه ای و بدون ابهام در اندام ها و بافت ها در طول رکود لنف و خون ایجاد می کند.
مایع بافتی از نظر پروتئین ضعیف است (1-2٪ نه بیشتر) و در سلول ها با کلوئیدهای پروتئینی و در بافت همبند - با پروتئین ها و گلیکوزامینوگلیکان های ماده اصلی مرتبط است. جرم اصلی آن در ماده بین سلولی است. نقض محتوای مایع بافتی یا در افزایش یا کاهش آن بیان می شود.
ادم تجمع بیش از حد مایع بافتی است. مایع ادماتوز یا ترانسودات (از لاتین trans - through، sudo، sudatum - ooze) شفاف است، حاوی بیش از 2٪ پروتئین نیست.
ادم می تواند در همه بافت ها ایجاد شود، اما به راحتی در بافت زیر جلدی دیده می شود. اولین شواهد بالینی ادم در آن حالت خمیری است - وجود یک قالب (گودی) (هنگام فشار دادن با انگشت، گودی باقی می ماند که پس از قطع فشار ناپدید نمی شود).
تورم قابل مشاهده پوست تنها زمانی رخ می دهد که مقدار زیادی مایع اضافی جمع شده باشد. در مراحل اولیه، به اصطلاح ادم نهفته با وزن کردن بیماران تشخیص داده می شود. ادم همچنین شامل تجمع مایع در حفره های از پیش ساخته شده (از قبل موجود) مانند حفره پلور (هیدروتوراکس، پلورال افیوژن)، شکم (آسیت) و حفره پریکارد (هیدروپریکارد).
Anasarca به معنای ادم عظیم بافت زیر جلدی و اندام های داخلی از جمله حفره ها است. ادم را می توان به صورت زیر طبقه بندی کرد:
محدود (ناشی از نقض موضعی مکانیسم تبادل مایع در بافت).
عمومی یا عمومی (ناشی از احتباس یون سدیم و آب در بدن).
در کلینیک، نقض توزیع مایع در ادم عمومی ناشی از گرانش (گرانش) است، یعنی مایع عمدتاً در اطراف مچ پا در بیماران سرپایی ("راه رفتن") و در ناحیه ساکرال در بیماران "درازکش" تجمع می یابد.
محلی یا محدود و غیره
تبادل مایع از طریق دیواره مویرگی معمولی توسط نیروهای مخالف محدود و تنظیم می شود:
فشار هیدرواستاتیک مویرگی مایع را از رگ هدایت می کند.
فشار کلوئیدی اسمزی پلاسما آن را برمی گرداند.
به طور معمول، اختلاف فشار اسمزی هیدرواستاتیک بافت و فشار اسمزی کلوئیدی نزدیک به صفر است و بر تبادل سیال تأثیری ندارد. مایع از دیواره مویرگی، عمدتاً از فضاهای بین سلول های اندوتلیال (منافذ) عبور می کند، که فقط مولکول های کوچک غیر پروتئینی می توانند از آن عبور کنند (اولترافیلتراسیون). تقریباً تمام پروتئین در رگ باقی می ماند. مقدار کمی پروتئین که از مویرگ خارج می شود به سرعت توسط آن خارج می شود عروق لنفاویبا مقدار کمی مایع که نمی تواند به ونول برگردد. اگر این تعادل به هم بخورد، ادم محدود رخ می دهد.
انواع ادم:
ادم آلرژیک. واکنش های آلرژیک حاد باعث آزاد شدن موضعی مواد وازواکتیو مانند هیستامین می شود که مجرای عروق میکروواسکولار را گسترش می دهد و باعث افزایش نفوذپذیری مویرگی می شود. ادم آلرژیک اغلب در پوست موضعی است، جایی که خود را به صورت تاول (کهیر) نشان می دهد. به طور معمول، مناطق بزرگی از پوست ممکن است تحت تأثیر قرار گیرند و حنجره و برونشیول ها درگیر شوند و باعث باریک شدن راه های هوایی (آنژیوادم) شوند. علیرغم اختلالات عمومی، آنژیوادم به عنوان یک نوع ادم محدود در نظر گرفته می شود، زیرا ناشی از اختلالات موضعی تبادل مایعات است و نه احتباس یون های سدیم و آب در بدن.
ادم ناشی از احتقان وریدی. شدت استاز وریدی به شدت گردش وریدی جانبی در این ناحیه بستگی دارد. در مواردی که احتقان وریدی با نارسایی کامل عملکرد زهکشی سیاهرگ ها همراه باشد، ایجاد می شود. تورم شدیدو خونریزی، از آنجایی که فشار هیدرواستاتیک افزایش می یابد، همراه با پارگی مویرگ ها (به عنوان مثال، ادم و خونریزی های عظیم در مدار همراه با ترومبوز سینوس غار). هنگامی که عملکرد تخلیه وریدها تا حدی مختل می شود، ادم کمتر مشخص می شود (به عنوان مثال، در صورت با انسداد ورید اجوف فوقانی). با انسداد وریدهای اندام، ادم گاهی اوقات ممکن است تلفظ نشود، زیرا گردش خون جانبی عملکرد زهکشی مناسب وریدها را فراهم می کند.
تورم ناشی از احتقان لنفاوی. هنگامی که درناژ لنفاوی مختل می شود، مقدار کمی پروتئین که در اثر پینوسیتوز از مویرگ ها آزاد می شود و در نتیجه اولترافیلتراسیون خارج می شود، خارج نمی شود و در فضای بین بافتی تجمع می یابد. پس از مدتی طولانی و با تجمع پروتئین، فشار کلوئیدی اسمزی در بافت بینابینی افزایش یافته و ادم ایجاد می شود. در ابتدا، ادم لنفاوی ادم شل (خفیف) است. اما در دراز مدت، بافت ادماتیک دچار فیبروز می شود و ناحیه آسیب دیده سفت، متراکم می شود و هیچ فرورفتگی روی آن باقی نمی ماند. فیبروز ممکن است با ضخیم شدن اپیدرم همراه باشد و پوست ظاهری فیل مانند به خود بگیرد (فیلانیازیس).
TOTAL ETHEK
ادم عمومی در نتیجه افزایش تعداد کل یون های سدیم و آب در بدن در حین احتباس آنها توسط کلیه ها، زمانی که سطح فیلتراسیون گلومرولی کاهش می یابد یا ترشح آلدوسترون افزایش می یابد، رخ می دهد. تعادل یونهای سدیم توسط مکانیسمهای زیادی تنظیم میشود: فیلتراسیون یونهای سدیم در گلومرولها (از دست دادن) و بازجذب یونهای سدیم در لولههای پیچیده پروگزیمال و دیستال. استفاده بیشتر از آن در لوله های پیچیده دیستال توسط سیستم رنین-آنژیوتانسین-آلدوسترون تنظیم می شود.
ادم قلبی. نارسایی قلبی با کاهش برون ده خون بطن چپ همراه است. کاهش انتشار خون در گردش خون سیستمیک منجر به کاهش فشار فیلتراسیون در گلومرول ها، تحریک دستگاه juxtaglomerular و ترشح رنین می شود. رنین به نوبه خود باعث افزایش تولید آلدوسترون (آلدوسترونیسم ثانویه) از طریق آنژیوتانسین می شود و یون های سدیم و آب را حفظ می کند که منجر به بروز می شود. ادم عمومی... اگر نارسایی قلب بطن چپ برای مدت طولانی ادامه داشته باشد، به دلیل افزایش فشار وریدی ریوی، آب احتباس شده تمایل دارد در ریهها جمع شود. این عوامل هیدرواستاتیک در ایجاد ادم قلبی در مقایسه با احتباس یونهای سدیم و آب در بدن نقش جزئی دارند، اما در تعیین توزیع مایع باقیمانده مهم هستند. در نارسایی قلب بطن راست، افزایش فشار هیدرواستاتیک سیستمیک به انتهای وریدی مویرگ منتقل می شود و به تجمع مایع در فضای بینابینی کمک می کند.
ادم هیپوپروتئینمی. با هیپوپروتئینمی، فشار کلوئیدی اسمزی پلاسما کاهش می یابد. در نتیجه از دست دادن مایعات در سیستم عروقی و کاهش حجم پلاسما، اسپاسم رفلکس عروق کلیوی رخ می دهد که منجر به ترشح بیش از حد رنین، آلدوسترونیسم ثانویه، احتباس یون های سدیم و آب توسط کلیه ها و ایجاد کلیوی می شود. ادم
هیپوپروتئینمی می تواند ناشی از دریافت ناکافی پروتئین در غذا (ادم ناشتا)، کاهش سنتز آلبومین در کبد (ادم کبدی)، یا افزایش از دست دادن پروتئین در ادرار (سندرم نفروتیک) یا از روده (انتروپاتی از دست دادن پروتئین) باشد.
ادم کلیه. در گلومرولونفریت حاد، سطح فیلتراسیون گلومرولی به طور قابل توجهی کاهش می یابد که منجر به احتباس یون های سدیم و آب و ایجاد ادم متوسط می شود. برخلاف سایر انواع ادم عمومی، با گلومرولونفریت حاد، ادم معمولاً ابتدا در بافت های اطراف چشم، روی پلک ها ظاهر می شود و سپس به دست ها و پاها گسترش می یابد. سایر بیماری های کلیوی، همراه با سندرم نفروتیک و از دست دادن قابل توجه پروتئین در ادرار، منجر به هیپوپروتئینمی می شود و با ادم عمومی گسترده همراه است.
ارزش ادم عمومی
در بیشتر موارد، ادم در ابتدا باعث اختلال در عملکرد سلول های پارانشیمی نمی شود. تورم شدید و مزمن پوست می تواند در بهبود زخم اختلال ایجاد کند و حساسیت به عفونت را افزایش دهد. ادم اندام های داخلی اغلب خود را با علائم مختلفی نشان می دهد، به عنوان مثال، ادم کبد در هپاتیت حاد یا نارسایی قلبی با درد ناشی از کشیده شدن کپسول کبد ظاهر می شود.
تورم برخی از اندام ها تهدید کننده زندگی است:
ادم ریوی. گردش خون ریوی در فشار هیدرواستاتیک پایین (برای شریان ریوی، فشار سیستولیک) عمل می کند.<20 мм рт.ст.). Когда оно становится выше, чем коллоидное осмотическое давление плазмы, небольшое количество жидкости выходит из легочных капилляров. Выход жидкости из легочного капилляра в альвеолы назван отеком легких. Легкие при отеке тяжелые, увеличены в размерах, приобретают тестоватую консистенцию, с поверхности разреза стекает большое количество прозрачной, розоватой, мелкопенистой жидкости. Отечная жидкость вначале скапливается в межуточной ткани (строме), а затем в альвеолах. Отек нарушает газообмен в легких и, в тяжелых случаях, вызывает гипоксию и смерть.
تورم مغز. ادم مغزی در طیف گسترده ای از آسیب های مغزی مشاهده می شود، به عنوان مثال، آسیب تروماتیک، بیماری های عفونی، نئوپلاسم ها و اختلالات عروقی. مایع عمدتاً در فضای خارج سلولی ماده سفید جمع می شود. مایع ادماتوز به طور فیزیکی اتصالات عصبی را می شکند و باعث آسیب حاد مغزی گذرا می شود. افزایش فشار داخل جمجمه ای منجر به سردرد و تورم دیسک بینایی (پاپیلادم) می شود. مغز بزرگ شده است، فضاهای زیر عنکبوتیه و بطن ها گشاد شده و با مایع شفاف پر می شود. ادم مغزی اغلب با تورم همراه است که در برخی موارد غالب است. با تورم مغز، هیدراتاسیون شدید ماده آن رخ می دهد، پیچش ها صاف می شوند، حفره های بطن ها کاهش می یابد. با ادم مغزی، مایع در اطراف عروق و سلول ها تجمع می یابد (ادم اطراف عروقی و اطراف سلولی)، با تورم مغز، تورم آستروسیت ها، تخریب رشته های گلیال و متلاشی شدن میلین مشخص می شود. افزایش فشار داخل مغزی و داخل جمجمه ای وجود دارد. افزایش قابل توجه فشار می تواند لوب گیجگاهی را به سمت دهانه تنتوریوم مخچه جابجا کند (فتق تنتوریوم) یا لوزه های مخچه را به سوراخ مخچه (آمیگدال) منتقل کند که می تواند به دلیل فشرده شدن مخچه منجر به مرگ شود. مرکز وازوموتور در تنه مخچه. مراقبت های فوری مورد نیاز: انفوزیون مانیتول فشار اسمزی پلاسما را افزایش می دهد و مایع را به سرعت از مغز خارج می کند.
کورتیکواستروئیدها با دوز بالا نیز در کاهش ادم مغزی موثر هستند.
ادم حفره های سروزی: تجمع مایع ادماتوز در بورس و فضای پلور می تواند عملکرد طبیعی قلب و انبساط ریه ها را مختل کند. تجمع مایع در حفره شکم (آسیت) باعث اتساع دیواره شکم می شود و معمولاً عملکرد طبیعی اندام های شکمی را به طور قابل توجهی مختل نمی کند.
75-85 میلیلیتر خون به ازای هر 100 گرم وزن قلب (حدود 5 درصد از مقدار حجم دقیقه قلب) از طریق عروق کرونر در انسان در طول استراحت عضلانی در 1 دقیقه جریان مییابد، که به طور قابل توجهی از مقدار جریان خون در هر واحد بیشتر است. واحد وزن سایر اندام ها (به جز مغز، ریه ها و کلیه ها). با کار عضلانی قابل توجه، مقدار جریان خون کرونر متناسب با افزایش برون ده قلبی افزایش می یابد.
میزان جریان خون کرونری به تن عروق کرونر بستگی دارد. تحریک عصب واگ معمولاً باعث کاهش جریان خون کرونر می شود که ظاهراً به کاهش ضربان قلب (برادی کاردی) و کاهش میانگین فشار در آئورت و همچنین کاهش نیاز به اکسیژن قلب بستگی دارد. تحریک اعصاب سمپاتیک منجر به افزایش جریان خون کرونر می شود که ظاهراً به دلیل افزایش فشار خون و افزایش مصرف اکسیژن است که تحت تأثیر نوراپی نفرین آزاد شده در قلب و آدرنالین وارد شده توسط خون. کاتکولامین ها به طور قابل توجهی مصرف اکسیژن میوکارد را افزایش می دهند، بنابراین افزایش جریان خون ممکن است برای افزایش نیاز به اکسیژن قلب ناکافی باشد. با کاهش تنش اکسیژن در بافتهای قلب، عروق کرونر منبسط میشوند و جریان خون از طریق آنها گاهی 2 تا 3 برابر افزایش مییابد که منجر به از بین رفتن کمبود اکسیژن در عضله قلب میشود.
نارسایی حاد کرونر (آنژین صدری)
نارسایی حاد کرونری با عدم تطابق بین نیاز قلب به اکسیژن و تحویل آن به خون مشخص می شود. اغلب، نارسایی با تصلب شرایین، اسپاسم عروق کرونر (عمدتاً اسکلروز شده)، انسداد عروق کرونر توسط ترومبوز، به ندرت آمبولی رخ می دهد. گاهی اوقات می توان نارسایی جریان خون کرونر را با افزایش شدید ضربان قلب (فیبریلاسیون دهلیزی)، کاهش شدید فشار دیاستولیک مشاهده کرد. اسپاسم عروق کرونر بدون تغییر بسیار نادر است. آترواسکلروز عروق کرونر علاوه بر کاهش لومن آنها، باعث افزایش تمایل عروق کرونر به اسپاسم نیز می شود.
نتیجه نارسایی حاد کرونری ایسکمی میوکارد است که باعث اختلال در فرآیندهای اکسیداتیو در میوکارد و تجمع بیش از حد محصولات متابولیک کمتر اکسید شده (لاکتیک، پیروویک و غیره) در آن می شود. در این مورد، میوکارد به اندازه کافی با منابع انرژی (گلوکز، اسیدهای چرب) تامین نمی شود، توانایی انقباض آن کاهش می یابد. خروج محصولات متابولیک نیز دشوار است. با محتوای بیش از حد، محصولات متابولیسم بینابینی باعث تحریک گیرنده های میوکارد و عروق کرونر می شوند. تکانه های حاصل عمدتاً از طریق اعصاب قلب چپ میانی و تحتانی، گره های سمپاتیک گردنی وسطی و پایینی سمت چپ و گره های سینه ای فوقانی و از طریق 5 شاخه اتصال دهنده قفسه سینه بالایی عبور می کنند. رامی ارتباط برقرار می کند) وارد نخاع شود. این تکانه ها پس از رسیدن به مراکز زیر قشری، عمدتاً هیپوتالاموس و قشر مغز، باعث درد مشخصه آنژین صدری می شوند (شکل 89).
انفارکتوس میوکارد
انفارکتوس میوکارد ایسکمی کانونی و نکروز عضله قلب است که پس از اسپاسم یا انسداد طولانی مدت شریان کرونر (یا شاخه های آن) رخ می دهد. عروق کرونر انتهایی هستند، بنابراین، پس از بسته شدن یکی از شاخه های بزرگ عروق کرونر، جریان خون در ناحیه میوکارد که به آن عرضه می شود ده برابر کاهش می یابد و بسیار کندتر از هر بافت دیگری در وضعیت مشابه ترمیم می شود. توانایی انقباض ناحیه آسیب دیده میوکارد به شدت کاهش می یابد و متعاقباً کاملاً متوقف می شود. مرحله انقباض ایزومتریک قلب و به ویژه مرحله اخراج با کشش غیرفعال ناحیه آسیب دیده عضله قلب همراه است که در آینده می تواند منجر به پارگی آن در محل حمله قلبی تازه یا کشش شود. و تشکیل آنوریسم در محل اسکار حمله قلبی (شکل 90). تحت این شرایط، نیروی پمپاژ قلب به طور کلی کاهش می یابد، زیرا بخشی از بافت انقباضی خاموش می شود. علاوه بر این، بخش معینی از انرژی میوکارد دست نخورده برای کشش مناطق غیر فعال تلف می شود. توانایی انقباضی نواحی دست نخورده میوکارد نیز در نتیجه نقض خون رسانی آنها کاهش می یابد که ناشی از اسپاسم فشرده یا رفلکس عروق نواحی دست نخورده است (به اصطلاح رفلکس بین کرونری).
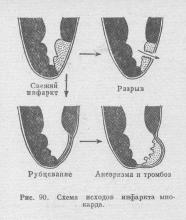
مکانیسم های تضعیف انقباض میوکارد در انفارکتوس به طور مفصل در این آزمایش مورد مطالعه قرار گرفته است.
انفارکتوس میوکارد تجربی... ایسکمی کانونی میوکارد با نکروز متعاقب آن در حیوانات آزمایشگاهی با بستن یکی از شاخه های شریان کرونری قلب به راحتی تکثیر می شود. پس از بستن شریان کرونر در میوکارد، محتوای کوآنزیم A، که برای سنتز استیل کولین ضروری است، کاهش می یابد. همراه با این، جریان کاتکول آمین ها به قلب - نوراپی نفرین و آدرنالین - افزایش می یابد، که به طور قابل توجهی مصرف اکسیژن توسط عضله قلب را بدون توجه به کار انجام شده توسط آن افزایش می دهد. به دلیل عدم امکان جریان خون کافی به نیازهای قلب، درجه هیپوکسی در میوکارد به شدت افزایش می یابد. در شرایط بی هوازی، متابولیسم کربوهیدرات ها مختل می شود - ذخایر گلیکوژن تخلیه می شود، محتوای اسیدهای لاکتیک و پیروویک افزایش می یابد و اسیدوز ایجاد می شود.
متلاشی شدن سلول با آزاد شدن یون های K + از آنها همراه است. پتاسیم که در ناحیه انفارکتوس آزاد می شود، عمدتاً در ناحیه پری کانونی متمرکز می شود. آنزیم ها و سایر مواد فعال بیولوژیکی که می توانند آسیب میوکارد را بیشتر تشدید کنند از سلول های آسیب دیده ناحیه نکروز آزاد می شوند. در برخی موارد، نتیجه آسیب به ساختارهای پروتئینی میوکارد، تشکیل اتوآلرژنها و متعاقب آن تولید اتوآنتیبادیهای اختصاصی علیه آنها است. تثبیت دومی در نواحی دست نخورده میوکارد می تواند باعث ضایعات بعدی آن شود.
نکروز میوکارد، از نظر اختلالات متابولیک مشابه با انفارکتوس در انسان، می تواند در حیوانات آزمایشگاهی با قرار گرفتن در معرض برخی از مواد دارویی و شیمیایی (به عنوان مثال، تجویز آدرنالین، عصاره دیژیتال، آماده سازی ارگوسترول تحت تابش و غیره) به دست آید. Selye نکروز میوکارد را در موشهای تحت درمان با داروهای کورتیکوئیدی تولید مثل کرد، مشروط بر اینکه نمکهای سدیم اضافی به رژیم غذایی آنها وارد شود. به نظر او، برخی از نمک های سدیم، عضله قلب را نسبت به اثرات مخرب کورتیکواستروئیدها "حساس" می کند.
تغییرات در نوار قلب در انفارکتوس میوکارد... انفارکتوس میوکارد با نقض ریتم قلب مشخص می شود که از همان ابتدای ایجاد حمله قلبی ظاهر می شود. مشخص ترین تغییرات در الکتروکاردیوگرام، جابجایی قطعه RST و تغییر در کمپلکس QRS و موج T است. این تغییرات می تواند نتیجه ایسکمی، گسترش به سیستم هدایت قلب و همچنین تأثیرات ناشی از قلب باشد. محل نکروز
کل ناحیه ضایعه در انفارکتوس میوکارد را می توان به سه منطقه تقسیم کرد: منطقه مرکزی نکروز، منطقه اطراف "آسیب" و محیطی ترین - منطقه ایسکمی. وجود ناحیه نکروز و متعاقباً یک اسکار، تغییر در کمپلکس QRS و به ویژه ظهور یک موج Q عمیق را توضیح می دهد.
منطقه "آسیب" باعث جابجایی بخش RST می شود و منطقه ایسکمی منجر به تغییر در موج G می شود. نسبت های مختلف مقادیر این مناطق در مراحل مختلف بیماری، پویایی پیچیده تغییرات را توضیح می دهد. در الکتروکاردیوگرام در انفارکتوس میوکارد (شکل 91).
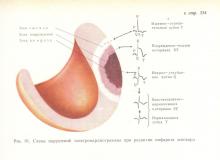
شوک قلبی... این یک سندرم نارسایی حاد قلبی عروقی است که به عنوان عارضه انفارکتوس میوکارد ایجاد می شود. از نظر بالینی، خود را به صورت ضعف شدید ناگهانی، رنگ پریدگی پوست با ته سیانوتیک، عرق چسبنده سرد، افت فشار خون، نبض سریع کوچک، بی حالی بیمار و گاهی اوقات اختلال کوتاه مدت در هوشیاری نشان می دهد.
در پاتوژنز اختلالات همودینامیک در شوک کاردیوژنیک، سه پیوند ضروری است:
- 1) کاهش سکته مغزی و حجم دقیقه قلب (شاخص قلبی زیر 2.5 لیتر در دقیقه / متر مربع)؛
- 2) افزایش قابل توجه مقاومت شریانی محیطی (بیش از 1800 دین در ثانیه).· سانتی متر + 5)؛
- 3) نقض میکروسیرکولاسیون.
کاهش در دقیقه و حجم ضربه ای قلب در انفارکتوس میوکارد با کاهش شدید انقباض عضله قلب به دلیل نکروز ناحیه کم و بیش گسترده آن مشخص می شود. نتیجه کاهش حجم دقیقه قلب کاهش فشار خون است.
افزایش مقاومت شریانی محیطی با توجه به این واقعیت که با کاهش ناگهانی حجم دقیقه قلب و کاهش فشار خون، بارورسپتورهای سینوکاروتید و آئورت فعال می شوند، مقدار زیادی از مواد آدرنرژیک به صورت انعکاسی در خون آزاد می شود و باعث انقباض گسترده عروق می شود. با این حال، مناطق مختلف عروقی واکنش متفاوتی به مواد آدرنرژیک نشان میدهند که منجر به درجه متفاوتی از افزایش مقاومت عروقی میشود. در نتیجه، توزیع مجدد خون اتفاق می افتد: جریان خون در اندام های حیاتی با انقباض رگ های خونی در نواحی دیگر حفظ می شود.
با این حال، انقباض عروق محیطی طولانیمدت و بیش از حد در یک محیط بالینی اهمیت پاتولوژیک پیدا میکند و به اختلال در مکانیسم پیچیده میکروسیرکولاسیون با اختلال در جریان خون محیطی و ایجاد تعدادی تغییرات شدید، گاهی غیرقابل برگشت، در اندامهای حیاتی کمک میکند.
اختلالات میکروسیرکولاسیون در شوک قلبی به صورت اختلالات وازوموتور و داخل عروقی (ریوگرافیک) ظاهر می شود. اختلالات وازوموتور میکروسیرکولاسیون با اسپاسم سیستمیک شریانها و اسفنکترهای پیش مویرگی همراه است که منجر به انتقال خون از شریانها به ونولها توسط آناستوموزها و دور زدن مویرگها میشود. در این حالت، خون رسانی به بافت ها به شدت مختل می شود و پدیده هایپوکسی و اسیدوز ایجاد می شود. اختلالات متابولیسم بافت و اسیدوز منجر به شل شدن اسفنکترهای پیش مویرگی می شود. اسفنکترهای پس مویرگی که کمتر به اسیدوز حساس هستند، در حالت اسپاسم باقی می مانند. در نتیجه، خون در مویرگ ها جمع می شود که برخی از آنها از گردش خون خارج می شوند. فشار هیدرواستاتیک در مویرگ ها افزایش می یابد و تخلیه مایع به بافت های اطراف آغاز می شود. در نتیجه حجم خون در گردش کاهش می یابد. در همان زمان، تغییراتی در خواص رئولوژیکی خون رخ می دهد - تجمع داخل عروقی گلبول های قرمز رخ می دهد که با کاهش سرعت جریان خون و تغییر در بخش های پروتئینی خون و همچنین شارژ گلبول های قرمز همراه است.
تجمع گلبول های قرمز باعث کاهش بیشتر جریان خون می شود و به بسته شدن مجرای مویرگ ها کمک می کند. به دلیل کاهش سرعت جریان خون، ویسکوزیته خون افزایش می یابد و پیش نیازهای تشکیل میکروترومبی ایجاد می شود که با افزایش فعالیت سیستم انعقاد خون در بیماران مبتلا به انفارکتوس میوکارد که با شوک عارضه شده است، تسهیل می شود.
نقض جریان خون محیطی با تجمع داخل عروقی واضح گلبول های قرمز، رسوب خون در مویرگ ها منجر به عواقب خاصی می شود:
- الف) بازگشت وریدی خون به قلب کاهش می یابد، که باعث کاهش بیشتر در حجم دقیقه قلب و نقض شدیدتر خون رسانی به بافت ها می شود.
- ب) گرسنگی اکسیژن بافت ها به دلیل حذف گلبول های قرمز از گردش خون عمیق می شود.
در شوک شدید، یک دور باطل رخ می دهد: اختلالات متابولیک در بافت ها باعث ظهور تعدادی از مواد وازواکتیو می شود که به ایجاد اختلالات عروقی و تجمع گلبول های قرمز کمک می کند، که به نوبه خود از اختلالات موجود در متابولیسم بافت پشتیبانی می کند و عمیق تر می شود. با افزایش اسیدوز بافتی، اختلالات عمیق سیستم های آنزیمی رخ می دهد که منجر به مرگ عناصر سلولی و ایجاد نکروز کوچک در میوکارد، کبد و کلیه ها می شود.
طبقه بندی
اختلالات گردش خون شامل فرآیندهای پاتولوژیک اصلی زیر است:
- پرخونی
- ایسکمی
- خون ریزی
- ترومبوز
- آمبولی
- شوکه شدن.
هایپرمی (کلیدور)
پرخونی- افزایش حجم خون در بستر عروقی.
طبقه بندی
هایپرمی به دو دسته شریانی و وریدی (احتقانی) تقسیم می شود.
I. پرخونی شریانی
- .
II. پرخونی وریدی (احتقانی).
- هیپرمی وریدی عمومی(حاد و مزمن)
- هیپرمی وریدی موضعی.
پرخونی شریانی
پرخونی شریانی- پرخونی به دلیل افزایش جریان خون شریانی.
هیپرمی شریانی می تواند نه تنها در شرایط آسیب شناسی ایجاد شود. بنابراین، هیپرمی شریانی فیزیولوژیکی عمومیدر طول کار فیزیکی شدید و دمای بالای محیط رخ می دهد. هیپرمی شریانی فیزیولوژیکی موضعیبا بارگیری از یک گروه عضلانی خاص، هیپرترمی موضعی، با تعدادی از احساسات مشخص می شود.
اشکال پاتولوژیک هیپرمی شریانی نیز به عمومی (تعمیم) و موضعی (محلی) تقسیم می شود.
هیپرمی شریانی پاتولوژیک عمومی
هیپرمی شریانی پاتولوژیک عمومیرخ می دهد (1) در بیماری رفع فشار (پرخونی عمومی خالی) و (2) برای پلی سیتمی ورا(لوسمی مزمن با افزایش قابل توجه تعداد گلبول های قرمز خون در خون محیطی). افزایش حجم خون به دلیل تعداد عناصر تشکیل شده نامیده می شود بازیکن: این با قرمزی مداوم پوست، به ویژه پوست صورت مشخص می شود.
هیپرمی شریانی پاتولوژیک موضعی
به هیپرمی شریانی پاتولوژیک موضعیشامل اشکال زیر احتقان عروقی است:
- هیپرمی آنژینوروتیک(در صورت نقض عصب عروق شریانی)
- پرخونی پس از ایسکمیک(با حذف سریع فاکتور ایسکمیک)
- پرخونی خالی موضعی(با کاهش سریع موضعی فشار هوا)
- پرخونی التهابی(با التهاب)
- پرخونی جانبی(با انسداد شریان اصلی)
- هایپرمی، در صورت وجود شانت شریانی وریدی(آناستوموز پاتولوژیک بین شریان و ورید).
هیپرمی آنژینوروتیکدر بیشتر موارد با فلج اعصاب منقبض کننده عروق شریان ها و شریان های کوچک رخ می دهد. پرخونی عصبی پارالیتیک). مکانیسم دیگری برای ایجاد پرخونی آنژیونورتیک مستثنی نیست - تحریک اعصاب گشادکننده عروقی که در انسان در تعدادی از اندام ها (به عنوان مثال، در پیا ماتر مغز) یافت می شود. یک نمونه کلاسیک پرخونی عصبی فلج کننده، قرمزی پوست صورت، گردن و قسمت بالایی بدن در تیفوس (در طول اوج بیماری) به دلیل آسیب به عقده های سمپاتیک گردنی و بر این اساس اعصاب منقبض کننده عروق سمپاتیک است.
پرخونی خالی موضعیدر تعدادی از کتابهای درسی تأثیر قوطیهای پزشکی نشان داده شده است، با این حال، تغییرات برگشتپذیر در عروق خونی در طی اقدامات پزشکی به سختی میتواند به فرآیندهای پاتولوژیک نسبت داده شود. نمونه ای از پرخونی خالی موضعی هستند لکه های میناکوف- لکه هایی به رنگ قرمز تیره که از سمت اندوکارد بطن چپ در صورت مرگ ناشی از از دست دادن خون شدید حاد تشخیص داده می شود. مکانیسم تشکیل لکه های میناکوف اثر نیروی انبساط بطن چپ "خالی" بر بافت اندوکارد و لایه زیر اندوکاردی میوکارد است. در عین حال، کاهش سریع فشار هوا در این بافت ها وجود دارد که با افزایش جریان خون شریانی به داخل عروق همراه است.
پرخونی التهابیبه انواع پرخونی شریانی پاتولوژیک تا حدی مشروط اشاره دارد. اولا، التهاب به خودی خود یک فرآیند پاتولوژیک نیست، یک واکنش محافظ و سازگاری بدن است. ثانیا، پرخونی التهابی برای مدت بسیار کوتاهی شریانی باقی می ماند و به سرعت ابتدا به پرخونی مختلط (شریانی-وریدی) و سپس به پرخونی وریدی تبدیل می شود.
پرخونی وریدی (احتقانی).
پرخونی وریدی (پرخونی احتقانی) - کاهش سرعت خروج و تاخیر در بافت خون وریدی.
تمیز دادن عمومی(با نارسایی قلبی) و محلی(با مشکل در جریان خون از طریق یک رگ وریدی خاص) پرخونی. پرخونی احتقانی عمومی به دو دسته تقسیم می شود حاد(با سندرم نارسایی حاد قلبی) و مزمن(با نارسایی مزمن قلبی).
پرخونی حاد وریدی عمومیبا ایجاد دو نوع تغییر بافت مشخص می شود: (1) ادم به دلیل افزایش فشار خون در عروق وریدی بیش از حد شلوغ و (2) فرآیندهای جایگزین به دلیل هیپوکسی. در برخی موارد خونریزی های دور عروقی کوچکی در بافت مشاهده می شود که در اثر اریترودیاپدزیس ایجاد می شود.
پرخونی وریدی عمومی مزمن
احتقان وریدی عمومی مزمنهمراه با ادم و فرآیندهای جایگزین، توسعه (1) اسکلروتیک (فیبروز) و 2) آتروفیکتغییرات در بافت اندام های مختلف. فیبروزفشردگی اندام ها را تعیین می کند، آتروفی پارانشیمیمنجر به آنها می شود اختلال عملکرد.
بارزترین تغییرات در پوست، کبد، ریه ها، طحال و کلیه ها ایجاد می شود.
چرمبه خصوص در اندام تحتانی، سفت، ادم، سیانوتیک، سرد در لمس، خشک، گاهی اوقات با زخم های طولانی مدت غیر التیام دهنده ("تروفیک") است.
تغییر در کبددر سه مرحله انجام می شود: کبد جوز هندی، فیبروز احتقانی جوز هندی و سیروز قلبی (احتقانی).
1.در مراحل کبد جوز هندیاندام بزرگ شده، متراکم شده است، بر روی برش یک رنگ متلاطم (مانند هسته جوز هندی) - در زمینه خاکستری مایل به زرد (نتیجه انحطاط چربی سلول های کبدی)، چندین نواحی کوچک قرمز تیره (مراکز پر خون لوبول ها) قابل مشاهده هستند.
2. وقتی فیبروز جوز هندیکبد به دلیل تکثیر بافت فیبری متراکم است، بافت بر روی برش متنوع است ("مسقط برعکس") - در برابر پس زمینه قرمز تیره (نتیجه جابجایی مجموعه از مرکز لوبول ها به سمت حاشیه) تعداد زیادی کانون خاکستری کوچک (فیبروز در مرکز لوبول ها) یافت می شود.
3. درباره سیروز قلبیآنها می گویند در صورت تغییر شکل کبد (سطح آن ناهموار می شود).
تغییر در ریه هانامیده می شوند استحکام قهوه ای: بافت ریه فشرده، پر خون، به رنگ قهوه ای زنگ زده به دلیل هموسیدروزیس، هوای آن کاهش می یابد، بررسی میکروسکوپی سیدروبلاست های متعدد و فیبروز را نشان می دهد.
تغییرات کلیهو طحالبا نارسایی مزمن قلبی نامیده می شوند استحکام سیانوتیکبه دلیل ظاهر مشخص آبی رنگ این اندام ها از سطح.
هیپرمی وریدی موضعی
توده احتقانی موضعی به دلیل نقض جریان خون از طریق عروق وریدی خاص ایجاد می شود. سه نوع اصلی پرخونی وریدی موضعی وجود دارد - انسدادی, فشرده سازیو وثیقهپرخونی
پرخونی انسدادیزمانی رخ می دهد که مانعی برای جریان خون در مجرای رگ وجود داشته باشد (اغلب چنین مانعی ترومبوز است).
هیپرمی فشاریبه دلیل فشرده شدن رگ وریدی (تومور، ترانسودات، لیگاتور و غیره) ایجاد می شود.
وثیقهتوده وریدی در سیروز کبدی نامیده می شود، زمانی که خون از اندام های شکمی قادر به جریان یافتن از طریق کبد نیست، رگ های آن توسط گره های بازسازی شده فشرده می شوند. در همان زمان، خون به آناستوموزهای کاوا-کاوال و پورت-کاوال سرازیر می شود و آنها را بیش از حد پر می کند و گسترش می دهد. اینطوری " سر چتر دریایی(رگ های پر خون دیواره قدامی شکم که به صورت شعاعی از ناف منحرف می شوند) و وریدهای واریسی مری، مملو از خونریزی کشنده است.
سیانوز همراه با پرخونی وریدی
توده وریدی با ظهور رنگ مایل به آبی بافت ها همراه است (سیانوز، "سیانوز"). با این حال، خون وریدی به رنگ قرمز تیره و بدون رنگ آبی است. در واقع، بافت های سیانوتیک از سطح (پوست، اندام های داخلی از سمت کپسول) به نظر می رسند، هنگامی که جدا می شوند، سیانوز ناپدید می شود و جای خود را به رنگ معمولی خون وریدی می دهد. سیانوز ناشی از توهم بینایی است - اثر تیندالکه به آن " پدیده کنتراست کف". امواج نوری با طول موج بیشتر (قرمز) توسط بافت همبند فیبری متراکم درم یا کپسول اندام ها جذب می شوند، در حالی که تابش نوری موج کوتاه (ناحیه آبی طیف) که قدرت نفوذ بیشتری دارد، به شبکیه چشم ناظر می رسد. "لکه کردن" بافت با تراکم راکد به رنگ آبی.
ایسکمی
ایسکمی- عرضه ناکافی خون شریانی به اندام. ایسکمی همیشه یک فرآیند موضعی است، بنابراین به آن "کم خونی موضعی" نیز می گویند (بر خلاف کم خونی - "کم خونی عمومی"). ایسکمی طولانی مدت با توسعه به پایان می رسد حمله قلبی... این فرآیند پاتولوژیک زمینه ساز بیماری های رایجی مانند ایسکمی قلبی(بیماری ایسکمیک قلب) و سکته مغزی ایسکمیک.
طبقه بندی
اشکال ایسکمی به شرح زیر طبقه بندی می شوند:
I. اصل پاتوژنتیک
- ایسکمی انسدادی
- ایسکمی فشرده سازی
- ایسکمی آنژیو اسپاستیک[به ویژه زمانی که توسعه می یابد آنژین پرینزمتال]
- ایسکمی توزیع مجدد.
II. ماهیت فرآیند
- ایسکمی حاد
- ایسکمی مزمن.
ایسکمی انسدادیزمانی رخ می دهد که انسدادی در جریان خون در مجرای شریان (ترومبوز یا آمبولی) وجود داشته باشد. ایسکمی فشرده سازیناشی از فشردگی رگ شریانی (تورم، مایع ادماتوز، لیگاتور و غیره). ایسکمی آنژیو اسپاستیکبه دلیل باریک شدن طولانی مدت مجرای رگ در نتیجه اسپاسم شریانی.
ایسکمی توزیع مجددهمراه با پرخونی شریانی پس از ایسکمیک. به طور سنتی، ایسکمی توزیع مجدد با مثال آسیت توضیح داده می شود. ترانسودات در حفره صفاقی با آسیت عروق اندام های مربوطه را فشرده می کند. ایسکمی فشرده سازی، باعث نقض برگشت پذیر عصب سمپاتیک رگ های خونی، در درجه اول شریان ها و شریان ها می شود. با استخراج سریع مایعات و در نتیجه حذف عامل فشرده سازی عروقی، خون شریانی بیش از حد آنها را پر می کند. هیپرمی شریانی پس از ایسکمیک). در همان زمان، سایر اندام ها (در درجه اول مغز) فاقد خون شریانی هستند، به عنوان مثال. ایسکمی در بافت آنها ایجاد می شود که به عنوان نشان داده شده است بازتوزیعی... به منظور جلوگیری از ایسکمی توزیع مجدد، مایع ادماتوز در آسیت به آرامی برداشته می شود و به اعصاب منقبض کننده عروق عروق فشرده اجازه می دهد تا عملکرد خود را بازیابی کنند.
تست ماکروسکوپی برای نکروبیوز پس از ایسکمیک
در عمل پس از مرگ، تشخیص تغییرات نکروبیوتیک در میوکارد که در نتیجه ایسکمی ایجاد شده است "در جدول بخش" ضروری است. در شکل حاد بیماری ایسکمیک قلبی، مرگ می تواند نه تنها در مورد انفارکتوس تشکیل شده با ظاهر معمولی یک کانون سفید نکروز، که در محیط اطراف توسط یک تاج هموراژیک احاطه شده است، بلکه در مرحله قبل از انفارکتوس (نکروبیوتیک) رخ دهد. . در عین حال، تحقیقات ماکرومورفولوژیکی امکان تشخیص بیماری عروق کرونر را نمی دهد و فناوری استاندارد برای تولید ریز آماده سازی با کیفیت بالا چندین روز طول می کشد. در چنین مواردی، برای تشخیص سریع دیستروفی ایسکمیک میوکارد(این نام شکل بیماری ایسکمیک قلبی با تغییرات نکروبیوتیک در کانون ایسکمی است) می توانید از تست ماکروسکوپی با نمک های تترازولیوم (تترازولیوم نیترو آبی) یا تلوریت پتاسیم... واضح ترین آزمایش با تلوریت پتاسیم است. یک معرف روی برش تازه میوکارد اعمال می شود: مناطقی از عضله قلب بدون علائم نکروز به دلیل کاهش تلوریوم تحت تأثیر اکسیدوردوکتازهای کاردیومیوسیت سیاه می شوند و مناطق نکروزی فاقد مقدار کافی آنزیم های ردوکس هستند. ، بدون لکه می ماند.
خون ریزی
خون ریزی (خونریزی) - خروج خون به خارج از عروق یا حفره های قلب.
طبقه بندی
اشکال اصلی خونریزی زیر وجود دارد:
I. اصل پاتوژنتیک
- خونریزی در هر رکسین
- خونریزی از طریق دیابروزین (خونریزی خورنده)
- هموراژی در دیاپدزین (خونریزی دیاپدزی)
- خونریزی روانی.
II. جهت خونریزی
- خونریزی خارجی
- خونریزی داخلی
- خونریزی.
پاتوژنز خونریزی
با توجه به مکانیسم ایجاد، چهار نوع خونریزی متمایز می شود: خونریزی در هر رکسین، خونریزی در هر دیابروزین، خونریزی در هر دیاپدزین و نوع به اصطلاح روان زا.
1. هموراژی در دیاپدزین (خونریزی دیاپدزی) به دلیل افزایش نفوذپذیری دیواره ریزرگ ها رخ می دهد. در این مورد، گلبول های قرمز از طریق عیوب دیواره ("منافذ"، "شکاف") از مجرای رگ خارج می شوند: این فرآیند نامیده می شود. اریترودیاپدزیسو تجمع گلبول های قرمز در بافت اطراف عروقی - زیاده روی.
خونریزی در هر رکسین و خونریزی در هر دیابروزین یک ویژگی مشابه دارند - تخریب دیواره عروق. اگر دیواره عروق در نتیجه انتقال فرآیند پاتولوژیک از بافت های اطراف به آن از بین برود، آنها از مکانیسم per diabrosin صحبت می کنند. دیابروزین- خوردگی)؛ اگر فرآیندی که به تخریب دیوار ختم شد، مستقیماً در بافتهای آن (در ضخامت دیواره رگ) ایجاد شد یا رگ در اثر عمل مکانیکی از بین رفت، آنها از مکانیسم per rexin صحبت میکنند. رکسین- شکاف).
2. خونریزی از طریق دیابروزین (خونریزی خورنده) تحت تأثیر عوامل اصلی زیر ایجاد می شود:
- التهاب چرکی(اثر چرکی خاصیت هیستولیتیک مشخص دارد)
- نکروز(به عنوان مثال، نکروز کازئوس در سل)
- اسید هیدروکلریک و آنزیم های گوارشی(با فرسایش و زخم معده، اثنی عشر)
- رشد تومور مهاجم
- رشد پرزهای کوریونی به دیواره عروق در طول حاملگی خارج از رحم.
3. دلایل خونریزی در هر رکسینعبارتند از: (1) آسیب مکانیکی به دیواره عروق و (2) یک فرآیند مخرب که عمدتاً در خود دیواره عروق ایجاد می شود (به عنوان مثال، پارگی آئورت با مزارتیت سیفلیس یا پارگی عروق با نکروز فیبرینوئیدی بافت های دیواره آن. ).
4. درباره وجود خونریزی روانی(توانایی ایجاد خونریزی در خود با "قدرت فکر") معمولاً در متون علمی ذکر نشده است ، اما در تک نگاری زینوی سولومونوویچ بارکاگان "بیماری ها و سندرم های هموراژیک" (1980) در پایان ذکر نشده است. از کتاب، مشاهدات خود نویسنده آورده شده است: زن جوانی که چند دقیقه در حالت تنش نشسته بود، توانست خونریزی نقطهای از لاله گوش ایجاد کند.
خونریزی خارجی
خونریزی خارجی- خونریزی، که در آن خون در خارج از بافت های پوششی (پوست یا غشاهای مخاطی) جریان می یابد.
انواع اصلی خونریزی خارجی عبارتند از:
- خون دماغ شدن(اپیستاکسیس) - خونریزی بینی
- هموپتو(hemoptísis, haematoptóe, haematoptísis) - هموپتیزی [هموپتیزی تلفظ شده نامیده می شود خونریزی ریوی]
- هماتمزیس- استفراغ خونی (استفراغ تفاله قهوه)
- ملنا(ملنا) - ترشح خون تغییر یافته با مدفوع ("مدفوع قیری")
- متروراژی(متروراژی) - خونریزی غیر حلقوی رحم [با فاز خونریزی مشخص چرخه قاعدگی، آنها در مورد منوراژی]
- هماچوری(هماچوری) - دفع خون در ادرار [ ماکرو هماچوری- قابل مشاهده با چشم غیر مسلح، میکرو هماچوری- تشخیص گلبول های قرمز در ادرار فقط با معاینه میکروسکوپی].
خونریزی داخلی
خونریزی داخلی- خونریزی در حفره های بسته بدن (به استثنای حفره صفاقی در زنان که بسته نیست).
انواع اصلی خونریزی داخلی زیر وجود دارد:
- هموتوراکس- خونریزی به داخل حفره پلور
- هموپریکاردیوم- خونریزی در حفره پریکارد
- هموپریتوئن- خونریزی به داخل حفره صفاقی
- هموسفالوس- خونریزی در بطن های مغز
- همارتروز- خونریزی داخل حفره مفصلی
خونریزی
خونریزی- خونریزی در بافت دو نوع خونریزی وجود دارد: (1) هماتوم و (2) ارتشاح هموراژیک. اگر خون ریخته شده بافت اطراف را از هم جدا کند و حفره تشکیل شده را پر کند، خونریزی نامیده می شود. هماتوم... اگر حفره تشکیل نشود و خون کم و بیش به طور مساوی در بافت نفوذ کند، در مورد آن صحبت می کنند انفیلتراسیون هموراژیک.
انواع اصلی ارتشاح هموراژیک (1) پتشی و (2) اکیموز است. پتهیا- خونریزی نقطهای در بافتهای پوششی (پوست، غشاهای مخاطی، سروز، پوششهای سینوویال، سطح داخلی بطنهای مغزی و غیره). مرسوم نیست که خونریزی های نقطه پتشی را در عمق اندام که در قسمت آن قابل مشاهده است نامیده شوند. اخیموس- خونریزی شدید در پوست اکیموز که تحت عمل مکانیکی ایجاد می شود و بنابراین، مرزهای آن با مرزهای سطح ضربه مطابقت دارد، نامیده می شود. ترشح (کبودی). خونریزی های متعدد در پوست، صرف نظر از اندازه آنها، به عنوان تعیین می شوند پورپورای هموراژیک(پورپورا هموراژیک).
ترومبوز
ترومبوز- انعقاد خون داخل حیاتی در مجرای رگ یا در حفره قلب. خون منعقده نامیده می شود ترومبوز... بر خلاف لخته شدن خون پس از مرگترومبوس دارای (1) سطح ناهموار است، (2) متراکم تر، (3) خشک است و (4) در بسیاری از موارد به دیوار چسبیده است. رول پس از مرگ از سطح صاف، نرم الاستیک، ژله مانند، مرطوب، براق است، به دیوار چسبیده نیست، بنابراین می توان آن را به راحتی از انتیما یا اندوکارد جدا کرد. ترومبوز یک فرآیند محافظتی و تطبیقی و نه تنها پاتولوژیک است؛ بنابراین، اشکال فیزیولوژیکی و پاتولوژیک ترومبوز مشخص می شود.
مکانیسم های ترومبوژنز
دو مکانیسم ترومبوژنز وجود دارد: (1) لخته شدن خون در امتداد مسیر بیرونی(در صورت آسیب به دیواره عروق یا اندوکارد) و (2) در امتداد مسیر درونی(بدون نقض یکپارچگی دیواره عروقی و بافت قلب).
مسیر خارجی انعقاد خون... رویداد کلیدی که مسیر خارجی ترومبوژنز را فعال می کند این است تخریب اندوتلیالو "قرار گرفتن" در نتیجه این لایه زیر اندوتلیال انتیما رگ که پلاکت ها به آن ثابت می شوند. در صورت آسیب به دیواره عروق با هر شدتی، تخریب سلول های اندوتلیال رخ می دهد، اما ترومبوز حتی در مواردی که سلول های اندوتلیال تنها ساختار آسیب دیده دیواره عروقی هستند، ایجاد می شود. نمونه بارز آسیب اندوتلیال جدا شده است سندرم آنتی فسفولیپید، که در آن سلول های اندوتلیال تحت تأثیر عوامل خودایمنی از بین می روند. مسیر خارجی فقط شامل یک عامل خاص انعقاد پلاسما است (فاکتور VII - قابل تبدیل) که هنگام تعامل با قطعات غشای سلول های تخریب شده فعال می شود (عامل III انعقاد پلاسما - ترومبوپلاستین بافتی) و به نوبه خود فاکتورهای X و V را فعال می کند (از این لحظه، انعقاد خون طبق یک مکانیسم بیوشیمیایی مشترک در مسیرهای خارجی و داخلی انجام می شود).
هنگامی که خون در امتداد مسیر خارجی لخته می شود، فرآیند (1) با فعال شدن پلاکت ها و تشکیل پلاکت ها آغاز می شود. ترومب پلاکتی، سپس (2) واکنش فاکتورهای انعقاد پلاسما و تشکیل وجود دارد ترومب فیبرین (انعقاد پلاسما، پس از آن (3) ترومبوس با گلبول های قرمز، لکوسیت ها و پروتئین های پلاسما اشباع می شود.
مسیر داخلی انعقاد خون... عوامل خاص مسیر داخلی ترومبوز عبارتند از XII (فعال کننده XI)، XI (فعال کننده IX)، IX و فاکتورهای هشتم (IX فعال فاکتور VIII را به خود متصل می کند و یک آنزیم را تشکیل می دهد. تنازو). این فرآیند با فعال شدن فاکتور XII (عامل هاگمن) در تماس با سطح آمبولی، از جمله میکروآمبولی ها، که می تواند تجمع عناصر تشکیل شده باشد، آغاز می شود. علاوه بر این، فرآیند طبق مکانیسم مشترک برای مسیرهای داخلی و خارجی پیش می رود. Tenase فاکتور X را فعال می کند، که به نوبه خود عامل V را فعال می کند و آن را به خود متصل می کند، در نتیجه یک کمپلکس آنزیمی واحد تشکیل می شود - پروترومبیناز... پروترومبیناز پروترومبین را به ترومبین (فاکتور II) تبدیل می کند که I (مونومر فیبرین از آن تشکیل می شود) و فاکتور XIII را فعال می کند. فاکتور فعال XIII (فاکتور تثبیت کننده فیبرین) مونومر فیبرین را به پلیمر فیبرین تبدیل می کند که ترومب فیبرین در واقع از آن تشکیل شده است.
عوامل موثر در ترومبوژنز... اختصاص دهید معمول هستندو محلیعوامل موثر در ترومبوژنز موارد کلی شامل (1) عدم تعادل بین سیستم های انعقادی و ضد انعقاد خون (به ویژه مهار فعالیت مکانیسم های ضد انعقاد) و (2) تغییر در ترکیب خون (به عنوان مثال، افزایش قابل توجه تعداد پلاکت ها). - ترومبوسیتوز). عوامل موضعی عبارتند از (1) اختلال در یکپارچگی دیواره عروقی یا اندوکارد (به عنوان مثال، تصلب شرایین، واسکولیت عفونی، اندوکاردیت)، (2) کاهش جریان خون (به عنوان مثال، تشکیل لخته های خونی احتقانی در رگ های واریسی) و ( 3) جریان خون نامناسب (به ویژه، گرداب).
مورفوژنز ترومبوز توسط مسیر خارجی
در آناتومی پاتولوژیک، مورفوژنز ترومبوز، که در امتداد مسیر خارجی ایجاد می شود، به طور دقیق مورد مطالعه قرار گرفته است. سه مرحله از فرآیند وجود دارد:
- واکنش پلاکتی(تحصیلات ترومب پلاکتی)
- انعقاد پلاسما(تحصیلات ترومب فیبرین)
- اشباع ترومبوس با گلبول های قرمز، لکوسیت ها و پروتئین های پلاسما(فرایند غیرفعال، به درجات مختلف بیان می شود).
واکنش پلاکتی و اختلالات آن
در طی واکنش پلاکتی، چهار فاز متمایز می شود:
- فعال سازیپلاکت ها
- چسبندگیپلاکت ها به ساب اندوتلیوم "برهنه" [که توسط مولکول های CD42 به دست می آید ( گلیکوکالیسین ها) روی سطح پلاکت و عامل فون ویلبراندپلاسمای خون]
- در حال گسترشصفحات روی ساب اندوتلیوم (با مشارکت پروتئین های CD61 و CD41 غشای پلاکتی رخ می دهد، زمانی که صفحه فعال می شود و یک مجتمع واحد را تشکیل می دهد)
- تجمعپلاکت ها با تشکیل ترومب پلاکتی (نقش اصلی را مواد دانه های صفحات و ADP ایفا می کنند).
اشکال ارثی متعددی از اختلالات در سیر واکنش پلاکتی مورد مطالعه قرار گرفته است که اصلی ترین آنها سندرم های زیر است:
I. اختلالات فعال شدن پلاکت(در درجه اول به اندازه صفحات بستگی دارد)
- ناهنجاری می-هاگلین(پلاکت های غول پیکر)
- سندرم Wiskott-Aldrich(بشقاب های بسیار کوچک).
II. اختلالات چسبندگی
- ترومبوسیتودیستروفی ماکروسیتی خونریزی دهنده برنارد سولیه(کمبود پروتئین CD42)
- بیماری فون فون ویلبراند(عدم وجود عامل فون ویلبراند).
III. اختلالات پخش پلاکتی
- ترومباستنی گلنزمن(کمبود پروتئین CD61 و CD41).
IV. اختلال در تجمع صفحات
- سندرم های فقدان گرانول- با آلبینیسم ( سندرم Hedgmansky-Pudlackو دیگران) و بدون آلبینیسم ( سندرم صفحه خاکستریو غیره.)
- ناهنجاری پیرسون-استوبا(یک واکنش غیر طبیعی صفحات به سطوح بالای ADP).
انعقاد پلاسما و اختلالات آن
در فرآیند انعقاد پلاسما ده پروتئین های خاص(عوامل I، II، V، VII، VIII، IX، X، XI، XII و XIII)، یون های کلسیم(فاکتور IV)، لازم برای فعال سازی پروتئین هایی است که سنتز آنها با مشارکت ویتامین K (II، V، VII، IX، X) و عامل فون ویلبراند، که حامل عامل هشتم است و بنابراین جزء تناسه است. فاکتور فون ویلبراند مختص آبشار انعقاد پلاسما نیست، زیرا در واکنش پلاکتی شرکت می کند. عامل سوم ( ترومبوپلاستین بافتیطبق سنت، به ضایعات غشای سلول های تخریب شده (مجموعه فسفولیپیدها و پروتئین های غشایی مختلف) گفته می شود.
مختلف وجود دارد ارثیو به دست آورداشکال اختلالات انعقادی پلاسما به انعقادهای ارثیشامل بیماری های زیر است:
1. آسیب شناسی فاکتور I (فیبرینوژن)
- هیپوفیبرینوژنمی- مقدار ناکافی فیبرینوژن (به طور معمول در بزرگسالان 2-4 گرم در لیتر)
- آفیبرینوژنمی- فقدان کامل فیبرینوژن (تظاهرات اصلی هیپو و آفیبرینوژنمی کمبازسازی است، نه تمایل به خونریزی)
- فیبرینوپاتی ها (دیس فیبرینوژنمی) - وجود فیبرینوژن غیر طبیعی (بسته به نوع فیبرینوژن غیرطبیعی که با سندرم هموراژیک و ترومبوفیلی آشکار می شود).
2. آسیب شناسی فاکتور II (پرترومبین) - هیپوپروترومبینمی(جنین به دلیل سندرم هموراژیک کشنده زنده نمی ماند). سایر اشکال انعقاد ارثی، به جز بیماری های هاگمن و لاکی لوران، نیز با سندرم هموراژیک آشکار می شوند.
3. آسیب شناسی فاکتور V (پراکسلرین، فاکتور اورن-کوئیک) - پاراهموفیلی (بیماری اورن-کوئیک).
4. آسیب شناسی فاکتور VII (پروکونورتین) - بیماری اسکندر.
5. آسیب شناسی فاکتور VIII (گلوبولین آنتی هموفیل A) - هموفیلی A.
6. آسیب شناسی عامل فون ویلبراند - بیماری فون ویلبراند.
7. آسیب شناسی فاکتور IX (گلوبولین آنتی هموفیل B، فاکتور کریسمس) - هموفیلی B (بیماری کریسمس).
8. آسیب شناسی فاکتور X (عامل استوارت-پرائر) - بیماری استوارت پروور.
9. آسیب شناسی فاکتور XI (گلوبولین C آنتی هموفیل، فاکتور روزنتال) - هموفیلی C (بیماری روزنتال).
10. آسیب شناسی عامل دوازدهم (عامل هاگمن) - بیماری هاگمنعمدتاً با ترومبوفیلی (نخستین بیمار با تشخیص قطعی بیماری D. Hageman در اثر آمبولی شدید ریه درگذشت)، گاهی اوقات سندرم هموراژیک آشکار می شود. در حالت دوم نامیده می شود هموفیلی D.
11. آسیب شناسی فاکتور سیزدهم (عامل تثبیت کننده فیبرین، فاکتور لاکی لوران) - بیماری لاکی لوران (سندرم نافی) با یک زخم ناف غیر التیام طولانی مدت در یک نوزاد مشخص می شود، یعنی. تظاهرات اصلی این بیماری کاهش باززایی است.
شایع ترین این بیماری ها هموفیلی A و B و همچنین بیماری فون ویلبراند است. تشخیص هموفیلی A و B فقط از طریق آزمایشگاهی امکان پذیر است: علائم بالینی و پاتولوژیک آنها مشابه است. در هموفیلی A و B، ایجاد (1) هماتوم بافت نرم، (2) همارتروز و (3) هماچوری معمول است.
طبقه بندی لخته های خون
لخته های خون به شرح زیر طبقه بندی می شوند:
I. حالت لومن رگ یا حفره قلب
- آهیانه (جداری) ترومبوز[لومن رگ را مسدود نمی کند]
- انسداد ترومبوز[لومن رگ را مسدود می کند
- ترومبوس کروی[ترومبوز غیر متصل واقع در حفره دهلیزی]
- ترومبوز گشاد شده[ترومبوز در آنوریسم عروق یا قلب].
II. اندازه ترومبوس
- ماکروترومب ها[قابل مشاهده با چشم غیر مسلح]
- ترومب های هیالین(لخته های خون در عروق میکروواسکولار) [با انعقاد داخل عروقی منتشر تشکیل می شوند که فقط در زیر میکروسکوپ قابل تشخیص است].
III. چسبیدن ترومبوز به دیواره رگ
- لخته های خون را ثابت کرد[زمانی که رگ یا اندوکارد آسیب دیده، به ساب اندوتلیوم یا بافتهای عمیقتر متصل میشود، تشکیل میشود]
- لخته های خون ثابت نشده است[به طور آزاد در مجرای رگ های خونی یا حفره های قلب قرار دارد].
لخته های خون ثابت نشده:
- ماکروتومبوس در ورید اجوف[می تواند منجر به آمبولی ریه شود]
- میکروترومبی(لخته شدن خون هیالین).
IV. اصل اتیولوژیک
- لخته شدن خون در صورت آسیب عروقی (ترومبوز فیزیولوژیکی)
- لخته شدن خون با ترومبوفیلی ارثی
- لخته شدن خون همراه با اگزیکوز [به عنوان مثال، لخته شدن خونهمراه با غلیظ شدن خون در هنگام خستگی]
- لخته های خون مرتبط با آمبولی [به عنوان مثال، تومورو لخته های سپتیکدر اطراف یک تومور یا آمبولی میکروبی تشکیل می شوند].
V. رنگ ترومبوز
- لخته خون قرمز[لخته شدن خون با تعداد زیادی گلبول قرمز]
- لخته خون سفید[لخته شدن خون با مقدار کمی گلبول قرمز]
- مختلط (لمینت) ترومبوز[ترومبوز با نواحی متناوب سفید و قرمز].
در ساختار یک ماکروترومب ثابت پیشرونده، (1) سر، (2) بدن و (3) دم متمایز می شوند. این بخشی از دم است که اغلب به ترومبوآمبولی ("گلوله") تبدیل می شود.
سندرم DIC
سندرم انعقاد داخل عروقی منتشر (سندرم DIC) با ظاهر شدن تعداد زیادی ترومبوز هیالین در اندام های مختلف با ایجاد خونریزی بعدی مشخص می شود. سندرم ترومبوهموراژیک). تظاهرات هموراژیک به این دلیل است که فاکتورهای انعقادی پلاسما در تشکیل لخته خون صرف می شود. انعقاد مصرف). علت DIC افزایش شدید محتوای ترومبوپلاستین در جریان خون (قطعات غشای سلول های تخریب شده) با منشاء مختلف است که در سپسیس، لوسمی، همولیز داخل عروقی، از دست دادن خون گسترده یا پیشرونده، نیش مار، مایع آمنیوتیک مشاهده می شود. آمبولی، شوک و غیره
پیامدهای ترومبوز
بین پیامدهای مطلوب و نامطلوب ترومبوز تمایز قائل شوید.
I. نتایج مطلوب
- اتولیز (لیز آسپتیک) ترومبوز[ذوب شدن کامل یک لخته خون توسط آنزیم های سیستم ضد انعقاد خودش]
- سازمان لخته خون[جایگزینی آن با بافت همبند فیبری ( فیبروز) با ظهور بعدی عروق در آن ( اندوتلیال شدن ترومبوز) و از سرگیری جریان خون از طریق آنها ( عروق ترومبوز)].
II. نتایج نامطلوب
- ترومبوآمبولی[تبدیل لخته خون یا بخشی از آن به ترومبوآمبولی]
- لیز سپتیک[ذوب شدن لخته خون توسط آنزیم های میکروارگانیسم هایی که وارد لخته خون شده و در آن تکثیر می شوند. ممکن است منجر به خونریزی مجدد و سپسیس شود].
آمبولی
آمبولی- وجود ذراتی در جریان خون که به طور معمول یافت نمی شوند. چنین ذرات نامیده می شود آمبولی... معنای اصلی آمبولی ایجاد یک حمله قلبی از جمله ریزانفارکتوس های متعدد و همچنین سایر عوارض شدید است.
طبقه بندی
آمبولی عمدتاً بر اساس جهت حرکت آمبولی و ترکیب آمبولی طبقه بندی می شود.
I. جهت حرکت آمبولی
- آمبولی ارتوگراد[حرکت آمبولی در طول جریان خون]
- آمبولی متناقض[حرکت آمبولی از وریدهای دایره بزرگ به شریان های دایره بزرگ، دور زدن ریه ها]
- آمبولی رتروگراد[حرکت آمبولی در برابر جریان خون].
آمبولی ارتوگراد به (1) طبقه بندی می شود. شریانی(آمبولی از قلب چپ و آئورت به شریانهای اندامها حرکت میکند)، (2) ریوی(از رگهای دایره بزرگ و قلب راست تا ریه ها) و (3) آمبولی عروق پورتال(از شاخه های ورید باب تا کبد). آمبولی متناقض شامل (1) ترانس قلبی(حرکت آمبولی از طریق نقص در سپتوم قلب) و (2) ترانس آناستوموز(حرکت آمبولی از طریق آناستوموزهای شریانی وریدی و شریانی وریدی) آمبولی.
II. ماهیت آمبولی
- ترومبوآمبولی
- متاستاز
- آمبولی چربی
- آمبولی هوا
- نیتروژن (« گاز») آمبولی[آمبولی حباب نیتروژن در بیماری رفع فشار]
- آمبولی بافتی
- آمبولی جسم خارجی.
ترومبوآمبولی
شایع ترین نوع آمبولی است ترومبوآمبولی، که در آن آمبولی قطعه ای از ترومبوس است، در درجه اول بخشی از دم یک ترومبوز مخلوط ("گلوله"). به شرح زیر طبقه بندی می شود:
I. ترومبوآمبولی عروق دایره بزرگ.
II. ترومبوآمبولی عروق دایره کوچک
- آمبولی شدید ریه[کشنده پایان می یابد؛ نقش اصلی در تاتوژنز توسط رفلکس ریوی کرونری ایفا می شود]
- ترومبوآمبولی شاخه های شریان های ریوی[منتهی به انفارکتوس هموراژیک ریهو پنومونی حمله قلبی].
متاستاز
متاستازهاآمبولی نامیده می شود که در محل تثبیت باعث آسیب به دیواره عروقی می شود.
آمبولی چربی
آمبولی چربی- آمبولی با قطره چربی. خطرناک ترین آمبولی چربی ناشی از آسیب دیافیز استخوان های لوله ای است، زیرا قطرات چربی از مغز استخوان چربی به راحتی به جریان خون نفوذ می کند (مویرگ های سینوسی مغز استخوان دارای یک مجرای عریض و دیواره سوراخ دار هستند). در این صورت آسیب شدیدی به ریه ها و مغز ایجاد می شود. آمبولی های چربی زمانی شناسایی می شوند که بخش های بافتی با سودان III یا آنالوگ های آن رنگ آمیزی شوند.
آمبولی هوا
آمبولی هوا- آمبولی حباب هوا این اغلب زمانی اتفاق میافتد که رگهای گردن آسیب میبینند، زمانی که هوا در حین دم وارد لومن آنها میشود. موارد شناخته شده ای از ورود هوا به وریدهای رحم در دوره پس از زایمان وجود دارد. با آمبولی هوا، مرگ ناگهانی... آزمایش آمبولی هوا در طی کالبد شکافی شامل پر کردن حفره پریکارد با آب و سپس تشریح دیواره قلب راست در زیر آب است. در همان زمان، حباب های هوا ظاهر می شوند.
آمبولی بافتی
آمبولی بافتیمی تواند با آسیب های مختلف (به عنوان مثال، در یک نوزاد پس از آسیب تولد)، با فرآیندهای مخرب ( آمبولی با توده های آتروماتوزبا زخم پلاک آترواسکلروتیک، آمبولی با قطعات دریچه قلب تخریب شده با اندوکاردیت سپتیک). تعدادی از نویسندگان نیز به آمبولی بافتی اشاره می کنند آمبولی سلولیکه به آمبولی سلولی توموری و غیر توموری تقسیم می شود. آمبولی سلولی غیر توموری، به ویژه، زمینه ساز اندومتریوز- بیماری که در آن ظاهر بافت آندومتر در خارج از پوشش رحم رخ می دهد (به عنوان مثال، در میوکارد یا مغز).
آمبولی مایع آمنیوتیک
یک عارضه وحشتناک زایمان است آمبولی مایع آمنیوتیک (آمبولی مایع آمنیوتیک) که توصیه می شود به عنوان یک نوع مستقل از آمبولی در نظر گرفته شود، زیرا مایع آمنیوتیک بافت نیست
شوکه شدن
شوکه شدن- نارسایی حاد عروقی با ایجاد انسداد میکروسیرکولاسیون. زیر انسداد میکروسیرکولاسیونکاهش یا توقف قابل توجه جریان خون در عروق میکروواسکولار را درک کنید. در همان زمان، متابولیسم بافت در اندام های آسیب دیده به شدت مختل می شود. در معاینه میکروسکوپی، رگهای ریز یا «خالی» با لومن فرو ریخته، یا بهطور فلجی گشاد شده و پر خون با ادم بافت اطراف عروقی یافت میشوند. کانون های کوچک نکروز اغلب در اطراف رگ های میکروواسکولار یافت می شوند.
طبقه بندی
شوک بسته به علتی که باعث آن شده است طبقه بندی می شود. عاملی که منجر به ایجاد محاصره میکروسیرکولاسیون شد (تکانه های دردناک شدید، اندوتوکسین میکروارگانیسم ها، کاهش شدید حجم خون در گردش و غیره).
انواع اصلی شوک شامل موارد زیر است:
- هیپوولمیک (پس از خونریزی) شوکه شدن[با از دست دادن خون شدید حاد]
- شوک قلبی[با نارسایی حاد قلبی]
- شوک آنافیلاکتیک[شوک ناشی از واکنش آلرژیک]
- سپتیک (سمی عفونی, اندوتوکسین) شوکه شدن[شوک ایجاد شده تحت تأثیر اندوتوکسین میکروارگانیسم]
- شوک خونی[در مرحله انعقاد انعقاد داخل عروقی منتشر]
- شوک انتقال خون[در صورت تزریق خون ناسازگار]
- پس از سانحه (دردناک) شوکه شدن[شکل کلاسیک شوک، که تصویر بالینی آن در پزشکی داخلی توسط نیکولای ایوانوویچ پیروگوف به تفصیل شرح داده شده است].
پاتوژنز شوک
در شوک، جریان خون عمدتاً در عروق بزرگ حفظ می شود. متمرکز شدن گردش خون). از رگ های شریانی، خون وارد رگ های وریدی می شود و ریز عروق مسدود شده را دور می زند. بای پس خون). بخشی از خون باقی مانده در ریزرگ ها از گردش خون حذف می شود. توقیف جریان خون). در نتیجه مسدود شدن میکروسیرکولاسیون، هیپوپرفیوژن بافتی (شکست پرفیوژن) منجر به توسعه می شود سندرم نارسایی چند عضوی.
اختلالات گردش خون در کل ارگانیسم بر اساس تغییرات عملکردی در همه اندام ها و سیستم ها و بالاتر از همه، البته تغییرات در قلب است.
اختلالات گردش خون به 6 نوع اصلی طبقه بندی می شوند:
- پرخونی یا پرخونی
- خونریزی یا خونریزی
- ترومبوز
- آمبولی
- ایسکمی یا کم خونی موضعی
- حمله قلبی
هایپرمی: پرخونی شریانی چندان مهم نیست. پرخونی وریدی با افزایش پر شدن خون بافت بیان می شود، خروج خون دشوار است، در حالی که جریان شریانی تغییر نمی کند یا کمی کاهش می یابد. پرخونی وریدی موضعی و عمومی است، اما پرخونی وریدی عمومی بسیار شایع تر است و برای تمرین اهمیت بیشتری دارد.
خصوصیات میکروسکوپی: روی بافت یک انسان زنده کاهش جزئی دما (1-0.5 درجه)، کمی انبساط سیاهرگ ها و مویرگ ها دیده می شود و رنگ مایل به آبی روی پوست ظاهر می شود (به آن سیانوز می گویند). با یک استاز وریدی که به سرعت در حال ظهور است، ادم بافتی ایجاد می شود و در همه بافت ها ایجاد نمی شود، بلکه در حفره ها و در اندام هایی که فضایی برای قرار دادن مایع وجود دارد ایجاد می شود. به عنوان مثال در کلیه ها و کبد که فضاهای خاصی به جز برخی ترک ها وجود دارد، تنها با میکروسکوپ ادمی قابل مشاهده نیست. در عین حال، ادم ریوی، در جایی که فضای زیادی وجود دارد، از نظر ماکروسکوپی قابل توجه است.
ترانسودات (مایع ادماتوز) - در هنگام استاز وریدی، معمولاً شفاف رخ می دهد و بافت هایی که شسته می شوند رنگ طبیعی خود را حفظ می کنند.
اگزودا مایعی با منشاء پلاسمایی است، در هنگام التهاب ایجاد می شود، به رنگ کدر، زرد متمایل به خاکستری یا قرمز است، بافت هایی که توسط اگزودا شسته می شوند رنگی کدر دارند.
با پرخونی که به آرامی در حال ظهور است، بافت دچار سفت شدن قهوه ای می شود. واقعیت این است که در رکود مزمن که بستر وریدی مملو از خون است به مرور زمان نفوذپذیری دیواره ها در آن افزایش می یابد و مقدار مشخصی مایع و کوچکترین سلول های خونی در بافت اطراف آزاد می شود. در بافت ها، رنگدانه های مختلفی از گلبول های قرمز آزاد می شود: هموگلوبین، هموسیدرین. دومی از طریق یک واکنش بیوشیمیایی پیچیده توده های قهوه ای را در بافت ایجاد می کند که توسط ماکروفاژها جذب می شود.
القاء در شرایط هیپوکسی مزمن استقامت است. واقعیت این است که هر بافت بدن، یک بار در شرایط گرسنگی اکسیژن، به دلیل بافت همبند (که اصلی ترین آن است - استرومای همه اندام ها) شروع به رشد استرومای خود می کند. بزرگ شدن استروما یک واکنش تطبیقی است، زیرا مویرگ ها همراه با استروما به داخل بافت رشد می کنند که هیپوکسی را جبران می کند. در عمل، به عنوان یک قاعده، این اتفاق نمی افتد، اما اسکلروز رخ می دهد - جوانه زدن بافت همبند یا سفتی. در نهایت خود سیاهرگ ها با استاز وریدی منبسط و سفت می شوند.
تصویر میکروسکوپی:- وریدهای گشاد شده و پر از خون. ونولا به راحتی از شریان متمایز می شود - شریان دیواره ضخیم تری دارد (به دلیل برجسته تر بودن لایه ماهیچه صاف - رسانه). اگر احتقان وریدی حاد وجود داشته باشد، می توانید یک مایع ادماتیک را مشاهده کنید (عملاً حاوی پروتئین نیست، برخلاف اگزودا که حاوی بیش از 1٪ پروتئین است) که به دلیل عناصر تشکیل شده خون کدر است. درصد کمی از پروتئین در ترانسودات شرایطی را برای رنگآمیزی صورتی کمرنگ مایع در آلوئولها با ائوزین ایجاد میکند. همچنین بافت همبند به خوبی توسعه یافته در آلوئول ها قابل توجه خواهد بود. در بافت ریه با سپتوم آلوئولی، که به طور معمول دارای "خصلت توری" است، با آسیب شناسی: فضاهای بین آلوئول ها با بافت همبند پر می شود که تا حدودی رگ های خونی را فشار می دهد. علاوه بر این، بلافاصله یک رنگدانه قهوه ای - هموسیدرین را خواهید دید که بخشی از آن در ماکروفاژها یافت می شود. ماکروفاژها در بسیاری از اندام های داخلی نقش "سرایدارهای وظیفه" را بازی می کنند: اینها سلول هایی هستند که از هموستاز ایمنی - تعادل محافظت می کنند. آنها هر ماده خارجی را برمی دارند، فاگوسیتوز می کنند، سعی می کنند آن را از بین ببرند. همین اتفاق در مورد هموسیدرین می افتد، وقتی ماکروفاژها آن را جذب می کنند، هموسیدروفاژ نامیده می شوند.
احتقان وریدی موضعی: معمولاً با انسداد یا بستن هر سیاهرگ اصلی همراه است.
پرخونی وریدی عمومی - 3 نوع اصلی وجود دارد - رکود گردش خون ریوی و رکود گردش خون سیستمیک، رکود ورید باب.
دلایل رکود در یک دایره کوچک:
· نارسایی بطن چپ. تصور کنید که بطن چپ، به دلیل نوعی آسیب به عضلاتش، مثلاً حمله قلبی، زخم گلوله، اسکلروز عروق کرونر، شروع به پمپاژ کل حجم خون نمی کند. تا حدی خون در آن باقی می ماند، به این معنی که رکود در دایره ریوی مشاهده می شود.
· نقص میترال می تواند به شکل تنگی باشد که در آن تمام حجم خون نمی تواند در هر واحد زمانی که برای دیاستول آزاد می شود از دهلیز به بطن وارد شود. این بدان معناست که مقداری حجم خون ذخیره شده در دهلیز باقی می ماند، به این معنی که فشار در وریدهای گردش خون ریوی افزایش می یابد. در صورت نارسایی دریچه میترال (بستن نشتی لت های دریچه) که با روماتیسم، اسکلروز رخ می دهد. در این حالت، در طی سیستول، خون به دهلیزها برمی گردد و در آنجا به تدریج تجمع می یابد.
· نقص آئورت: باریک شدن یا نارسایی دریچه های آئورت نیمه قمری به دلیل سخت شدن آنها. با هر دو، خون ابتدا در بطن نگه داشته می شود (که می تواند این وضعیت را برای مدتی با افزایش نیروی انقباض جبران کند) و سپس خون در دهلیزها شروع به تجمع می کند.
فشرده شدن وریدهای مدیاستن توسط تومور نادرترین علت است.
دینامیک تغییر
در احتقان وریدی حاد یک دایره کوچک (از چند دقیقه تا چند ساعت ایجاد می شود)، ادم ریوی رخ می دهد.
ماکروسکوپی: ریه ها فرو نمی ریزند، هنگامی که با انگشت فشار داده می شوند، حفره های صاف نشده باقی می مانند، مقدار زیادی از ترانسودات و خون وریدی تیره روی برش جریان می یابد.
بطور میکروسکوپیک: ضخیم شدن سپتوم آلوئولی، رنگدانه قهوه ای که تا حدی آزاد در سپتوم ها تا حدی در ماکروفاژها، سیاهرگ های گشاد شده با خون قرار دارد.
علت مرگ: نارسایی قلبی و ریوی.
مجسمه تیراژ بزرگ:
احتقان وریدی یک دایره کوچک از قبل موجود است. بطن راست خون را از طریق ریه ها هدایت می کند. اگر شبکه وریدی ریه ها با خون وریدی مسدود شده باشد و شریان کم و بیش آزاد باشد، بطن راست نمی تواند خون را از طریق شبکه وریدی عبور دهد؛ در ابتدا نیروی انقباضات و هیپرتروفی را افزایش می دهد. . قلب هیپرتروفی شده ناشی از بطن راست کور ریوی نامیده می شود. ضخامت دیواره بطن راست به جای 1-2 میلی متر به طور معمول به 5-10 میلی متر می رسد، یعنی از نظر ماکروسکوپی حتی می توان بطن چپ را از راست با ضخامت دیواره تشخیص داد. برای مدتی، افزایش ضخامت دیواره ماهیت جبرانی دارد، اما پس از آن به ناچار منجر به جبران خسارت می شود، همراه با اتساع - انبساط، که در آن رکود گردش خون سیستمیک ایجاد می شود.
· تغییرات اسکلروتیک منتشر در ریه ها. با ذات الریه مزمن طولانی مدت، پنوموسکلروز ممکن است رخ دهد. همچنین در مورد گردگیری حرفه ای (پنوموکونیوز)، به عنوان مثال، در بین معدنچیان، کارگران صنعت سیمان نیز اتفاق می افتد. سپتوهای بین آلوئولار تقریباً در هر آلوئول ضخیم شده است، بافت همبند ایجاد می شود که اندکی وریدهای ریوی را فشار می دهد. این برای مسدود کردن جریان خون کافی است.
· یک علت نادر - نارسایی بطن راست زیرا حملات قلبی در بطن راست بسیار نادر است.
· فشرده سازی تنه ورید توخالی توسط تومور.
دینامیک تغییر
با رکود به سرعت در حال توسعه، ادم ایجاد می شود - با پرخونی دایره بزرگ - ادم پوست و بافت های نرم، که آناسارکا نامیده می شود. اندام ها معمولاً بزرگ می شوند ، خطوط کلی بافت ها تغییر می کند ، هنگام فشار دادن ، حفره هایی باقی می مانند که صاف نمی شوند ، یک الگوی وریدی قابل مشاهده است.
فرم های OTHEK:
ادم حفره شکم آسیت، ادم حفره پلور - هیدروتوراکس، ادم حفره پریکارد - هیدروپریکارد و غیره نامیده می شود. سیانوز با وریدهای واریسی همراه است، هر چه بافت از قلب دورتر باشد، مشخص تر است
"کبد جوز هندی" - از نظر بالینی با بزرگ شدن کبد آشکار می شود: لبه پایینی از زیر قوس دنده ای توسط چندین انگشت گسترش می یابد، در لمس دردناک می شود و گرد می شود. کبد بسیار بزرگتر از حد طبیعی است (به طور معمول 28 سانتی متر اندازه پیشانی، 16 اندازه ساژیتال لوب بزرگ، 12 اندازه کوچک، 8 سانتی متر اندازه عمودی است). برش یک الگوی جوز هندی مشخص را نشان می دهد.
بطور میکروسکوپیک: این در این واقعیت بیان می شود که در لوبول های کبدی همه وریدهای مرکزی گشاد شده و پر از خون هستند ، تمام مویرگ هایی که به آنها می ریزند نیز با خون مسدود می شوند و چربی در قسمت های محیطی لوبول ها به دلیل اختلالات متابولیک ظاهر می شود.
علت مرگ نارسایی قلبی است.
SSTAGER IN THE GATE VIN SYSTEM
علل آن فقط با کبد مرتبط است - تغییرات اسکلروتیک منتشر - سیروز، کمتر مواقع سفتی راکد منجر به این واقعیت می شود که مویرگ ها در لوبول های کبدی توسط بافت همبند فشرده می شوند. فشار خون پورتال شامل تعدادی تظاهرات بالینی است:
· وریدهای واریسی خارج از آناستوموزهای پورتوکاوال کبدی (وریدهای معده و مری، سیاهرگهای راست روده، سیاهرگهای دیواره قدامی شکم).
· بزرگ شدن راکد طحال - طحال و به دنبال آن سفتی.
ترومبوز
این فرآیند انعقاد خون in vivo به مجرای یک رگ یا در حفرههای قلب است. به عبارت دیگر، دناتوره شدن غیرقابل برگشت پروتئین ها و سلول های خونی است.
· تغییرات دیواره عروقی در هنگام التهاب، تصلب شرایین، آنژیوادم، فشار خون بالا (به جای انقباض-اتساع صحیح، رگ وریدی باریک می شود و شکل خود را به صورت اسپاسم برای مدت طولانی حفظ می کند).
· تغییر در سرعت و جهت جریان خون. این تغییرات اغلب موضعی و عمومی هستند و با نارسایی قلبی همراه هستند. لخته های خونی که با ضعف شدید انقباضی و با افزایش نارسایی قلبی ظاهر می شوند، معمولاً مارانث (راکد) نامیده می شوند. آنها می توانند در وریدهای محیطی ایجاد شوند.
· تعدادی از دلایل مرتبط با تغییر در ترکیب شیمیایی خون: با افزایش پروتئین های درشت، فیبرینوژن، لیپیدها. چنین شرایطی در تومورهای بدخیم، آترواسکلروز یافت می شود.
مکانیسم تشکیل ترومبوز شامل 4 مرحله است:
1. فاز آگلوتیناسیون پلاکتی
2. انعقاد فیبرینوژن، تشکیل فیبرین
3. آگلوتیناسیون گلبول های قرمز
4. بارش - رسوب بر روی یک لخته از تمام پروتئین های اصلی پلاسما.
از نظر ماکروسکوپی: اول از همه، تشخیص ترومبوز از لخته پس از مرگ ضروری است: ترومبوز ارتباط نزدیکی با دیواره رگ خونی دارد و لخته آزادانه قرار دارد. ترومبوس دارای سطحی کسل کننده و گاهی حتی زبر است، در حالی که لخته دارای سطحی صاف، براق و "آینه مانند" است. ترومبوز قوام شکننده ای دارد، در حالی که قوام لخته شبیه ژله است.
بسته به مکان و شرایط تشکیل لخته خون، موارد زیر وجود دارد:
1. سفید (پلاکت، فیبرین، لکوسیت). این لخته های خون زمانی تشکیل می شوند که جریان خون سریع در رگ ها وجود داشته باشد.
2. قرمز (پلاکت ها، فیبرین، گلبول های قرمز) در شرایط جریان خون آهسته، بیشتر در رگ ها تشکیل می شود.
3. مختلط: محل اتصال سر نامیده می شود، بدن آزادانه در مجرای رگ قرار دارد. سر معمولاً بر اساس اصل لخته خون سفید ساخته می شود، مناطق سفید و قرمز به طور متناوب در بدن قرار می گیرند و دم معمولاً قرمز است.
4. ترومب های هیالین - نادرترین نوع (آنها از گلبول های قرمز تخریب شده، پلاکت ها، رسوب پروتئین تشکیل شده اند). این رسوب پروتئین است که شباهت به غضروف را ایجاد می کند. این لخته های خون در شریان ها و ونول ها یافت می شوند.
در رابطه با لومن رگ، ترومبوس ها متمایز می شوند:
1. مسدود کردن (انسداد) به این معنی که مجرای رگ توسط جرم یک ترومبوس بسته می شود.
2. آهیانه
3. در حفره های قلب و در آنوریسم ها ترومب های کروی شکل وجود دارد
از نظر میکروسکوپی: لخته های خون قرمز نکروز غنی از پروتئین هستند که با ائوزین به رنگ قرمز رنگ آمیزی شده اند. در توده های نکروزه، می توان عناصر و ریزه ها - بقایای سلول ها را تشکیل داد.
متداول ترین آنها سازماندهی است، یعنی جوانه زدن توسط بافت همبند
سنگ سازی - رسوب آهک
نرم شدن ثانویه (تقابل) ترومبوز به دو دلیل رخ می دهد: زمانی که یک میکروب وارد ترومبوس می شود (آنزیمولیز میکروبی)، و آنزیمولیز موضعی به دلیل آنزیم های خود که در هنگام آسیب آزاد می شوند.
آمبولیزم
این انتقال ذرات توسط جریان خون است که معمولاً در آن وجود ندارد. سه جهت اصلی حرکت آمبولی در گردش خون وجود دارد:
از قلب چپ تا سیستم شریانی
از وریدهای دایره بزرگ از طریق قلب راست به تنه ریوی
توسط ورید باب
7 نوع آمبولی وجود دارد:
1. ترومبوآمبولی: یکی از دلایل جدا شدن ترومبوز نرم شدن آن است، اما می تواند خود به خود از محل چسبندگی جدا شود. مثال بالینی: پسر 14 ساله مبتلا به روماتیسم پس از بازی فوتبال در اثر مرگ ناگهانی فوت کرد. معلوم شد که او لخته خون روی لتک دریچه میترال اسکلروز شده دارد. در زمان تلاش بدنی شرایط برای جدا شدن لخته خون ایجاد شد، او یکی از شریان های مغزی را مسدود کرد که در نتیجه مرگ اتفاق افتاد.
2. آمبولی بافتی یا سلولی. در تومورهای بدخیم، زمانی که سلولهای سرطانی یا سارکوم وارد جریان خون میشوند، از تومور جدا میشوند و همراه با جریان خون به گردش در میآیند و در شاخههای دوردست اندامهای داخلی گیر میکنند و باعث آمبولی تومور میشوند. این ندولهای تومور دور در ارتباط با تومور مادری متاستاز نامیده میشوند و خود فرآیند متاستاز نامیده میشود. در سرطان معده، متاستاز از طریق سیاهرگ باب به کبد می رود.
3. آمبولی میکروبی - با التهاب چرکی رخ می دهد. چرک بافت های اطراف را با آنزیم های خود ذوب می کند، از جمله رگ های خونی و میکروب ها این توانایی را دارند که از طریق رگ ذوب شده به داخل خون نفوذ کرده و بیشتر در بدن گردش کنند. هرچه آبسه بزرگتر باشد، احتمال ورود میکروب ها به جریان خون بیشتر می شود. وضعیتی که در این حالت ایجاد می شود سپسیس نامیده می شود.
4. آمبولی چربی در شکستگی های بزرگ استخوان های لوله ای با رقیق شدن رخ می دهد. قطرات چربی (از مغز استخوان) که وارد سیاهرگ ها می شود، مویرگ های ریه ها را از بین می برد.
5. آمبولی هوا. زمانی اتفاق می افتد که رگ های بزرگ زخمی شوند. برای یک حیوان آزمایشگاهی، به ویژه برای خوکچه هندی، 5 مکعب هوا که از طریق سرنگ تزریق می شود برای ایجاد آمبولی هوا کافی است.
6. آمبولی گازی. با بیماری کیسون رخ می دهد: با افزایش شدید غواصان، ترکیب گاز خون تغییر می کند، حباب های نیتروژن خود به خود در آن ظاهر می شود (در فشار بالا - در حین غواصی - نیتروژن به میزان بیشتری در خون حل می شود و در طول صعود. وقت ترک خون را ندارد).
7. آمبولی توسط اجسام خارجی: حرکت گلوله ها و قطعات در برابر جریان خون تحت تأثیر نیروی جاذبه (عقب نشین) یا از طریق جریان خون.
INFARKT
این نکروز ناشی از قطع خون رسانی به بافت است. با رنگ متمایز کنید - سفید، قرمز و سفید با لبه قرمز.
در شکل، که با نوع گردش خون مرتبط است: نامنظم و مخروطی (در کلیه ها، ریه ها). بر اساس قوام: خشک و مرطوب.
مراحل توسعه انفارکتوس میوکارد:
1. مرحله ایسکمیک بیان ماکروسکوپی ندارد و تنها چند ساعت (تا 8-10 ساعت) طول می کشد. از نظر میکروسکوپی: ناپدید شدن گلیکوژن و آنزیم های ضروری در سلول ها.
2. مرحله نکروز - انفارکتوس ماکرو و میکروسکوپی بیان مربوطه دارد. مدت زمان مرحله تا یک روز می باشد.
3. مرحله نتیجه، اغلب سازمان. یک حفره در مغز تشکیل می شود - یک کیست، در قلب و سایر اندام ها سازماندهی و ظاهر یک اسکار است. این یک هفته یا بیشتر طول می کشد.