脂肪肝治療。 非アルコール性脂肪性肝疾患小児におけるNSAIDとの鑑別診断が必要な疾患と状態
非アルコール性脂肪性肝疾患(NAFLD)、または脂肪症、脂肪肝症、脂肪肝症は、中性脂肪が肝細胞に蓄積し、それらを破壊する疾患です。 危険因子 - 太りすぎ 2型糖尿病を背景としたインスリン抵抗性。 ただし、NAFLDは痩せた人にも影響を与えることがよくあります。 この病気は、時間内に医師の診察を受けずに開始すると、合併症を引き起こす可能性があります 効果的な治療.
すべて表示する
原因
非アルコール性脂肪性肝疾患(NAFLD)は、臓器の細胞が機能を破壊する中性脂肪で満たされている病状です。 その後、脂質の過剰により肝細胞が破裂し、その代わりに最初に線維症が形成され、次に肝硬変が形成されます。 機能的に活性な組織が減少し、代謝に関連する他の障害が現れます。 肝疾患の分類では、この病理は別の場所に与えられます。
脂質浸潤の発生の主な理由:
- インスリン抵抗性の代謝障害-肥満を伴うメタボリックシンドローム。
- 慢性疾患 消化管.
- 重金属、農薬、その他の毒物による中毒。
- 薬の服用-経口避妊薬、糖質コルチコイド、抗生物質、ニコチン酸、スタチン。
- いいえ 適切な栄養、劇的な体重減少または体重増加。
- ウイルス性肝炎。

脂肪肝肝症-原因、症状、治療、 フォークレシピとダイエット
処理
脂肪性肝硬変は、治療が時間通りに処方されない場合、肝硬変につながる可能性のある深刻な病気です。 良いニュースもあります-病気はの助けを借りて正常に修正されています バランスの取れた栄養、肝保護剤、民間療法を服用するだけでなく。
脂質ジストロフィーの治療における重要な役割は、代謝と消化のプロセスの正常化によって果たされます。

肝保護剤
異なる作用機序を持つ多くの肝保護剤があります。
肝臓の脂肪変性では、肝細胞からの中性脂肪を利用する脂肪親和性化合物が使用されます。 彼らのために 化学組成メチル基の存在が特徴的です。

脂肪症の段階の病変の治療のための主な薬:
- ヘプトラル。
- 必須脂質(Rezalut、Essentiale forte、Essliver、Phosphogliv)。
- オオアザミ抽出物(Silimar、Karsil、Gepabene)。
- ビタミン-葉酸、メチルコバラミン、ビタミンU。
- ウルソおよびケノデオキシコール酸製剤(ヘノファルク、ウルソファルク、ウルソリフ、リボデキサ、ウルドクサ)。

脂肪肝浸潤-主な兆候、診断および治療
ヘプトラル
これは、S-アデノシルメチオニンと呼ばれる脂肪親和性化合物です。 それは体内に存在して合成され、不安定なメチル基のドナーとして新しい細胞を生成するために必要です。 さまざまな神経伝達物質やその他の重要な物質の合成に参加しています。 したがって、脂肪肝症では、無気力、うつ病、無気力、関節の問題などの症状を緩和します。
S-アデノシルメチオニンは、肝細胞からの中性脂肪の利用を促進し、脂質代謝を正常化します。 脂肪浸潤のプロセスを逆転させ、線維症と肝硬変の変化を防ぎます。 レンダリング ポジティブアクション解毒機能について。 グリコーゲンの形でブドウ糖の貯蔵を改善します-いつ 糖尿病肝細胞を維持することにより、血中のレベルを低下させます。
錠剤および注射液の形で入手できます。 静脈内および筋肉内注射では、Heptralという薬のバイオアベイラビリティは95%ですが、消化管に吸収されるのはわずか5%です。
必須のリン脂質
化学名はリン脂質であり、いくつかのクラスの化合物が含まれています-ホスホチジルコリン(レシチン)、ホスホチジルイノシトール、ホスホチジルセリン。
これらの薬は、細胞に蓄積された脂質の利用を促進し、肝臓の脂肪変性を引き起こす脂肪親和性化合物です。 それらの組成にメチル基を持って、それらは器官の再生、解毒のプロセスに貢献します。
必須脂質は、乳化剤である脂肪の吸収を改善し、消化プロセスを正常化し、胆汁分泌促進効果をもたらします。 肝臓組織の脂肪変性により、胃腸管が苦しみ、胆石を形成する傾向が高まります。 レシチンは胆汁中のコレステロール値を下げるのに役立ち、粘度を下げます。
ホスホチジルイノシトールは、メタボリックシンドローム(2型糖尿病)で重要なインスリンの作用に対する細胞受容体の感受性を高めます。
Phosphoglivには、脂肪性肝炎におけるウイルスの増殖を防ぐグリチルリチン酸が含まれています。
オオアザミ
その抽出物が肝保護効果を持っている植物。 胆汁分泌促進効果があります。 それは抗酸化物質です-それは中毒のために起こる肝臓のグルタチオンの枯渇に必要です。

胆汁の流れを刺激するため、脂溶性ビタミンの消化と同化を改善します。 肝臓でのタンパク質合成を正常化し、浮腫を防ぎます。 メタボリックシンドロームで重要な過剰な血糖値からのグリコーゲンの形成を促進します。
それは脂肪変性のための追加の治療法として使用されます。 それは、女性の脂肪症を伴うことが多い多嚢胞性卵巣疾患の代謝にプラスの効果をもたらします。
Silimar、Karsil、Legalonにはオオアザミ抽出物が含まれており、Gepabeneには煙抽出物も含まれています。
ビタミン
それらの中には、脂肪親和性化合物もあります。 消化器疾患における脂肪性肝障害は、メチルコバラミン(B12)や葉酸などの重要な補因子の欠乏によって引き起こされます。 それらがないと、肝細胞の回復が遅く、肝細胞の中性脂肪が集中的に沈着します。
萎縮性胃炎、小腸の細菌汚染の増加は、キャッスルの外的要因であるコバラミンの欠乏を引き起こします。 この場合、貧血が発症し、肝臓と脾臓が増加します。
新陳代謝に 葉酸抗生物質、スルホンアミドは干渉します。 トリグリセリド、つまり中性脂肪は、そのような治療後に肝臓に蓄積する可能性があります。
ビタミン様化合物のコリンは脂質代謝を改善し、インスリンに対する細胞の感受性を高め、ブドウ糖の利用を促進します。 キンミズヒキに含まれている-薬用植物。
ビタミンUはチオクト酸またはリポ酸です。 重金属などの毒物による中毒の場合の解毒に使用されます。 脂肪肝症において脂肪親和性効果があります。 2型糖尿病には、抗低酸素剤として、またインスリン抵抗性を低下させるために処方されています。
胆汁酸
ウルソリフ、ウルソサン、ウルソファルク、ヘノファルク-胆汁酸。 それらは脂肪浸潤に複雑な影響を及ぼします:
- 細胞を損傷から保護します。
- それらは胆汁分泌促進効果があり、微生物叢の成長を抑制します 小腸-脂肪症の病因に重要な役割を果たすSIBO。
- 脂肪代謝を最適化することによりコレステロール値を下げます。
非アルコール性脂肪性肝疾患は、しばしば略称NAFLDと略され、その結果として脂肪が肝細胞に蓄積し始め、その機能を停止します。 予防策を講じず、一連の治療を受けていない場合は、高い可能性があります 重篤な合併症まで 致命的な結果..。 彼らによると、統計の乾燥した数字は期待外れであり、成人人口の最大40%がさまざまな程度の重症度でこの病気に直面しています。 この病気は、肝硬変や肝臓の脂肪変性と同じくらい危険です。 時間内に病気を決定することは非常に重要であり、そのために私たちがあなたのために準備した情報を以下に持っている必要があります。
非アルコール性脂肪性肝疾患は人口の40%に影響を及ぼします
NAFLDの種類
非アルコール性脂肪性疾患では、人間の肝臓に次のような多くの構造変化が起こります。
- 脂肪症;
- 肝臓肝障害;
- 脂肪性肝障害;
- 非アルコール性脂肪性肝炎。
脂肪症は、肝臓の脂肪が過剰であることを特徴としています。
非アルコール性脂肪性肝炎
NASHと略されます。 脂肪の蓄積だけでなく、時間の経過とともに炎症過程もあり、線維症や肝硬変を引き起こします。
医学的分類によると、NAFLDは一次と二次に分けられます。
原発性非アルコール性脂肪性疾患は、インスリンに対する体の反応の違反(インスリン抵抗性)の直接的な結果です。
二次NAFLDは、さまざまな理由で発生する可能性があります。 それらのほんの一部を次に示します。

NAFLDは、薬を服用した場合の副作用になる可能性があります。
- 薬を服用することによる副作用;
- 手術後の合併症;
- 腸疾患と 消化器系;
- 不適切な栄養;
- 食事療法、特に低タンパク質;
- 飢餓;
- 体重の急激な減少;
- 体の中毒。 きのこ、有機溶剤、リンによる中毒は特に危険です。
誰が危険にさらされているか
医学において、ホルモン、臨床および代謝障害の複合体を組み合わせたメタボリックシンドロームの概念。
特別なリスクグループには、以下に苦しむ人々がいます。
- 2型糖尿病;
- 肥満;
- 血中の高レベルのトリグリセリド。
2型糖尿病患者は、脂肪肝疾患を発症する可能性が70〜100%あります。
NAFLDの症例の大部分は、40〜60ゴスの中年の人々で診断されており、全症例の半分以上が女性で発生しています。 しかし、この病気は太りすぎに苦しんでいる子供たちにしばしば発生します。
病気につながる主な原因
すべてのリスク要因は、外部と内部の2つのグループに分けることができます。
外部インクルード:
- 脂肪の多い揚げ物が主流の食品。
- 肝臓での脂肪の生成と蓄積に寄与するのは炭水化物であるため、お菓子の過剰摂取。
- コーヒーへの過度の情熱;
- 悪い習慣:アルコール、喫煙、薬物使用;
内部要因のリストは次のとおりです。

非アルコール性脂肪性肝疾患は、貧しい食生活と肥満に起因する可能性があります
- 肥満;
- いくつかの病状の後の合併症、肝硬変;
- 遺伝的要因;
- 体の年齢と自然な老化;
- 血中の大量の「悪玉」コレステロール。
- 腸内毒素症。
知っておくべき重要なこと! 病気の名前には「ノンアルコール」という言葉が含まれています。これは、危険因子からアルコールを除外することを意味します。 しかし、飲酒は補完することによっても役割を果たすことができることを覚えておく必要があります ノンアルコールファクター危険。 健康な人では、肝臓の脂肪の割合は約5%です。 一方、アルコールは、体内での脂肪酸の生成を促進し、それらの酸化を防ぎ、血液の組成とトリグリセリドの量を侵害し、肝硬変を発症します。
症状
非アルコール性脂肪性肝疾患は、ほとんどの場合、すでに後期段階で病理が検出されるため、非常に危険です。 これは、 病気は症状なしで、またはわずかな逸脱を伴って長期間進行します、ほとんどの患者はこれをあまり重視していません。
脂肪肝を伴う 初期次の症状のみを区別できます。
- 弱点;
- 速い疲労性;
- パフォーマンスの低下。
- 眠気の増加;
- 高血圧;
- 肋骨の下に 右側わずかな不快感とわずかな重さ;
- 肝腫大;
- 血管の「アスタリスク」の形成。
病気の発症と肝臓への大量の脂肪の蓄積により、症状は明白な特徴を帯び始めます:
- 皮膚のひどいかゆみ;
- 吐き気の絶え間ない感覚;
- 消化不良と便;
- 皮膚と目の白が黄色になります(黄疸);
- 腹部の増加は視覚的に目立つようになります。
- 重度の認知障害が現れます。
診断
非アルコール性脂肪性肝疾患を診断するため、またはそれを否定するために、患者に面接して最初に診察した後、医師は一連の検査と診断手順を処方します。 先に述べたように、NAFLDには実質的に症状がなく、存在する症状は他の多くの疾患に固有のものであり、分化する必要があります。
分析の中で、最も有益なのは 生化学的分析血液。肝臓の状態を評価するための多くの指標が含まれています。
NAFLDの診断で最も難しいタスクの1つは、アルコール成分の影響の排除または評価です。 評価のための多くの特徴的なマーカーがありますが、そのようなテストは、病気の発症に対するアルコールの影響について常に明確な答えを与えることができるとは限りません。
NAFLDの治療方法
非アルコール性脂肪性肝疾患の治療は包括的でなければなりません。
薬物療法には以下が含まれます:

非アルコール性脂肪性肝疾患の治療は包括的でなければなりません
- 代謝の正常化;
- 酸化ストレスの予防;
- 正常な腸内細菌叢の回復;
- 脂肪肝症の治療;
- 線維症および他の関連する病状の治療。
太りすぎの患者さんには、食事制限や食事療法の遵守が特に必要であり、それとの闘いが治療のポイントのひとつです。 統計によると、10%の体重減少はすでに幸福の大幅な改善につながり、病気は後退し、後退します。 しかし、そのような食事療法は、有能な栄養士によって独占的に開発されるべきであり、その遵守は、中間の医学的監督を伴うべきです。 体重と飢餓を減らしたいという独立した欲求は、壊死的な結果と、急性期への病気のオーバーフローと壊死の発現につながる可能性があります。
患者が肥満であるかどうかに関係なく、彼の食事には十分な量のビタミンとミネラルが含まれている必要があり、タンパク質の量は十分に多い必要がありますが、逆に動物由来の脂肪は可能な限り除外する必要があります。
多くの食品には、肝臓での脂肪の蓄積を抑制し、それらの浸潤を引き起こして、脂肪肝を正常に戻す能力があります。 これらの中で最も人気のあるものは、オートミール、小麦、 そば、 カッテージチーズ。
NAFLDに常に処方されている「EssentialeforteN」という薬の基礎となる必須リン脂質は、NAFLDとの闘いに役立ちます。 その受信は開発の速度を減らすのに役立ちます 結合組織脂質代謝を正常化します。 これにより、脂肪が肝細胞に蓄積する理由がなくなります。
患者は彼のライフスタイルを完全に修正する必要があります、観察します 正しい食事そして十分な身体活動。 ただし、ここにも注意点があります。過度の負荷は非常に有害であるため、身体活動を行う必要があります。スポーツに参加する必要がありますが、投与します。 患者は、インターネットで流行しているアドバイスとは異なる方法で、理学療法士に相談し、彼らの推奨事項に従うことをお勧めします。
治療の予後は初期段階でのみ良好であり、後期段階では、完全な肝臓の損傷と死亡のリスクが非常に高くなります。
予防

NAFLDの予防とは、健康的でアクティブなライフスタイルを維持することです。
NAFLDの予防は、健康的でアクティブなライフスタイルを維持し、回避することで構成されます 悪い習慣、あなたの精神的感情状態の制御とストレスの量を最小限に抑えます。
コレステロール値を管理し、低下させる対策が必要です。
さまざまな生物学的食品添加物(栄養補助食品)がインターネットやメディアで広く宣伝されており、ほとんどが輸入品ですが、国内のものもあります。 それらの成分はすべて同じ必須のリン脂質、カルニチン、ビタミンであり、脂肪代謝を正常化し、肝硬変を予防するのに役立ちます。 あなたはそのような薬に用心する必要があり、それらを肝疾患の万能薬と見なさないでください。 購入する場合は、最初に医師に相談してください。販売者は、栄養補助食品が合法であり、期待される利益の代わりにあなたに害を及ぼさないことを確認するために、免許と証明書を要求する必要があります。
結論
医学の発展にもかかわらず、NAFLDの出現につながる病気の経過と原因または病因の完全なリストはまだ徹底的に研究されていません。 太りすぎ、糖尿病、心臓血管系の病気との関連についてのみ知られています。
誰もこの病気に免疫がなく、脂肪肝を持つ人々の数は、ある程度、目を見張るものがあります-これは、私たちの国のほぼ毎秒の住民です。 非アルコール性脂肪性肝疾患は現代の真の問題になりつつあり、国が繁栄し、人口の生活水準が高いほど、診断される症例は多くなります。 肝硬変はNAFLDほど一般的に診断されません。
非アルコール性脂肪性肝疾患の場合、たとえば、アルコール依存症に起因する病変のように、すべてが単純なわけではありません。 確かに、健康的で正しいライフスタイルでさえ、保証を提供するものではありませんが、NAFLDの可能性を減らすことしかできません。 大きな問題は、肝臓に脂肪沈着物が蓄積することは、障害が全身性になるまでまったく現れないことです。この場合、治療を行っても、死亡する可能性が高くなります。
唯一の方法は、定期的に医師による予防検査を受け、肝臓の状態や異常の出現を判断するための検査に合格することです。
ビデオ
脂肪性肝障害。 脂肪肝。 脂肪肝疾患。 非アルコール性脂肪性肝炎。
脂肪肝疾患は、肝臓に脂肪沈着物が蓄積することを特徴としています。 それらは細胞内で形成され、その結果、肝細胞(肝臓の構造要素)の正常な発達が妨げられます。 時間が経つにつれて、健康な細胞は脂肪代謝産物に置き換えられます。 病気の進行に伴い、肝臓組織に瘢痕が形成されます(線維症が形成されます)。 肝臓はその生物学的機能を実行しなくなり、患者は気分が悪くなり、特定の症状が現れ始めます。
この病気には多くの名前がありますが、現時点では一般的に受け入れられている医学名は脂肪肝肝症のように聞こえます。 理由から、この病気にはアルコール性肝炎とノンアルコール性の2種類があります。 非アルコール性脂肪性肝疾患(NAFLD)は、さまざまな理由で発生します。
WHOによると、この病気は先進国の人口の最大25%に影響を及ぼします。 専門家は警報を鳴らし、現在の状況は流行と呼ぶことができると言います。 現在、NAFLDは文明の病気、つまり進行が幸福のレベルに直接関係している病気として分類されています。
病気の発症段階
進行性疾患には3つの主要な段階があります。 最初の段階は脂肪症と呼ばれます。 肝細胞の脂肪変性が特徴です。 過剰な脂肪が細胞に入り、細胞の排泄が遅くなります。
脂肪性化合物の特定の割合が細胞に蓄積すると、第2段階が始まります-脂肪性肝炎。 それは肝臓の炎症過程の発達によって特徴づけられます。
3番目の最後の段階は、肝細胞が結合組織細胞に置き換わることを特徴としています。 したがって、肝臓はその主要な機能を部分的に失い、線維症が発症し、次に肝硬変が発症します。
非アルコール性脂肪肝疾患の発症は、アルコール性脂肪肝疾患の発症と類似しています。 病気は同じ3つの段階を経ます。 違いは、病気の原因と病理学的プロセスの進行速度にあり、ノンアルコール飲料はよりゆっくりと進行します。
脂肪肝疾患の原因
病気は完全には理解されていないので、病気の発症のいくつかの危険因子について話すのが通例です:

- 太りすぎ、特に肥満。 太りすぎの人はこの病気に60%かかりやすいことが証明されています。 肥満の極端な段階の場合、この数字は90%に上昇します。 データは、成人と肥満児の両方に関連しています。
- 正常体重の人の腹部脂肪の過剰な蓄積も、NAFLDを発症するリスクを高めます。
- インスリン抵抗性。 この危険因子は、2型糖尿病の患者だけでなく、重度の肥満の患者にも関係があります。
- 腸内細菌叢の不均衡、消化不良につながる消化管のいくつかの病気。
- 肝毒性のある薬の長期使用。
専門家は、この危険因子のリストは、近年の罹患率の急激な増加を説明していないことに注意しています。 現在、WHOによって支持されている一般的な仮説があります。 彼女は、この病気の主な原因は炭水化物、特に食事療法士の間で人気のあるフルクトースの過剰摂取であると述べています。
ノンアルコール飲料の症状
一般的な症状は次のとおりです。
- 不当な倦怠感、倦怠感の増加。
- 右季肋部の膨満感と不快感、わずかな痛み。
- 食欲不振。
脂肪肝疾患の特定の症状は、疾患が進行するにつれて現れます:
- 定期的な吐き気、嘔吐が可能です。
- 肝臓の痛みと不快感。
- 皮膚と強膜の黄変。
最初の段階では、患者は病気の症状にまったく気付かないかもしれません。 機器診断を使用して、初期段階で病気を特定することが可能です。
非アルコール性脂肪性肝疾患の診断と治療
診断を下すために、いくつかの検査が使用されます。
- 腹部臓器の超音波。
- 肝臓エラストグラフィ。
- 検査室診断(臨床的および生化学的血液検査)。
- 臓器のコンピュータ断層撮影 腹腔.
NAFLDの治療は、診断後にのみ開始されます。
治療は保守的です。 食事療法を処方し、すべての有害で挑発的な要因を除外します。 脂肪肝疾患の主な治療法は、肝細胞をさらなる損傷から保護する薬を服用することです。
治療の本質は、残りの肝細胞を保護し、体重を減らすことです。 わずか5%の体重減少で、患者は顕著な改善に気づきます。 徐々に体重を減らすことが重要です。急激な体重減少は病気の悪化につながる可能性があります。 したがって、肝肝疾患の治療は、疾患を退行させ、患者の健康を改善することを目的としたあらゆる範囲の保守的な対策です。
私たちの医者
NAFLDの予防
この病気を予防するための主な推奨事項は、健康的なライフスタイルを維持することです。 維持 通常の体重そして適切な栄養。 できるだけ多くの危険因子を排除することが重要です:体重を監視し、食べ過ぎないで、悪い習慣を取り除きます。
予防策の中には、アクティブなライフスタイル、適度な身体活動、適切な飲酒レジメンもリードしています。
引用の場合: Makhov V.M.、Volodina T.V.、Panferov A.S. アルコール性および非アルコール性脂肪肝疾患-腹部消化//紀元前も考慮に入れます。 2014. No.20。 S. 1442
胃腸病学における診断と治療への臓器疾病分類学的アプローチは、肝臓、胆道(BH)、および膵臓(RV)の疾患が別々に考慮されるという事実につながります。 消化器系の器官の解剖学的および生理学的関係によって引き起こされる問題は、背景に後退する可能性があります。 システム内のリンクが失われると、その後の変更がカスケードされます。 一般的な病因はまた、併存する病状につながります:アルコール、脂質および炭水化物代謝の障害、食事中のタンパク質欠乏、ウイルスおよび細菌感染。
肝臓と膵臓の「友好的な」病状、つまり消化と代謝のプロセスの主な参加者に最大の注意が向けられています。 この同時関与は、「肝膵臓症候群」の概念によって定義されます。
治療では、肝臓と膵臓の同時機能障害によって引き起こされる結果を考慮する必要があります-アルコール性脂肪肝疾患(AFLD)と非アルコール性脂肪肝疾患(NAFLD)の重要な共通の病原性基盤を持つ病理学で発生します。 臓器機能障害の全身的な組み合わせの最も重要な結果は、虫歯の消化の違反です
肝臓、膵臓、胃腸管は、アルコールの病理学的影響に最も影響を受けやすいです。 慢性的な消化器系への損傷の兆候 アルコール中毒(CAI)にはいくつかの特徴があります。病変の重症度はアルコール依存症の期間と直接相関し、消化管の病理には多臓器の全身性があります。 プロセスへの関与の発達、順序および程度は、主に臓器の解剖学的および機能的関係によって決定されます。
次のような多くの要因が、CAIの消化器官への同時損傷につながります。
..。 細胞や臓器に対するアルコールの同じタイプの効果;
..。 単一の運河(消化管);
..。 消化プロセスへの相互依存的な参加。
..。 全身代謝;
..。 神経液性調節のコミュニティ。
毎日のアルコール摂取量が40〜60 g(男性の場合)および20 g(女性の場合)を超えると、「アルコール性肝疾患」(ABD)の概念と一致して、肝臓に形態学的変化が起こります。
臨床的および実験的に、肝臓損傷の重症度がCAIの期間およびエタノールの量に直接依存することが示されています。 CAIによる肝臓の形態学的変化は、次の段階を経ます。
..。 脂肪変性;
..。 肝炎(急性、慢性);
..。 線維症;
..。 肝硬変。
脂肪肝疾患(FAD)では、脂肪、主にトリグリセリド(TG)の量が、臓器の乾物の5%以上に達します。 FDPは、アルコールによって引き起こされるすべての肝臓病変の最大85%を占めます。 RWPは門脈路の炎症性浸潤を伴わないことが強調されています。
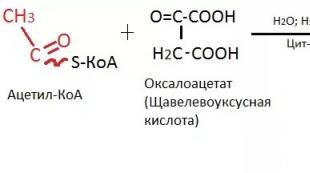
アルコールは酵素アルコールデヒドロゲナーゼ(ADH)の関与によりアセトアルデヒドに酸化されます:10-15%-胃粘膜で、80-85%-肝臓で、5%はそのまま尿中に排泄されます。 アセトアルデヒドは非常に毒性があります。 病原性の影響は、細胞質ゾルで形成されるアセトアルデヒドの量に依存します。これは主に、受け取ったアルコールの量とその酸化速度によるものです。 エタノールの酸化速度は、個人で利用可能なADHアイソザイムの活性に直接関係しています。 肝臓中のアセトアルデヒドの量は、その形成速度とさらなる代謝速度の両方に依存します。 アルデヒドデヒドロゲナーゼが関与するアセトアルデヒドは、アセチルCoAに変換され、次に酢酸に変換され、続いて二酸化炭素と水に代謝されるか、クエン酸回路に含まれ、脂肪酸を含む他の化合物に変換されます。
脂肪変性では、他の肝毒性因子がない状態でのアルコール摂取の停止は、肝細胞の完全な形態学的正常化につながります。
あらゆる病因の脂肪変性における肝臓でのTG蓄積の病因には、以下の主な関連が含まれます。
..。 遊離脂肪酸(FFA)の摂取量の増加;
..。 肝細胞のミトコンドリアにおける脂質合成の増加;
..。 肝細胞のミトコンドリアにおける脂質のβ酸化の活性の低下;
..。 肝臓からのTGの排出を遅くします。
有機溶媒としての肝臓組織中のアルコールは、細胞やミトコンドリアの膜を損傷する可能性がありますが、肝臓組織中のアセトアルデヒドの高濃度と長期濃度、および関連するニコチンアミドアデニンジヌクレオチドの高含有量は、アルコールLAD。 同時に、末梢脂肪分解が強化され、肝臓による脂肪酸の取り込みが増加します。 肝細胞内の脂肪封入体の数とサイズの過度の増加は、肝細胞の代謝とその死の致命的な違反、すなわち脂肪壊死につながります。
アセトアルデヒドの関与による脂質過酸化(LPO)の開始は、壊死につながります。 LPOの活性化は、肝小葉の酸素需要の増加、特に小葉中心部での低酸素症の発症につながります。 病因を理解する上で重要なのは、アセトアルデヒドのリン脂質(PL)への結合の影響であり、これは細胞膜とミトコンドリア膜の破壊につながります。
CAIの抗酸化防御の枯渇を背景に、酸化ストレスの発生の推進力は、特に脂肪分の多い食品との組み合わせで、アルコール過剰である可能性があると考えられます。
J. Ludwig etal。 1980年、アルコールを乱用しなかった人の肝臓を調べたところ、アルコール性肝炎と同じ組織像が見つかりました。 NAFLDと呼ばれる肝臓病理学のこの病因的変異のダイナミクスは、アルコール性に似ています:FDP(非アルコール性脂肪性肝炎)-非アルコール性脂肪性肝炎(NASH)-肝硬変。
NAFLDの診断基準:
..。 穿刺生検データ:アルコール性肝炎と同様のFDPまたは炎症性変化。
..。 肝毒性用量でのアルコール消費の欠如;
..。 他の肝臓の病理の欠如。
2007年に、NAFLDの有病率を特定し、この病気の発症の危険因子を決定するために、スクリーニングプログラムがロシアで実施されました。 ポリクリニックで30,787人の患者を検査したところ、NAFLDは患者の26.1%で観察されました。 このグループでは、FSが79.9%、NASHが17.1%、肝硬変が3%で検出されました。
伝統的に、NAFLDの病因には2つの段階(2つの「ショック」)があります。 1つ目は、炭水化物と脂質代謝の違反によるものです。 同時に、NAFLDおよびNASHの病因におけるインスリン抵抗性の高い役割が注目されています。 NAFLDは、インスリン抵抗性が主要な関連であるメタボリックシンドロームを伴うことが非常に多いことが指摘されました。
病因の段階に従って、一次および二次NAFLDが区別されます。 原発性NAFLDでは、病因が肥満の場合、2型糖尿病(DM)、高脂血症、高レベルのトリグリセリド、リポタンパク質、および血液と肝臓のFFAが検出されます。 肝臓でのFFAの蓄積は、高い血中インスリンレベルに寄与します。 インスリンはFFA、TGの合成を刺激し、FFAのβ酸化と肝臓からの脂質の排出速度を低下させるため、肥満、2型糖尿病、メタボリックシンドロームに伴う高インスリン症は病因です。 NASHの一次変異体の「最初の推進力」は肝細胞におけるFFAの蓄積であると考えられています。 FFAは反応性の高いLPO基質です。 活性ラジカルの形成を伴うこのプロセスは、ミトコンドリアと細胞膜への損傷につながります。
肝臓におけるFFAの過剰な蓄積のみが必要であるが、酸化ストレスの発生には十分ではないことが理解された。 NASHとNAFLDの二次変異体につながる「二次ショック」の概念が策定されました。 誘発物質として、「第二の推進力」の追加の要因は、薬物の効果、食物中の抗酸化物質の不足、ホルモンの不均衡と考えられています。
「二次的」NAFLDおよびNASHが発生する疾患および状況のリストは非常に幅広く、以下が含まれます。特に肥満の手術中の吸収不良症候群。 激しい体重減少; 長期的で不均衡な非経口栄養; 蓄積性疾患。 また、アミオダロン、グルココルチコステロイド、テトラサイクリン、非ステロイド性抗炎症薬、メトトレキサート、合成エストロゲン、タモキシフェンなどの摂取がNASHの発症を伴うことが非常に多い薬物も特定されています。
したがって、ABDとNAFLDの病因における共通の関連性が追跡されます:まず第一に、LPOの活性化、酸化ストレス、ミトコンドリア膜のPLへの損傷、脂質代謝の全身的および細胞的関連性の破壊。 アルコール依存症、肥満、インスリン抵抗性、高脂血症、腸の消化障害などの素因の「クロス」を想定することも可能です。
RWPは、びまん性の病理学的細胞内脂肪沈着を特徴とします-より多くの場合、粗い液滴。 脂肪症の強度に応じて、肝細胞は正常に機能するか、脂肪壊死が発症します。 原則として、RWDは無症候性であり、肝腫大が検出された場合、患者は誤って医師の監督下に置かれます。 機能性肝機能検査はわずかに変更されています。患者の1/3で、わずかな非抱合型高ビリルビン血症、高血中コレステロールおよびTGが見られます。 ALTおよびAST、g-グルタミルトランスペプチダーゼの活性の増加は、観察の半分未満で認められ、アルコール過剰に続きます。
患者は、右季肋部またはみぞおちの食欲不振、不快感、鈍い痛み、吐き気を訴えることがあります。 触診により、肝臓が肥大し、滑らかで、縁が丸くなっていることがわかります。 超音波診断は、肝実質の構造のびまん性の中等度の超エコー源性を診断します。 診断は組織学的に確認する必要があります。
膵臓はアルコールに対してより敏感であるため、膵臓の肝臓のアルコール量に対していわゆる比較的安全な量は、男性では2倍、女性では3倍減らす必要があります。 膵臓の細胞内のアルコール濃度は、血中の濃度の60%に達します。 エタノールの直接的な効果の結果として、脂肪酸の合成の増加とそれらの酸化の減少から生じる膵臓の脂肪浸潤が現れます。 グリシル-プロピル-ジペプチド-アミノ-ペプチダーゼの活性の増加により、コラーゲン産生も増加します。 この場合、大きな十二指腸乳頭に対するアルコールの直接的な影響は、オッディ括約筋のけいれんを伴います。
肝毒性のある用量でアルコールを飲むと、常にアルコール性慢性膵炎(ACP)が発症します。 臨床機器研究により、CAIのあらゆる形態の慢性膵炎(CP)を特定することができます。 ACPの進行は、腺の石灰化の形成、脂肪便および糖尿病の発症につながります。 アルコールを拒否しても、膵臓の構造は正常化されません。
AFLDとACPの開発は、胃嚢の状態の違反と組み合わされています。 したがって、CAIの286人の患者の超音波検査は、検査された膀胱壁の肥厚と肥厚の31%で胆嚢の変形を明らかにしました-それぞれ58%と51%、そして動的超音波胆嚢造影で、運動機能低下性ジスキネジアは48%で診断されました。 胃十二指腸内視鏡検査では、52%の患者で乳頭炎、22%の患者でオッディ括約筋の機能不全が明らかになりました。 したがって、重要な状況があります。ACPでは、二重依存性CPに固有の病因因子に遭遇することがよくあります。 したがって、ACPを用いた内視鏡的逆行性胆道膵管造影の実施中に、総胆管膵臓逆流が8%で検出され、総胆管の末端部分の狭窄が20%の症例で検出されました。
V 臨床像 AFLDは、CAIの全身性の複数の臓器への影響において重要な役割を果たします。外分泌機能不全を伴うCP、吸収不良につながる慢性萎縮性胃炎です。 の過剰な細菌の増殖 小腸腸の消化不良を悪化させます。
摂食障害、炭水化物および脂質代謝の障害も、AFLDおよびNAFLDの発症における一般的な要因と見なすことができます。 AFLDの患者の1/3で、肥満度指数の増加が認められます。 これは、追加のアルコールカロリー(1.0gエタノール-7kcal)、アルコールによる酸生成の刺激、食欲増進、および過剰な動物性脂肪とおいしいスナックを含む食品の制御されていない消費によるものです。 「空腹」の酩酊状態では、食事中のタンパク質が不足しているだけでなく、不飽和脂肪酸、抗酸化物質、ビタミンも不足しています。 血中のTGとコレステロールの含有量の増加もCAIで認められました。 アルコール依存症の血中のインスリンとC-ペプチドのレベルの研究は、真の高インスリン血症を示しました。
NASHの診断基準の1つは、肝毒性用量でのアルコール消費がないことです。つまり、NASHの識別は、消費されたアルコールの量を決定することに基づいています。 患者との会話では、彼が飲んでいるアルコールの量について正確なアイデアが得られることはめったにないことに留意する必要があります。
RWDのアルコール発生により、鼻の血管拡張、強膜の注射、手のひらの紅斑、耳下腺の肥大、女性化乳房、デュピュイトラン拘縮を観察することができます。 身体検査データはあまり有益ではありません。
アルコール関連の病状では、痛みの訴えはそれほど顕著ではなく、これはエタノールの鎮痛、抗うつ、陶酔効果の効果であると考えられています。
AFLDでは、月曜日(金曜日と土曜日にアルコールを飲んだ後)に無力症候群や胃や腸の消化不良の症候群が発生すると、「週末症候群」の一部となる症状が現れることがあります。 NAFLDの場合、患者は、上腹部痛症候群または食後苦痛症候群のいずれかの変種における機能性胃消化不良の特徴である胆嚢のジスキネジアによって引き起こされることが最も多い愁訴を示します。
アルコール性脂肪性肝炎(ASH)では、腸の消化不良の症状がより頻繁に観察され、NASHでは、 病理学的プロセス胆嚢。
KhAIの客観的マーカーは結果です 実験室研究:
..。 γ-グルタミルトランスペプチダーゼ(GGT)の血中活性の増加;
..。 クラスA免疫グロブリンの血中濃度の上昇;
..。 赤血球の平均量の増加;
..。 ALTの活性を超える血中のASTの活性の増加;
..。 血中トランスフェリンの増加(炭素欠乏)。
ASHの細胞溶解の実験室指標は、アルコール摂取からの経過時間に依存しますが、ASHのGGTのレベルはNASHよりも著しく高くなっています。 これは、小葉中心帯における小管胆汁うっ滞の発現によるものです。
NASHとASHの両方の経過と予後は、高度の肥満、高トリグリセリド血症、インスリン抵抗性、肝血液酵素の高活性など、進行の一般的な要因の存在も決定します。 高齢者、栄養失調。 ABDとNAFLDの病因の組み合わせは、併存疾患として定義されます。 アルコール禁止は、AFLDとNAFLDの両方の治療において必須であると考えられています。
AFLDとACPの併存症、および消化管の共存機能障害は、腸の消化障害の深刻な原因です。 脂肪便は、ACPの診断トライアドに含まれています:石灰化、脂肪便、真性糖尿病。 アルコール化は、膵臓の排泄機能のより高い減少率を伴います。 NAFLDでは、腸の消化不良の発症に寄与する状況も特定されています。 NAFLDを伴う肝細胞における脂質の蓄積は、一次胆汁酸の産生および胆汁酸へのそれらの摂取の減少につながることが示されています。 十二指腸(KDP)。 糖尿病の経過には、胃腸障害や合併症のさまざまな症状が伴います。 多くの研究者が、糖尿病患者の胆嚢収縮性の低下を示しています。
エラスターゼ-1を測定した試験では、糖尿病患者の3分の1以上で酵素の排泄が減少し、糖尿病と肥満の組み合わせで膵臓機能不全のリスクが高くなることが明らかになりました。
実証されたプラスの影響 代替療法 NAFLDの肝臓の構造的および機能的状態に対する膵臓酵素。 病因における同様の関連性の存在は、ABDおよびNAFLDの治療へのアプローチにおける共通の立場を議論することを可能にします。
肥満とインスリン抵抗性はNAFLDとNASHの発症の主な要因であるため、非薬物療法の主な目的は、主に脂肪と炭水化物による食事のカロリーを減らし、増加させることです。 身体活動..。 減量は個別化されています。 一般的な原則:ゆっくりとした体重減少(月に1.5〜2kg); 単純な炭水化物、飽和脂肪の摂取に対する厳しい制限。 食事には十分な量の植物繊維(30〜40 g /日)を含める必要があります。小麦ふすま、亜麻仁を使用することをお勧めします。
アルコールを避けることは治療の重要な要素です。 患者の1/3は飲酒をやめ、1/3は減量するだけで、1/3は通常の量で飲酒を続けると考えられています。 耐性が低く、二日酔い症候群やその症状が弱い人、疑わしい人(コーディング!)、そして社会的地位の高い人は、原則として飲酒をやめます。
アルコールの継続使用は、治療を拒否する理由ではありません。 アルコール投与量の減少を背景にエッセンシャルPL(EPL)を使用すると、プラセボを投与された患者と比較して、患者の線維症形成率が低下することが実証されました。
RWDの病因における主要なリンクの有害な影響を排除することを目的とした最も重要な病原的に実証された、十分に証明された手段はEPLです。
EPLはホスファチジルコリンであり、主にリノール酸(約70%)、およびリノレン酸とオレイン酸の多価不飽和脂肪酸が含まれています。 多価不飽和脂肪酸を多く含むホスファチジルコリンは、ポリエニルホスファチジルコリン(PPC)とも呼ばれます。 健康な人は、主に食品から多不飽和脂肪酸を摂取します 植物油..。 産業目的で作成する 薬物 PPCは大豆から抽出されます。 PPCには、バイオアベイラビリティが最も高く、EPLの有効成分である1,2-ジリノレオイルホスファチジルコリンが含まれています。
1カプセルに300mgのEPLを含む薬剤はEssentiale®forteNです。
Essentiale®forteNは、肝保護剤のグループで主導的な地位を占めています。 この薬は、50年以上にわたって世界の多くの国で広く成功裏に使用されてきました。 Essentiale®forteNの有効性と安全性は、数多く実証されています。 臨床研究、これは重要ですが、二重盲検法を含みます。 Essentiale®forteNは、EPLを含む製剤の中で最も研究されている薬剤です。
細胞膜とミトコンドリアの代謝に対するプラスの効果、抗酸化効果、脂質代謝に対する正常化効果は、「交差」病因を考慮に入れて、AFLDとNAFLDでEssentiale®forteNをうまく使用するための鍵でした。 さらに、NAFLD患者のホスファチジルコリンの含有量は、健康な個人の含有量と比較して大幅に減少していることが示されています。
AFLDとNAFLDの両方での空洞消化は、栄養素の分解障害につながる要因の影響を受けやすくなっています。 吸収不良の発症を伴う腹部消化の異常の検出は、多酵素補充療法の任命の主な適応症です。
AFLDでは、腸の消化不良の主な原因は、膵臓の外部分泌の減少とBVDの機能の欠陥です。NAFLDでは、胆汁の組成の変化、胆嚢ジスキネジア、酵素産生障害が優勢です。
このような臨床状況では、パンクレアチン、胆汁、ヘミセルロースを含む複合置換剤を処方することをお勧めします。 実績のあるFestalはそのような手段に属します。 1つの耐酸性コーティング錠には192.0mgのパンクレアチンが含まれています。 国際薬剤師連盟の単位では、この量は6000 IUのリパーゼ、4500 IUのアミラーゼ、300IUのプロテアーゼに相当します。 この薬には、ヘミセルラーゼ-50.0mgと胆汁成分-25.0mgも含まれています。
十二指腸に入るパンクレリパーゼは腸の消化に含まれ、酵素の不足を補ったり、膵臓の酵素を補ったりします。 製剤中の胆汁酸とヘミセルラーゼの存在は、製剤の有効範囲を大幅に拡大します。 胎児の胆汁酸は、一次胆汁酸の肝臓産生が低下した場合、および十二指腸への胆汁の流れが不十分または調整されていない場合に、脂肪を独立して乳化します。 したがって、胆汁補充療法が行われます。
フェスタルの胆汁酸は膵臓の分泌活動を刺激し、腸の運動性を加速することに注意する必要があります。 それらは真の胆汁分泌促進剤であり、腸への胆汁の流れを増加させます。 これは、胆汁の殺菌作用の強化、汚染の減少を伴います。
薬を服用する際に特別な議論が必要な重要な点は、外分泌膵臓機能の刺激です。 痛みを伴う慢性および急性膵炎では、そのような効果は受け入れられないことは明らかであり、この薬はCPの悪化には推奨されません。 胆汁の存在による禁忌のリストには、高ビリルビン血症、閉塞性黄疸、胆嚢の蓄膿症が含まれます。
薬の組成に含まれるヘミセルラーゼは、腸の消化不良を軽減するのに役立ちます。 この酵素は植物繊維の多糖類を分解し、ガスの生成を減らし、鼓腸の減少によって臨床的に現れます。
Festalの機能を分析することで、Essentiale®forteNとともにAFLDおよびNAFLDに使用できます。TherapyEssentiale®forteNは、病原的に正当化され、脂肪変性のあらゆる病因に受け入れられます。 フェスタルコースを導入する必要があるのは、膵臓の外部分泌の状態、肝臓の胆汁形成機能、および胆嚢の緊張によるものです。
Essentiale®forteNとFestalaの共同コースの期間は次のように決定されます。Essentiale®forteNは2カプセル3r。/日を少なくとも3か月間服用し、コースは2〜3r。/年繰り返されます。 胎児療法の期間は、腸の消化不良の臨床像、脂肪便の程度、超音波中の胃腸管の状態によって決定され、3〜4週間である可能性があります。 数ヶ月まで。
FDP、一次または二次外分泌膵臓機能不全、およびGVD機能不全の組み合わせの場合は、Essentiale®forteNとFestalの併用療法が推奨されます。
Essentiale®forteNとFestalaの病原的に実証された併用により、膵臓および胆管の機能不全と組み合わせて、あらゆる病因の気道の治療を最適化することができます。
文学
1. Makhov V.M.、Ugryumova L.N.、Gitel E.P. etal。慢性アルコール依存症における肝膵臓症候群// Ter。 記録。 1987. No. 12.S.68-71。
2.モイセーエフS.V. 敗北 内臓アルコール依存症//医者。 2004. No. 9. S.15-18。
3.ハザノフA.I. 私たちの時代の重要な問題はアルコール性肝疾患です// Ros。 zhurn。 胃腸病学および肝臓学。 2003. No. 2. S.13-20。
4. Pavlov Ch.S.、Zolotarevsky VB、Ivashkin V.T. 生検データとその組織の形態学的研究による慢性肝疾患の構造//胃腸病学、肝臓学、結腸直腸学のロシアジャーナル。 2007. No. 1. S.90-95。
5. Khomeriki S.G.、Khomeriki N.M. アルコール性肝疾患:発症のメカニズム、形態学的症状、鑑別診断、および治療への病因的アプローチ// ConsiliumMedicum。 消化器病学。 2012. No. 1. S.27-34。
6. Sherlock S.、Dooley J. Liver、および 胆道:実用的な手。 /あたり。 英語から ed。 Z.T. アプロシナ、N.A。 ムヒナ。 M。:GEOTAR-Med、2002.859p。
7. Kostyukevich O.I. アルコール性肝障害:社会的影響、臨床的影響および病因療法の側面// RMJ。 2007. No. 2. S.62-67。
8.モイセーエフV.S. アルコール関連の病状の診断と治療の問題:開業医のための講義。 XIロシア国民会議「人と医学」。 M.、2004.S。370-381。
9. Ludwig J.、Viqgiano T. R、McGill D. B. Ob Bj非アルコール性脂肪性肝炎:これまで名前のない病気でのMeyoクリニックの経験// Meyo ClinProc。 1980年。 55. P.434-438。
10. Ivashkin VT、Shulpekova Yu.O. 非アルコール性脂肪性肝炎//消化器系の病気。 2000. No. 2. S.41-45。
11. Polunina T.E.、Maev I.V. 非アルコール性脂肪性肝疾患:疫学、病因、診断、治療// ConsiliumMedicum。 消化器病学。 2012. No. 1. S.35-40。
12. Drapkina O.M.、Smirin V.I.、Ivashkin V.T. NAFLDの病因、治療、疫学-何が新しいのか? ロシアにおけるNAFLDの疫学//紀元前。 2011. No. 28. S.1717-1721。
13. Vovk E.I. セラピストの実践における非アルコール性脂肪性肝疾患の治療:何ですか? どこ? いつ? // RMJ。 2011. No. 11. S.1038-1046。
14.マコルキンV.I. メタボリック・シンドローム。 M。:MIA、2010.S.142。
15. Larter C.Z.、Farrell G.C. インスリン抵抗性、アディポネクチン、NASHのサイトカイン:これは//J.Hepatolを治療するための最良の標的です。 2006.Vol。 44. P.253-261。
16. Makhov V.M. 消化器系のアルコール依存性病変の診断と治療。 M.、2005.S。24。
17. Makhov V.M.、Gitel E.P.、Ugryumova L.N. 慢性アルコール依存症における膵臓のホルモン産生機能の評価//実験室での作業。 1987. No. 1. S.16-21。
18. Marschall H.-U.、EinarssonC。胆石症// Journal ofInternalMedicine。 2007.Vol。 261.P.529-542。
19. Leites Yu.G.、Galstyan G.R.、Marchenko E.V. 糖尿病の消化器合併症// ConsiliumMedicum。 2007. No.2。
20. Polunina T.E. 糖尿病における消化管の病理//効果的な薬物療法。 消化器病学。 2011. No. 5. S.36-42。
21. Ebert E.C.糖尿病の胃腸合併症//Dis。Mon。 2005.Vol。 51(12)。 P.620-663。
22.GürsoyM。、GüvenerN。、Isiklar I.、Tutal E.、Ozin B.、Boyacioglu S.II型糖尿病患者の胆嚢収縮性に対するシサプリドの効果//肝胃腸病学。 2001年9月-10月 巻 48(41)。 R.1262-1265。
23. Gaur C.、Mathur A.、Agarwal A.、Verma K.、Jain R.、SwaroopA。胆嚢機能障害を引き起こす糖尿病性自律神経障害// J Assoc PhysiciansIndia。 2000年6月 巻 48(6)。 R.603-605。
24. Sharma M.P.、Saraya A.、Anand A.C.、Karmarkar M.G. 糖尿病における胆嚢運動障害-超音波検査// TropGastroenterol。 1995年7月-9月 巻 16(3)。 R.13-18。
25. Nunes A.C.、Pontes J.M.、Rosa A.、Gomes L.、Carvalheiro M.、FreitasD。糖尿病患者の膵外分泌機能不全のスクリーニング// Am JGastroenterol。 2003年12月 巻 98(12)。 R.2672-2675。
26.永井正明、翔正明、佐藤聡、豊川秀樹ほか 膵頭十二指腸切除術後の非アルコール性脂肪肝疾患に対するパンクレリパーゼの効果// J肝胆道膵科学。 2014年3月 巻 21(3)。 R.186-192。
27. Bueverov A.O.、Yeshau V.S.、Mayevskaya M.V.、Ivashkin V.T. 脂肪性肝炎の複雑な治療に不可欠なリン脂質// Clin。 視点。 胃腸。 とヘパトール。 2012. No. 1. P.27-34。
28.ミヌーシュキンO.N. 必須リン脂質による肝疾患の治療経験// ConsiliumMedicum。 追加リリース。 2001年、p。 9-11。
29. Podymova S. D. アルコール性肝疾患の治療における必須リン脂質の病因的役割// ConsiliumMedicum。 追加リリース。 2001年、p。 3-5。
30. KurtzE。肝臓学に不可欠なリン脂質-50年間の実験的および臨床的実験//消化器。 1991.Vol。 29.補足 2.P.7-13。
31. Drapkina O.M.、Korneeva O.N.、Ivashkin V.T. メタボリックシンドロームにおける非アルコール性脂肪性肝炎の治療:必須のリン脂質に焦点を当てる//主治医。 2010. No. 2. S.18-24。
32. A.V.カリーニン。 Essentiale forteN-アルコール性肝疾患に薬を使用した経験// ConsiliumMedicum。 追加リリース。 2001年。
33. Shulpekova Yu.O. アルコール性肝疾患:チャールズS.リーバーの注目に値する研究に基づいて// RMJ。 2010. No. 13. S.815-818。
34.サムソノフA.A. 消化不良障害の矯正における基本的な要素としての胎児//紀元前。 2013. No. 13. S.685-690。