عدوى فيروس الهربس. تكاثر فيروس الهربس البسيط
يعد الفيروس شكلًا خاصًا من أشكال الحياة لا يمتلك جهازًا خاصًا به للتكاثر ، لذلك تخترق الجزيئات الفيروسية الخلية المضيفة وتستخدم قدراتها وأجهزتها للتكاثر.
خارج الخلية ، يمكن مقارنة الفيروس بشريط كاسيت ملقى على حافة النافذة: يتم تسجيل بعض المعلومات على الشريط ، لكن لا يمكنك سماع الموسيقى. عندما يكون الكاسيت على حافة النافذة ، لا يحدث شيء له. لا يمكن نسخ شريط صوتي أو تشغيله بمفرده ؛ يلزم وجود مسجل شريط لهذا الغرض. وبالمثل ، لا يمكن للفيروس أن يتكاثر خارج الخلية ؛ علاوة على ذلك ، لا تحدث عمليات أيضية فيه: فهو لا يحتاج إلى التنفس أو الشرب أو الأكل.
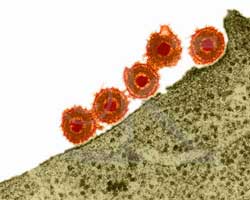
تكاثر الفيروس الهربس البسيطيتم تنفيذها على عدة مراحل متتالية ، لتحل محل بعضها البعض. في المرحلة الأولى ، "يلتصق" الفيروس (يتم امتصاصه) بالخلية المضيفة ، ثم
يدخل ، "ويتخلص من ملابسه" (قذائف خارجية). ثم يدخل إلى نواة الخلية ، حيث يتم تصنيع فيروس جديد. تشغيل المرحلة الأخيرةالفيروس يغادر الخلية.
بعد الجماع أو الجنس الفموي ، تدخل الفيروسات عدد كبيرالحصول على الأغشية المخاطية أو جلدالشريك الجنسي غير المصاب. تصطدم العديد من الجزيئات الفيروسية بالخلايا الظهارية البشرية. في المرحلة الأولى ، يلتصق (يلتصق) جزء من الجزيئات الفيروسية بالغشاء الخارجي للخلية بمساعدة "أشواك" من البروتينات السكرية. مقابل 1000 تصادم مع خلية ، فقط في حالة واحدة يلتصق الفيروس بغلافها الخارجي. في هذه المرحلة ، والتي تسمى "مرحلة الالتصاق العكسي" ، لا يزال من الممكن للفيروس أن ينفصل عن الغشاء الخارجي للخلية.
تدريجيًا ، يندمج الغلاف الخارجي للفيروس مع غشاء الخلية ، مما يغير بنية سطحه.
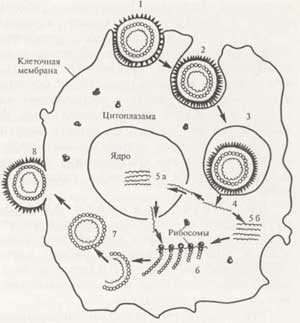
شكل "مراحل تكاثر الفيروس (رسم بياني)".
1 - امتزاز الفيروس على الخلية ؛
2 - تغلغل الفيروس في الخلية ؛
3 - فيروس داخل فجوة الخلية ؛
4 - "نزع ملابس" الفيروس ؛
5 - تكاثر الحمض النووي الفيروسي في نواة الخلية (أ)
6 - تركيب البروتينات الفيروسية على ريبوسومات الخلية ؛
7 - تكوين الفيروس.
8- خروج الفيروس من الخلية عن طريق التبرعم.
ويقوم الفيروس "بخلع ملابسه" متخلصا من الأغشية الواقية التي لا يحتاجها داخل الخلية. بقي قفيصة واحدة فقط من 20 وجهًا على الحمض النووي الفيروسي.
ثم يتشكل حول الفيروس المحقون في الخلية فقاعة صغيرة- فجوة عصارية. ينتقل الفيروس في هذه الحويصلة إلى نواة الخلية. يتصل الكابسيد بنواة الخلية. يذوب جزءًا من غشاء نواة الخلية والحمض النووي الفيروسي داخل النواة.
بعد ساعتين من دخول الفيروس إلى الخلية ، يمنع الحمض النووي الفيروسي إنتاج الحمض النووي الخاص به في نواة الخلية ويجبر الخلية على إنتاج الحمض النووي للفيروس.
في غضون 7-9 ساعات ، تتراكم نواة الخلية الحمض النووي الفيروسي. يتكون قفيصة الفيروس هنا أيضًا. تم تدمير هياكل النواة. بعد 9 ساعات من بداية لحظة تخليق الحمض النووي الفيروسي ، تترك الفيروسات النواة في سيتوبلازم الخلية. هنا ، باستخدام الغشاء النووي وغشاء الخلية ، يكتسبون غلافًا خارجيًا - كبسولة فائقة.
بعد 24 ساعة ، تغادر الفيروسات الخلية عن طريق التبرعم. بسبب التلف ، تمتلئ الخلية بالسوائل وتموت قريبًا.
خلية واحدة تنتج عدة ملايين من الفيروسات. من الخلية الظهارية في موقع الاختراق ، تدخل الفيروسات إلى مجرى الدم ، وتلتصق بكريات الدم الحمراء وتنتقل في جميع أنحاء الجسم بالدم.
الطريقة الثانية لنشر الفيروسات هي الألياف العصبية... من خلال الفروع الحساسة ، يدخل الفيروس إلى العصب ، حيث يخترق مع تيار السائل المحوري العصبونات الحساسة لعقد الضفيرة العجزية. في الخلايا العصبية ، يفرز الفيروس قفيصة وسوبر كابسيد و "يعيش" في الخلايا كجزيء DNA مزدوج الشريطة. في هذه الحالة ، يكون الجهاز المناعي غير قادر على اكتشاف الفيروس وإزالته من الجسم.
في حالة العوامل الخارجية: الكحول ، الإجهاد ، الصدمة ، المرض الذي يؤدي إلى انخفاض المناعة ، يبدأ الفيروس في التكاثر في العقد العجزية وينجرف نحو الأعضاء التناسلية بتيار من السائل المحوري. حيث تتكرر العدوى في الخلايا الظهارية.
المصادر: مخطط تكاثر الفيروسات مستعار من كتاب علم الأحياء الدقيقة من قبل فوروبييف وبيكوف وباشكوف وريباكوفا إم ، "الطب" 1994 ، ص 47
جامعة البحوث الطبية.
NI بيروجوفا
وزارة الصحة والتنمية الاجتماعية في روسيا
قسم الأحياء الدقيقة والفيروسات
رئيس القسم– كفرسكايا لودميلا إيفانوفنا
ملخص عن موضوع "الحلأ البسيط"
أكمله طالب المجموعة 244
كولباكوف ديمتري
تحقق من قبل المعلم:
خاريتونوف أناتولي أركاديفيتش
موسكو 2013
1) الوضع التصنيفي - عائلة الجنس ، الأنواع 2) علم التشكل ؛ 3) تكاثر فيروسات الهربس 4) خصائص الأنتيجين. 5) التسبب. 6) التشخيص 7) العلاج 8) المناعة
1) الوضع التصنيفي - جنس الأسرة ، الأنواع
الهربس البسيط ، عائلة الهربس ، فصيلة ألفا هيربسفيريداي ، جنس الفيروس البسيط ، أنواع HHP 1 و 2
2) الصرف.
حمض نووي كبير يحتوي على فيروسات. حجم الفيريون هو 150-200 نانومتر. يحتوي الفيروس على قفيصة مكونة من 162 كبسولة ، بالإضافة إلى كبسولة فائقة. يحتوي الكابسيد على دنا خطي مزدوج الشريطة يحتوي على حوالي 80 جينًا. نوع التناظر مكعب.
يتم زراعتها في مزارع الخلايا الحية وتسبب تعدد النوى. حساس للحرارة ، سريع التعطيل بواسطة المطهرات فوق البنفسجية.
3) تكاثر فيروسات الهربس
ترتبط الاختلافات الرئيسية بين الدورة التناسلية لفيروسات الهربس من فيروسات الحمض النووي الأخرى بهيكل جينوم أكثر تعقيدًا. يتم امتصاص الفيروسات على الخلايا من خلال مستقبلات محددة. بعد التفاعل مع المستقبلات ، يندمج الغلاف الفيروسي مع غشاء الخلية ، ويتم إطلاق nucleocapsid في السيتوبلازم. يحدث تجريد (نزع البروتين) من الجينوم الفيروسي عند الغشاء النووي ، ويتم احتجاز الحمض النووي الفيروسي في نواة الخلية المضيفة. يشمل التكاثر المراحل المبكرة والمتأخرة ، لكن لم يتم تحديدها بوضوح. المرحلة المبكرة من تكاثر فيروس الهربس. في مرحلة مبكرة ، يتم تصنيع "البروتينات المبكرة" ، وترميزها بواسطة الثلث القريب من جزيء الحمض النووي. إنها تعرض خصائص تنظيمية ، بما في ذلك تنشيط نسخ مناطق أخرى من الجينوم الفيروسي الذي يشفر بوليميريز الحمض النووي والبروتينات المرتبطة بالحمض النووي. المرحلة المتأخرة من تكاثر فيروس الهربس. في المرحلة المتأخرة ، يؤدي بوليميراز الحمض النووي الفيروسي إلى تكرار الحمض النووي للأم. نتيجة لذلك ، تتشكل جزيئات الحمض النووي للسكان البنات. تتم قراءة جزء من DNA الابنة بواسطة polymerases الخلوية ، مما يؤدي إلى نسخ الجينات الطرفية التي تشفر البروتينات الهيكلية (بروتينات الغلاف والبروتينات السكرية للأشواك). يتم تجميع المجموعات البنت من فيروسات الهربس في النواة ، حيث تحيط بروتينات القفيصة بجزيئات الحمض النووي ، مكونة نوكليوكابسيدات. المرحلة الأخيرة من تشكل فيروس الهربس هي تكوين قفاز فائق على السطح الداخلي للغشاء النووي. تتبرعم الأبناء الناضجة من الغشاء النووي المعدل ، وتنتقل عبر السيتوبلازم ، وتفرز.
4) خصائص الأنتيجين.
يتم تمثيل المستضدات الخاصة بالنوع بواسطة البروتينات السكرية القفيصة ، والتي على أساسها يتم عزل نوعين من الفيروسات: HSV-1 و HSV-2... يتم تمثيل المستضدات الخاصة بالمجموعة بواسطة البروتينات النووية. السطح glycoprotein gpC خاص بالمجموعة ، والبروتينات السكرية السطحية gpB ، gpD خاصة بالنوع.
5) التسبب.
فيروس الهربس غير قادر على اختراق الطبقة القرنية السليمة للجلد ، بسبب عدم وجود مستقبلات محددة عليه. ينتقل الهربس عن طريق التلامس المباشر مع المناطق المتضررة من الجلد أو السوائل البيولوجية للشخص المصاب. ينتقل فيروس HSV-2 حصريًا عن طريق الجلد (عبر الجلد).
يندمج الغلاف الخارجي للفيروس مع غشاء الخلية. علاوة على ذلك ، فإن nucleocapsid الفيروسي موجود في البلازما العصبية ، حيث يحدث إطلاق الحمض النووي الفيروسي. ثم يتم نقله على طول تشعبات النهايات العصبية إلى جسم خلية عصبية حساسة ، تقع في العقدة الحسية ، حيث يتم تضمينها في جهازها الوراثي إلى الأبد. بعد تغلغل الفيروس ، تبدأ عملية التكاثر النشط في الخلية - الثبات. مع الآفات الشفوية ، يكون استمرار الفيروس مميزًا في الخلايا العصبية للعقد الحساسة للعصب ثلاثي التوائم ، والآفات التناسلية ، القطنية.
في معظم الناس ، يكون تكاثر الفيروس وإفرازه بعد الإصابة مباشرة بدون أعراض. يمكن أن يحدث هذا قبل أكثر من أسبوع أو بعد ظهور الأعراض الأولى في 50٪ من الحالات. يتكاثر العامل المسبب بشكل مكثف فيه ، مما يؤدي إلى إطلاق نوع من العدوى المثمرة. يحدث التنكس البؤري للظهارة: تزداد الخلايا في الحجم ، ثم تموت ، وتشكل بؤر النخر.
تمتلك فيروسات الهربس فترات نشاط دورية (تتكون فقاعات تحتوي على جزيئات فيروسية في غضون 2-21 يومًا) وفترات مغفرة تختفي خلالها القروح. عادة ما يكون الهربس التناسلي (HSV-2) بدون أعراض ، على الرغم من أن الفيروس يتكاثر ويمكن أن ينتقل إلى أشخاص آخرين. هذا هو الأكثر شيوعًا مع فيروس HSV-2. لا يتم تحديد انتكاسات المرض في الوقت المناسب ، على الرغم من تحديد بعض مسببات المرض. تشمل هذه العوامل تأثيرات مثبطات المناعة ( انظر أدناه). مع الانتكاس ، يتم تنشيط الفيروس ، الذي هو في مرحلة كامنة ، مما يؤدي إلى تكوين العديد من الجسيمات المعدية التي تتحرك على طول عمليات الخلايا العصبية ، والتي تنتقل منها بعد ذلك إلى ظهارة الجلد والأغشية المخاطية. غالبًا ما تظهر الحويصلات ، مصحوبة بأضرار نخرية في الظهارة. دورة تكاثر الفيروس 10 ساعات. بمرور الوقت ، يطور الجسم مناعة مضادة للفيروسات ويقل تواتر وشدة الانتكاسات.
غالبًا ما يستمر النقل خلال الأشهر الـ 12 الأولى بعد الإصابة. مدة هذا الناقل مع نقص المناعة (على سبيل المثال ، مع عدوى فيروس نقص المناعة البشرية) أكثر. بمجرد الإصابة بالعدوى ، يبدأ الجسم في تصنيع الأجسام المضادة ضد فيروس HSV المحدد ، مما يمنع العدوى من الانتشار. في حالة الإصابة بفيروس HSV-1 ، فإن هذا التحول المصلي (إنتاج الأجسام المضادة) سيحمي الجسم من العمليات المعدية الأخرى التي يسببها هذا الفيروس ، مثل الهربس التناسلي والتهاب القرنية الهربسي والباناريتيوم.
الأجسام المضادة التي يتم إنتاجها بعد الأولي عدوى الهربسمنع العدوى بنفس النوع من الفيروسات: الأشخاص الذين أصيبوا بفيروس الهربس الفموي HSV-1 ليس لديهم الباناريتيوم أو الهربس التناسلي الذي يسببه HSV-1.
في الزواج الأحادي ، تكون المرأة السالبية المصلية معرضة لخطر العدوى من رجل إيجابي المصل بنسبة تزيد عن 30٪ في السنة. خلال الإصابة الأولى بالفم ، سيستغرق إنتاج الأجسام المضادة الواقية 6 أسابيع ، وبعدها ستكون المناعة الخلطية قادرة على حماية الجسم من العدوى التناسلية المتكررة.
6) التشخيص
الطريقة المصلية.لا تميز الطريقة المصلية مع IgM بين الأجسام المضادة لأنواع الفيروسات HSV-1 و HSV-2. ومع ذلك ، فإن اختبار HSV الجديد الخاص بنقطة مناعية للبروتين السكري يوفر أكثر من 98 ٪ خصوصية ، وبالتالي يسمح بتمييز أنواع الهربس HSV-1 و HSV-2. يعتقد بعض الأطباء الأجانب أنه سيتم استبدال اختبار IgM قريبًا بآخر جديد.
الطريقة الخلوية.في تجريف المنطقة المصابة من الظهارة ، الملطخة وفقًا لـ Romanovsky - Giemsa ، توجد خلايا متعددة النوى مع شوائب داخل الخلايا.
الطريقة الفيروسية.تُصاب المزارع الخلوية بالعدوى ويتم الكشف عن الإجراء المرضي الخلوي (CPE) في شكل خلايا عملاقة متعددة النوى مع شوائب يتم تدميرها. يتم تحديد الهوية في تفاعل تحييد CPP ، الشعاب المرجانيةمع الأجسام المضادة وحيدة النسيلة. تتكون لويحات بيضاء على الغشاء المشيمي لأجنة الدجاج بعد 2-3 أيام.
الطريقة البيولوجية.عندما يتم تطبيق مادة فيروسية على خدش قرنية الأرانب ، يحدث التهاب القرنية ، ويحدث التهاب الدماغ في دماغ الفئران حديثي الولادة.
طريقة التألق المناعي ، اختبار حساسية الجلد ، تفاعل البوليميراز المتسلسل
7) العلاج
في الوقت الحالي ، لا توجد طريقة لإزالة الفيروس من الجسم. تقلل الأدوية المضادة للفيروسات فقط من تكرار الانتكاسات ومدتها وشدتها. المسكنات مثل الإيبوبروفين والباراسيتامول تقلل الألم والحمى فقط. كما أن أدوية التخدير الموضعية مثل بريلوكائين أو ليدوكائين أو بنزوكائين أو تتراكائين تخفف الحكة والألم.
فعال ضد التهابات الهربس: اسيكلوفير ، فالاسيكلوفير ، فامسيكلوفير ، بنسيكلوفير. كان الأسيكلوفير أول ما تم اكتشافه ، وهناك العديد من الجينات.
ثبت أن الأسيكلوفير وفالاسيكلوفير فعالان في علاج هربس الوجه (الشفاه) ، بما في ذلك مرضى السرطان. الأدلة التي تدعم استخدام الأسيكلوفير في علاج التهاب اللثة والفم الهربسي الأولي أقل قوة.
8) الحصانة
مع العدوى الأولية ، تتشكل الأجسام المضادة IgM ، مع الانتكاسات - IgG و IgA. بسبب استمرار الفيروس في الأشخاص المصابين ، فإن المناعة غير عقيمة ومؤقتة - مع انخفاض في المناعة ، خاصة مع نقص الخلايا القاتلة الطبيعية (NK) ، يحدث الانتكاس. بالإضافة إلى ذلك ، فإن فيروس الهربس نفسه قادر على إحداث نقص المناعة ، وإحدى آلياته تحفيز تخليق الأجسام المضادة IgG "غير الفعالة" ، التي تثبط المناعة وتثبط NK. في الأشخاص المقاومين للعدوى ، يتم ممارسة المناعة عن طريق نظام الإنترفيرون ، والخلايا القاتلة الطبيعية والخلايا التائية القاتلة ، وكذلك الأجسام المضادة لـ sIgA. 80-90٪ من البالغين لديهم أجسام مضادة IgG لـ HSV-1. يؤثر مستوى المناعة بشكل كبير على عدد وشدة الانتكاسات.
في السنوات الأخيرة ، أصبحت فيروسات الهربس (من الهربس اليوناني - الزاحف) ذات أهمية متزايدة في علم الأمراض المعدية. يرتبط الاهتمام الذي أظهره علماء الفيروسات والأطباء في السنوات الخمس والعشرين الماضية بأمراض فيروس الهربس البشري بدورها الوبائي الهام وأهميتها الاجتماعية في العالم الحديث... تتطلب الزيادة المطردة في عدد أمراض الهربس لدى البالغين والأطفال دراسة شاملة لعدوى الهربس وتطوير طرق فعالة للوقاية والعلاج من مختلف أشكال هذه العدوى. من بين عدوى فيروسيةيحتل الهربس أحد الأماكن الرائدة بسبب انتشار الفيروسات في كل مكان ، ومجموعة متنوعة من المظاهر السريرية ، كقاعدة عامة ، الدورة المزمنة ، بالإضافة إلى الطرق المختلفة لانتقال الفيروسات.
وهي تُصنف من بين أكثر أنواع العدوى البشرية شيوعًا والتي يتم التحكم فيها بشكل سيئ. يمكن لفيروسات الهربس أن تنتشر بدون أعراض في أجسام ذات جهاز مناعة طبيعي ، ولكنها تسبب أمراضًا خطيرة ومميتة للأشخاص الذين يعانون من كبت المناعة. وفقا لمنظمة الصحة العالمية ، والوفيات من عدوى الهربس بين أمراض فيروسيةفي المرتبة الثانية (15.8٪) بعد التهاب الكبد (35.8٪).
يتم دمج فيروسات الهربس في عائلة كبيرة الهربسوهو حاليًا الأكثر تصنيفًا بشكل واضح. أسرة الهربسيضم أكثر من 80 ممثلاً ، 8 منهم أكثر مسببات الأمراض للإنسان (فيروس الهربس البشري - HHV). تنقسم فيروسات الهربس - وهي عائلة قديمة نسبيًا من فيروسات الحمض النووي الكبيرة - إلى 3 فصائل فرعية اعتمادًا على نوع الخلايا التي تحدث فيها العملية المعدية ، وطبيعة تكاثر الفيروس ، وبنية الجينوم ، والسمات البيولوجية الجزيئية والمناعية: α ، و γ ( ، وفقًا لـ N.G. Perminov ، IV Timofeeva وآخرون ، مركز أبحاث الدولة لعلم الفيروسات والتكنولوجيا الحيوية).
تتميز فيروسات α-herpes ، بما في ذلك HSV-1 و HSV-2 و VZV ، بالتكاثر الفيروسي السريع والعمل الخلوي على مزارع الخلايا المصابة. يحدث تكاثر فيروسات α-herpes في أنواع مختلفةالخلايا ، يمكن للفيروسات أن تبقى في شكل كامن ، وخاصة في العقد.
فيروسات β-herpes هي خاصة بالأنواع ، تصيب أنواع مختلفةالخلايا التي يزيد حجمها (تضخم الخلايا) يمكن أن تسبب حالات مثبطة للمناعة. يمكن أن تأخذ العدوى شكلاً معممًا أو كامنًا ؛ تحدث العدوى المستمرة بسهولة في ثقافة الخلية. تشمل هذه المجموعة CMV و HHV-6 و HHV-7.
تتميز فيروسات γ-herpes بالتداريب للخلايا الليمفاوية (T- و B-lymphocytes) ، حيث تستمر لفترة طويلة ويمكن أن تتحول ، مسببة الأورام اللمفاوية ، الأورام اللحمية. تشمل هذه المجموعة فيروس Epstein-Barr و HHV-8-herpes ، وهو فيروس مرتبط بساركوما كابوزي (KSHV). KSHV هو الأقرب في التنظيم الجيني لفيروس Simiri herpes simplex simplex (HVS) في الخلية التائية المدارية.
ترتبط فيروسات الهربس بالأورام الخبيثة وهي قادرة (على الأقل من EBV و HVS) على تحويل الخلايا في المختبر. تتشابه جميع فيروسات الهربس في الخصائص المورفولوجية ، والحجم ، ونوع الحمض النووي (DNA مزدوج الشريطة) ، وقفيصة الأيكوساديلتاهيدرال ، والتي يحدث تجميعها في نواة الخلية المصابة ، والمغلف ، ونوع التكاثر ، والقدرة على التسبب في مزمن. والعدوى الكامنة في البشر.
يحدث استنساخ فيروسات الهربس وفقًا للمخطط التالي: الامتزاز العشوائي التلقائي للفيروس "الأم" الأصلي على سطح الخلية المستهدفة ، "نزع الملابس عن الفيروس" - انقسام الغلاف والقفيصة ، تسلل الحمض النووي الفيروسي إلى نواة الخلية المستهدفة ، تكوين ونضوج فيريونات "ابنة" من خلال التبرعم على الغشاء النووي. بعد إصابة الخلية ، على سبيل المثال بفيروس الهربس البسيط من نوع أو نوعين ، يبدأ تخليق البروتينات الفيروسية الجديدة في غضون ساعتين ، ويصل عددها إلى الحد الأقصى في حوالي 8 ساعات. أثناء نضوج فيريونات "الابنة" ، تتشكل أغشية الكبسولات والحمض النووي من تلك المتوفرة داخل الخلايا المصابة من الأحماض الأمينية والبروتينات والبروتينات الدهنية والنيوكليوسيدات. تدخل هذه الجزيئات الخلية المصابة من الفراغات الخلالية حيث يتم استنفاد الاحتياطيات داخل الخلايا. في هذا الصدد ، تعتمد الفيروسات على شدة التمثيل الغذائي داخل الخلايا ، والتي بدورها تحددها طبيعة الخلية المستهدفة. وبالتالي ، فإن أعلى معدل استقلاب هو سمة من سمات الخلايا قصيرة العمر من النوع الظهاري فيروسات الهربستستعمر بشكل خاص خلايا الظهارة والأغشية المخاطية والدم والأنسجة اللمفاوية. تكون الفيروسات المعدية "الابنة" كاملة وجاهزة للتكاثر النشط اللاحق ، وتظهر داخل الخلية المصابة بعد 10 ساعات ، ويصبح عددها بحد أقصى بعد حوالي 15 ساعة. ويؤثر عدد الفيروسات إلى حد ما على معدل انتشار العدوى ومعدل انتشار العدوى. منطقة الآفة.
يبدأ الجيل الأول من فيروسات الهربس "الابنة" بالدخول إلى البيئة (الفراغات بين الخلايا ، والدم ، والليمفاوية والوسائط البيولوجية الأخرى) بعد حوالي 18 ساعة. ويمكن ملاحظة ذلك في الممارسة السريرية مع العمليات غير المنضبط (على سبيل المثال ، مع جدري الماء ، والهربس النطاقي ، التعميم عدوى الفيروس المضخم للخلايا) - تظهر عناصر من الطفح الجلدي الهربسي على الجلد أو الأغشية المخاطية على شكل موجات. في الحالة الحرة ، تكون فيروسات الهربس لفترة قصيرة جدًا (من 1 إلى 4 ساعات) - هذه هي المدة المميزة لهذه الفترة تسمم حادمع الالتهابات الفيروسية. يبلغ متوسط العمر الافتراضي لكل جيل من فيروسات الهربس المتكونة والممتزة 3 أيام.
من الناحية الوبائية ، فإن المعلومات التالية حول فيروسات الهربس هي الأكثر إثارة للاهتمام: الفيروسات شديدة القابلية للحرارة - يتم تعطيلها عند درجة حرارة 50-52 درجة مئوية لمدة 30 دقيقة ، عند درجة حرارة 37.5 درجة مئوية - في غضون 20 ساعة ، تكون مستقرة عند درجة حرارة 70 درجة مئوية ؛ يتحمل التجفيف جيدًا ، ويستمر لفترة طويلة في الأنسجة في محلول الجلسرين بنسبة 50 ٪. على الأسطح المعدنية (العملات المعدنية ، ومقابض الأبواب ، وصنابير المياه) ، تعيش فيروسات الهربس لمدة ساعتين ، على البلاستيك والخشب - حتى 3 ساعات ، في القطن الطبي الرطب والشاش - حتى تجف في درجة حرارة الغرفة (حتى 6 ساعات).
الخصائص البيولوجية الفريدة لجميع فيروسات الهربس البشرية هي انتفاخ الأنسجة ، والقدرة على الاستمرار والكمون في جسم الشخص المصاب. الثبات هو قدرة فيروسات الهربس على التكاثر المستمر أو الدوري (التكاثر) في الخلايا المصابة للأنسجة الاستوائية ، مما يخلق تهديدًا دائمًا لتطور العملية المعدية. الكمون لفيروسات الهربس هو الحفاظ على الفيروسات مدى الحياة في شكل معدل شكليًا وكيميائيًا مناعيًا في الخلايا العصبية للعقد الإقليمية (فيما يتعلق بمكان إدخال فيروس الهربس) من الأعصاب الحسية. تتمتع سلالات فيروسات الهربس بقدرة غير متكافئة على المثابرة والكمون والحساسية للأدوية المضادة للهربس بسبب خصائص أنظمة الإنزيم الخاصة بها. لكل فيروس من فيروس الهربس معدل الثبات والكمون الخاص به. من بين الذين تمت دراستهم ، كانت فيروسات الهربس البسيط الأكثر نشاطًا في هذا الصدد ، وأقلها نشاطًا هو فيروس Epstein-Barr.
وفقًا لدراسات عديدة ، بحلول سن 18 عامًا ، يصاب أكثر من 90 ٪ من سكان الحضر بسلالة واحدة أو أكثر من 7 فيروسات هربس مهمة سريريًا على الأقل (نوع الهربس البسيط 1 و 2 ، الحماق النطاقي ، الفيروس المضخم للخلايا ، إبشتاين بار ، أنواع الهربس البشري 6 و 8). في معظم الحالات ، تحدث العدوى الأولية وإعادة العدوى عن طريق الرذاذ المحمول بالهواء ، أو من خلال الاتصال المباشر أو من خلال مستلزمات المنزل والنظافة (المناشف المشتركة ، والمناديل ، وما إلى ذلك). كما تم إثبات طرق انتقال العدوى عن طريق الفم ، والأعضاء التناسلية ، والتناسلية ، ونقل الدم ، والزرع ، وطرق المشيمة.
تنتشر عدوى الهربس الفيروسية في العالم وتميل إلى النمو باطراد. تتمثل إحدى سمات عدوى فيروس الهربس في إمكانية إشراك العديد من الأجهزة والأنظمة في العملية المعدية ، وهو ما يفسر مجموعة متنوعة من الأمراض التي تسببها فيروسات الهربس ، والتي تتراوح من العدوى الجلدية المخاطية البسيطة إلى العدوى المعممة التي تهدد الحياة. من الخصائص المهمة لفيروسات الهربس القدرة ، بعد الإصابة الأولية ، على مرحلة الطفولةتستمر مدى الحياة في الجسم وتنشط تحت تأثير عوامل استفزاز خارجية وداخلية مختلفة.
يصاحب العدوى البشرية بفيروس الهربس المشار إليه أعراض مرضيةالحادة المناسبة الأمراض المعديةفي المتوسط ، لا يزيد عدد الأشخاص عن 50٪ ، وخاصة عند الأطفال: حمامي مفاجئ (فيروس الهربس البشري من النوع 6) ، التهاب الفم القلاعي (فيروسات الهربس البسيط نوع أو نوعان) ، جدري الماء (فيروس الحماق النطاقي) ، كريات الدم البيضاء المعدية (فيروس ابشتاين - بار) ، متلازمة شبيهة بعدد كريات الدم البيضاء (الفيروس المضخم للخلايا). في مرضى آخرين ، تكون العدوى بدون أعراض ، وهو أمر نموذجي بشكل خاص للمراهقين والبالغين. بالإضافة إلى الخصائص البيولوجية لسلالة فيروس الهربس ، فإن الخصائص الفردية (المرتبطة بالعمر ، والجنسية ، والتطور ، والورم السرطاني) للاستجابة المناعية للشخص المصاب للعديد من مستضدات الفيروس لها تأثير على مسار الحادة و أمراض الهربس الفيروسية المتكررة.
في كثير من الأحيان ، خاصةً مع انخفاض نشاط المناعة في الجسم ، تعمل فيروسات الهربس كفيروسات انتهازية ، مما يؤدي إلى المزيد من الشدة ، مع الاعراض المتلازمة، مسار المرض الأساسي. تعد فيروسات الهربس البسيط من النوعين 1 و 2 ، وكذلك CMV من بين العوامل المسببة لعدوى TORCH. يلعبون دورًا مهمًا في انتهاك الوظيفة الإنجابية للإنسان ، وتطور الأمراض الخطيرة للأم والجنين وحديثي الولادة والأطفال الصغار.
تعتبر الأمراض التي تسببها فيروسات HSV و CMV و EBV من مؤشرات الإيدز نظرًا لاكتشافها المتكرر في هذه الحالة المرضية. في عام 1988 ، تم تضمينهم في التعريف الموسع لحالات الإيدز. تشير نتائج الدراسات الحديثة إلى دور بعض فيروسات الهربس (HHV-8 ، CMV ، EBV ، إلخ) في تطوير عدد من فيروسات الهربس. الأورام الخبيثة: سرطان البلعوم الأنفي ، ورم الغدد الليمفاوية بوركيت ، ورم الغدد الليمفاوية للخلايا البائية ، وسرطان الثدي ، وسرطان غدي في الأمعاء والبروستاتا ، وسرطان قناة عنق الرحم في عنق الرحم ، وساركوما كابوزي ، وورم الخلايا البدائية العصبية ، إلخ.
يتمثل الخطر الأكبر على الصحة في العدوى العصبية الهربسية (تصل نسبة الوفيات إلى 20٪ ، وتبلغ نسبة الإعاقة 50٪) ، والهربس العيني (في نصف المرضى تقريبًا يؤدي إلى الإصابة بإعتام عدسة العين أو الجلوكوما) والهربس التناسلي.
على ما يبدو ، يمكن أن تتكرر جميع عدوى فيروس الهربس المعروفة ، ومع ذلك ، تختلف عتبة وأسباب تحول الشكل الحاد إلى شكل متكرر لكل نوع من أنواع فيروس الهربس. بشكل عام ، تأخذ العدوى الفيروسية الهربس مسارًا متكررًا في ما لا يزيد عن 8-20 ٪ من المرضى. يمكن أن يُنظر إلى أمراض الهربس الفيروسية المتكررة لدى بعض الأشخاص على أنها "مزمنة" عندما تتطور على مدى سنوات عديدة ، ولا تدمر الصحة البدنية ووظائف الأجهزة الحيوية فحسب ، بل تؤثر أيضًا بشكل سلبي نفسيًا على المريض. لذلك ، لأغراض عملية ، يتم تصنيف الالتهابات الفيروسية للهربس مع مراعاة توطين العملية وتكرارها ومسبباتها ( ).
أسباب المسار المتكرر للعدوى الفيروسية الهربس متعددة. أحدها هو أن تحول عملية فيروسية هربس حادة إلى عملية مزمنة يحدث "بتواطؤ" واضح الجهاز المناعي... إذا كان من السهل تفسير نقص المناعة المكتسب نتيجة العلاج الكيميائي أو عدوى فيروس العوز المناعي البشري ، فإن كل المحاولات لمعرفة أسباب الخلل الرئيسي في الاستجابة المناعية لدى الأشخاص الأصحاء مناعياً المصابين بعدوى فيروس الهربس المتكررة لم تنجح. سبب آخر هو ، على ما يبدو ، في السمات الكمية والنوعية لاستمرار ووقت انتقال سلالة معينة من فيروس الهربس في جسم المريض.
تشخيص عدوى الهربس
تستند جميع طرق الكشف عن الفيروسات والتعرف عليها إلى المبادئ التالية:
- الكشف عن الفيروس في حد ذاته (الفحص المجهري الإلكتروني) ؛
- الكشف عن الفيروسات والتعرف عليها عن طريق الخلايا التي تتفاعل معها (تراكم الفيروسات في الخلايا الحساسة لها) ؛
- الكشف عن الفيروسات والتعرف عليها باستخدام الأجسام المضادة (MFA ، ELISA ، RAL ، IB ، RN ، RSK) ؛
- كشف وتحديد الأحماض النووية (PCR ، MG).
الفحص المجهري الإلكتروني: يسمح التشخيص السريع باكتشاف التهاب الغدد العرقية المقيّح أو مكوناته مباشرة في العينات المأخوذة من المريض وإعطاء استجابة سريعة بعد بضع ساعات. تم الكشف عن العامل الممرض باستخدام المجهر الإلكتروني للمواد السريرية ذات التباين السلبي.
تعتبر الطرق المصلية أقل شأنا من حيث المحتوى المعلوماتي والحساسية للطرق الأخرى التشخيص المختبريولا تسمح بتحديد مسببات هذا الشكل أو ذاك من المرض بدرجة كافية من اليقين. تحدث زيادة في عيار الأجسام المضادة
الخامس مواعيد متأخرة(عدة أسابيع) بعد الإصابة بالفيروس أو إعادة تنشيطه ، وفي الوقت نفسه ، قد لا يتم ملاحظته في الأشخاص الذين يعانون من نقص المناعة. لإنشاء زيادة بمقدار 4 أضعاف في عيار الأجسام المضادة للعدوى الفيروسية للهربس (مؤشر على الإصابة الأولية) ، من الضروري دراسة الأمصال المزدوجة. التفاعلات المصلية (RSK ، RN) لها نوعية عالية ، ولكن حساسية منخفضة نسبيًا ، وعلاوة على ذلك ، يصعب تنفيذها.
تلقت طريقة التألق المناعي ، ELISA ، RAL ، IB تطبيقًا عمليًا واسعًا.
الطريقة الأكثر دقة لتشخيص العدوى الفيروسية هي عزل الفيروس من مزارع الخلايا المختلفة.
تستخدم الطرق البيولوجية الجزيئية للكشف عن فيروس الهربس: البوليميراز تفاعل تسلسليوتفاعل التهجين الجزيئي ، الذي يمكنه الكشف عن وجود الحمض النووي الفيروسي في مادة الاختبار. يمكن اعتبار تفاعل البوليميراز المتسلسل أكثر تفاعلات الحساسية والأسرع حساسية. تجعل حساسية الطريقة من الممكن تحديد جزيء واحد من الحمض النووي المطلوب في عينات تحتوي على 10 خلايا.
علاج عدوى الهربس
حتى الآن ، لا يزال علاج عدوى الهربس مهمة صعبة. يؤدي المسار المزمن للعملية إلى إعادة هيكلة الجهاز المناعي: تطور نقص المناعة الثانوي ، وتثبيط تفاعل المناعة الخلوية ، وانخفاض دفاع الجسم غير النوعي. على الرغم من التنوع المخدراتتستخدم لعلاج عدوى الهربس ، أدويةتوفير علاج كاملمن الهربس غير موجود. عدوى الهربس الفيروسيةيشير إلى الأمراض التي يصعب السيطرة عليها. هذا يرجع ، أولاً وقبل كل شيء ، إلى مجموعة متنوعة من الآفات السريرية ، وتطور مقاومة الفيروس للأدوية ، ووجود التقليد الجزيئي في فيروسات الهربس. لذلك ، من أجل العلاج الناجح لعدوى الهربس ، من الضروري اختيار الصواب دواء مضاد للفيروسات، جرعته ومدة العلاج ، استخدم مزيجًا من الأدوية المختلفة. من أجل زيادة فعالية العلاج ، من الضروري أيضًا تضمين الأدوية المناعية التي تساهم في تصحيح الحالة المناعية ، وكذلك العوامل الممرضة التي تخفف من حالة المريض.
حاليًا ، يتم تقسيم جميع الأدوية المضادة للحساسية إلى 3 مجموعات رئيسية من الأدوية المضادة للفيروسات ( ).
ترتبط آلية عمل عقاقير العلاج الكيميائي (النيوكليوسيدات غير الطبيعية: فالتريكس ، فيكتافير ، فامفير ، سيميفين) بتثبيط تخليق الحمض النووي الفيروسي والتكاثر الفيروسي عن طريق التثبيط التنافسي لبوليميراز الحمض النووي الفيروسي.
في الأدوية - مناعة الأدوية (alpizarin ، imunofan ، lycopid ، polyoxidonium) بنشاط مكونات نشطةلها خصائص تحفيز المناعة فيما يتعلق بالمناعة الخلوية والخلطية ، عمليات الأكسدة والاختزال ، تخليق السيتوكين.
تجمع الأدوية المحفزة IFN (amiksin و neovir و cycloferon) بين تأثيرات التأثير الموجه للسبب والتأثير المناعي. تحفز الأدوية على تكوين IFN الذاتية (α ، ، γ) بواسطة الخلايا اللمفاوية التائية والبائية والخلايا المعوية وخلايا الكبد.
يحتل لقاح الهربس مكانة خاصة بين وسائل العلاج المضاد للفيروسات لتنشيط المناعة الخلوية ، وتصحيح المناعة في مرحلة مغفرة. التطعيم له هدفان: الوقاية من العدوى الأولية وظهور حالة من الكمون ، وكذلك الوقاية أو التخفيف من مسار المرض.
ومع ذلك ، على الرغم من وجود قائمة واسعة من الأدوية المضادة للهربس ، لا يزال الهربس عدوى سيئة السيطرة. ويرجع ذلك إلى الخصائص الوراثية للعامل الممرض ، واستمرار الفيروس على المدى الطويل في الجسم ، وتكوين سلالات مقاومة للأدوية المضادة للفيروسات. لا يمكن الحصول على التأثير السريري الأقصى إلا من خلال العلاج العقلاني المعقد للأدوية ذات آليات العمل المختلفة.
اقترحت مجموعة سانت بطرسبرغ من علماء الفيروسات وأخصائيي الأمراض المعدية ، برئاسة ف.إيساكوف ، برنامجًا للعلاج والوقاية من عدوى الهربس (الجدول 4).
فوائد العلاج المعقد للجهاز الهضمي.
- يوفر الاستخدام المشترك للعلاج الكيميائي المضاد للهربس والعوامل المناعية تأثيرًا تآزريًا.
- عن طريق تقليل جرعة مضادات HPP ، احتمالية التطور آثار جانبية، يتم تقليل التأثير السام على جسم المريض.
- يتم تقليل احتمالية ظهور سلالات مقاومة من فيروسات الهربس لهذا الدواء.
- يتم تحقيق تأثير تصحيح المناعة.
- يتم تقليل مدة الفترة الحادة للمرض ومدة العلاج.
وبالتالي ، فإن علاج الجهاز الهضمي مهمة معقدة ومتعددة المكونات.
للأسئلة الأدبية ، يرجى الاتصال بمكتب التحرير.
ت. ك. كوسكوفا ، مرشح العلوم الطبية
إي جي بيلوفا, مرشح العلوم الطبية
MGMSU ، موسكو
1. علم الفيروسات. تاريخ علم الفيروسات. تشامبرلين. RU. باستير. إيفانوفسكي.
2. تكاثر الفيروسات. تكاثر فيروسات + RNA. بيكورنا فيروسات. تكاثر فيروسات بيكورنا.
3. الفيروسات الطوعية. تكاثر فيروسات التوجا. الفيروسات القهقرية. تكاثر الفيروسات القهقرية.
4. تكاثر فيروسات الرنا. تكاثر الفيروسات باستخدام RNA مزدوج الشريطة.
5. تكاثر فيروسات الدنا. دورة النسخ المتماثل للفيروسات المحتوية على الحمض النووي. تكاثر فيروسات البابوفا. تكاثر فيروسات الغد.
7. تكاثر فيروس التهاب الكبد B. الدورة التكاثرية لفيروس التهاب الكبد B.
8. علم الوراثة من الفيروسات. توصيف التجمعات الفيروسية. تجمع الجينات للتعدادات الفيروسية.
9. الطفرات الفيروسية. الطفرات العفوية للفيروسات. الطفرات المستحثة للفيروسات. مظهر من مظاهر الطفرات الفيروسية في النمط الظاهري.
10. التفاعلات الجينية بين الفيروسات. إعادة التركيب وإعادة توزيع الجينات بالفيروسات. تبادل شظايا الجينوم بالفيروسات. التحول الأنتيجيني.
الاختلافات الرئيسية في الدورة التناسلية فيروسات الهربسمن عند فيروسات الحمض النووي الأخرىالمرتبطة بهيكل جينوم أكثر تعقيدًا. يتم امتصاص الفيروسات على الخلايا من خلال مستقبلات محددة. بعد التفاعل مع المستقبلات ، يندمج الغلاف الفيروسي مع غشاء الخلية ، ويتم إطلاق nucleocapsid في السيتوبلازم. يحدث تجريد (نزع البروتين) من الجينوم الفيروسي عند الغشاء النووي ، ويتم احتجاز الحمض النووي الفيروسي في نواة الخلية المضيفة. يشمل التكاثر المراحل المبكرة والمتأخرة ، لكن لم يتم تحديدها بوضوح.
المرحلة المبكرة من تكاثر فيروس الهربس... في مرحلة مبكرة ، يتم تصنيع "البروتينات المبكرة" ، وترميزها بواسطة الثلث القريب من جزيء الحمض النووي. إنها تعرض خصائص تنظيمية ، بما في ذلك تنشيط نسخ مناطق أخرى من الجينوم الفيروسي الذي يشفر بوليميريز الحمض النووي والبروتينات المرتبطة بالحمض النووي.
المرحلة المتأخرة من تكاثر فيروس الهربس... في المرحلة المتأخرة ، يؤدي بوليميراز الحمض النووي الفيروسي إلى تكرار الحمض النووي للأم. نتيجة لذلك ، تتشكل جزيئات الحمض النووي للسكان البنات. تتم قراءة جزء من DNA الابنة بواسطة polymerases الخلوية ، مما يؤدي إلى نسخ الجينات الطرفية التي تشفر البروتينات الهيكلية (بروتينات الغلاف والبروتينات السكرية للأشواك).
تجمع السكان بنات من فيروسات الهربسيحدث في النواة ، حيث تحيط بروتينات القفيصة بجزيئات الحمض النووي ، مكونة نوكليوكابسيدات. المرحلة الأخيرة من تشكل فيروس الهربس هي تكوين قفاز فائق على السطح الداخلي للغشاء النووي. تتبرعم الأبناء الناضجة من الغشاء النووي المعدل ، وتنتقل عبر السيتوبلازم ، وتفرز.
فيروسات الجدري. تكاثر فيروس الجدري.
فيروسات الجدريلديها الدورة التناسلية الأكثر تعقيدًا ، بينما يتم تصنيع أكثر من 100 بروتين مختلف تشكل الفيروسات (معظمها يشكل الغلاف الخارجي). يتميز تكاثر Poxvirus بالميزات التالية.
نسخ الحمض النووييبدأ قبل نزع البروتين الكامل للفيروس ، حيث يتم تنفيذه بالكامل بواسطة البوليميرات الفيروسية.
تكراريحدث فقط في السيتوبلازم وهو مستقل تمامًا عن البوليميرات الخلوية ، لأنه ، على عكس الفيروسات الأخرى ، تمتلك فيروسات الجدري بوليميريز الحمض النووي الريبي المعتمد على الحمض النووي الريبي ، والذي يقرأ أكثر من نصف الجينوم الفيروسي خلال المراحل الأولية والمراحل المبكرة.
الخامس دورة الإنجاب هناك ثلاثة المراحل - الأولي، مبكرًا ومتأخرًا.
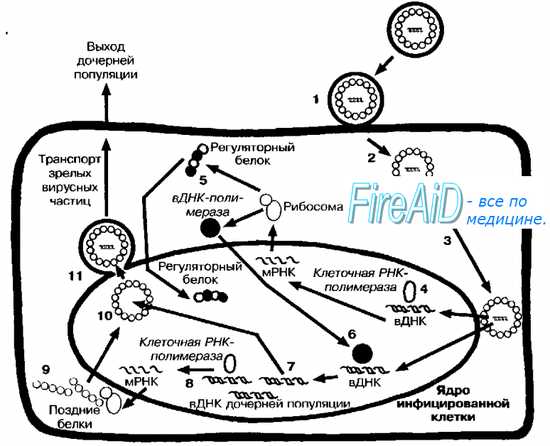 أرز. 5-4. دورة تكرار فيروسات الحمض النووي(في مثال تكاثر فيروس الهربس). بعد الامتزاز (1) ، يدخل الفيروس الخلية عن طريق الاندماج مع الغشاء (2). يتم نقل nucleocapsid إلى الغلاف النووي (3) ، ويدخل الحمض النووي الفيروسي (vDNA) إلى نواة الخلية ، حيث يبدأ نسخه بواسطة بوليميريز الحمض النووي الريبي المعتمد على الحمض النووي الخلوي (4). أولاً ، يتم نسخ "الجينات المبكرة". نتيجة لترجمة "الجزء المبكر" من الجينوم الفيروسي ، يتم تصنيع "البروتينات المبكرة" (5) ، بما في ذلك البوليمرات التنظيمية والمصفوفة والفيروسية. يدخل البوليميراز الفيروسي جينوم الخلية (6) ، حيث يبدأ تخليق جزيئات الحمض النووي للمجموعات البنت (7). يتم نسخ جزء من الحمض النووي الفيروسي ("الجينات المتأخرة") للمجموعات البنت بواسطة بوليميراز الحمض النووي الريبي الخلوي (8) ، مما يؤدي إلى تخليق "البروتينات المتأخرة" (9) اللازمة لتجميع التجمعات البنت (10). هذا الأخير يترك النواة ، من غشاءها (11) ، شظايا موجودة في غلافها.
أرز. 5-4. دورة تكرار فيروسات الحمض النووي(في مثال تكاثر فيروس الهربس). بعد الامتزاز (1) ، يدخل الفيروس الخلية عن طريق الاندماج مع الغشاء (2). يتم نقل nucleocapsid إلى الغلاف النووي (3) ، ويدخل الحمض النووي الفيروسي (vDNA) إلى نواة الخلية ، حيث يبدأ نسخه بواسطة بوليميريز الحمض النووي الريبي المعتمد على الحمض النووي الخلوي (4). أولاً ، يتم نسخ "الجينات المبكرة". نتيجة لترجمة "الجزء المبكر" من الجينوم الفيروسي ، يتم تصنيع "البروتينات المبكرة" (5) ، بما في ذلك البوليمرات التنظيمية والمصفوفة والفيروسية. يدخل البوليميراز الفيروسي جينوم الخلية (6) ، حيث يبدأ تخليق جزيئات الحمض النووي للمجموعات البنت (7). يتم نسخ جزء من الحمض النووي الفيروسي ("الجينات المتأخرة") للمجموعات البنت بواسطة بوليميراز الحمض النووي الريبي الخلوي (8) ، مما يؤدي إلى تخليق "البروتينات المتأخرة" (9) اللازمة لتجميع التجمعات البنت (10). هذا الأخير يترك النواة ، من غشاءها (11) ، شظايا موجودة في غلافها.
المرحلة الأولى من تكاثر فيروسات الجدرييبدأ فورًا بعد خلع الفيروس من الملابس وإطلاق الحمض النووي الفيروسي في السيتوبلازم.
المرحلة المبكرة من تكاثر فيروس الجدري... في هذه المرحلة ، يتم نسخ حوالي نصف الحمض النووي الفيروسي. يتم تصنيع الإنزيمات وترميزها بواسطة "جينات مبكرة" وتشارك في تكرار الحمض النووي الفيروسي. في موازاة ذلك ، تتشكل البروتينات الهيكلية بكميات صغيرة.
المرحلة المتأخرة من تكاثر فيروس الجدرييتزامن مع بداية تكرار الحمض النووي (الذي يغير آليات النسخ لقراءة النصف الثاني من الجينوم). تمنع البروتينات المنظمة ترجمة "الرنا المرسال المبكر" وتحفز تخليق البروتينات (الهيكلية) المتأخرة. يتم إجراء تجميع الفيروسات فقط في السيتوبلازم من خلال تفاعلات تخليق الغشاء. ويرافق إطلاق المجموعات الناضجة تحلل الخلايا.