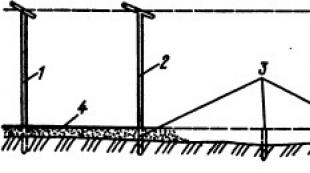
壊死の主な形態学的タイプ。 凝固壊死:説明、原因および治療。
壊死、アポトーシス、萎縮
トピックの関連性
生物学的概念としての死は、生物の生命の不可逆的な停止の表現です。 死が始まると、人は死体、死体(死体)に変わります。 法的な観点から、ほとんどの国では、脳の活動が完全かつ不可逆的に停止すると、生物は死んだと見なされます。 しかし同時に、合法的に死んだ生物の多くの細胞や組織は、死後しばらくの間生存し続けます。 これらの臓器や組織は、移植の主な供給源を構成します。
吸入経路苛性アルカリ製品は、そのほとんどが液体の形で市販されていますが、不注意または自発的に発生する可能性があります 有害な影響粘膜に 消化管穿孔のリスクに。 それらは皮膚に接触し、さまざまな程度の火傷を引き起こす可能性があります。 それらは目に接触して刺激を与える可能性があり、しばしば角膜損傷を引き起こす可能性があります。 異なる製品を混合するときにしばしば存在する蒸気は吸入される可能性があり、刺激、火傷、咳、そして時には重度の呼吸困難を伴う重度の気管支痙攣を引き起こします。
細胞死は体の生命活動の絶え間ない現れであり、健康な状態では細胞の生理学的再生とバランスが取れていることを知る必要があります。 細胞の構造要素と細胞全体の両方が摩耗し、老化し、死に、交換する必要があります。 さまざまな臓器や組織を健康な状態に維持することは、「自然な」生理学的再生なしには不可能であり、その結果、個々の細胞の死がなければ不可能です。 この細胞死は1972年に「アポトーシス」と呼ばれていました。 アポトーシスはプログラムされた細胞死です。 アポトーシスと多くの病的状態との直接的な関係は、今日ではもはや疑わしいものではありません。 アポトーシスを調節する多くの遺伝子の機能不全の研究は、これらの疾患の治療における完全に新しい方向性の開発を可能にします。 アポトーシスを調節できる薬剤の開発は、悪性腫瘍、ウイルス感染、神経系の特定の疾患、免疫不全、および自己免疫疾患の治療に新しい可能性を開きます。 例えば、悪性腫瘍やリンパ増殖性疾患ではアポトーシスを増強する必要があり、細胞損傷を特徴とする疾患ではアポトーシスを弱める必要があります。
治療:何をすべきか、何をすべきでないか-嘔吐を誘発しないでください! -医師の同意がない限り、口から何も与えないでください。 -可能であれば復元します 商標名または問題の製品の組成。 -皮膚に付着した場合は、すぐに水をたっぷりと当ててください。 -目に入った場合は、流水で数分間洗い流してください。 -刺激的な煙が発生した場合は、すぐに部屋を出てください。 -ただし、指示があれば、できるだけ早く盗難防止センターに連絡してください。
警告他のボトルに化学薬品をスプレーしないでください。 化学クリーナーは子供の手の届かないところに保管してください。 異なる製品を混ぜないでください。 化学反応は、非常に刺激性の高い煙によって引き起こされる可能性があります。 の説明と警告を読む 正しい使い方ラベルの製品。 家庭用洗剤を保管または使用しないでください。
しかし、細胞死は、外部の損傷(病原性)要因の「暴力的な」行動の結果として、生物で発生する可能性があります。 この細胞死は壊死と呼ばれます。 死んだ細胞は完全に機能を停止します。 細胞死は、不可逆的な生化学的および構造的変化を伴います。
苛性食品を飲み込むときに嘔吐すると、食道粘膜に攻撃剤が2回通過するため、状況が悪化し、損傷が大きくなります。 それはまた製品の吸収を促進することができます 気道。 ミルクは苛性活動から保護せず、嘔吐を促進する可能性があります。
家では、中に入った製品を復元する以外に何もしてはいけません。 苛性アルカリを使用する場合、疑わしいですが、特に子供では、部門に行くのが最善です 救急医療徹底的な医学的評価のために、そしておそらく適切な治療のために。
この上、 細胞死 2つの方法で発生する可能性があります。 壊死とアポトーシス。壊死とアポトーシスの生物学的兆候と重要性は異なるため、この章ではこれらのプロセスを個別に検討します。
学習の主な目標 – 壊死、アポトーシス、萎縮の主なマクロおよびミクロの兆候を認識し、それらの原因と発生メカニズムを説明し、それらを評価することができます 予想される結果そして体のためのこれらのプロセスの重要性を決定します。
コースティクスを希釈するという概念自体は間違っていませんが、特に大量の飲料水は嘔吐の一因となる可能性があります。 また、この特定のケースでは、胃の漂白剤と接触する水は塩素ガスの生成を増加させる可能性があり、それは胃を大きく膨満させる可能性があります。
組織の死は、組織または臓器の一部の破壊と死として定義され、それがなければ、必然的に生物全体の死につながります。 このプロセスは、2つのカテゴリーの病変に現れます。 組織のネロシスは、広い領域にわたる肉眼での可視性の限界から始まる、破壊された生存不能な領域によって表されます。
知る必要がある理由:
–光光学レベルと超微細構造レベルの両方で壊死とアポトーシスの特徴的な形態学的兆候を特定する。
-肉眼的徴候により、さまざまな凝固および凝固壊死を診断する。
–さまざまな局在の壊死とアポトーシスの重要性を評価します。
干ばつ壊死は、水分含有量の少ない臓器に特有であり、凝固可能なタンパク質が豊富です。 病因と関与する臓器に応じて、いくつかのタイプが知られています。 凝固壊死は、タンパク質の分解とそれに続く脱水の結果として起こります。 心筋、肝臓、腎臓、脾臓が最も影響を受ける臓器です。 通常、壊死は限局性です。 壊死の閃光は、それらの可視性の限界で小さいか、またはセンチメートルからセンチメートルまでの直径で大きくなる可能性があります。 壊死は、皮膚や粘膜の表面にも影響を与える可能性があります。
–萎縮の特徴的な形態学的特徴を形成不全、形成不全および形成不全から決定し、重要性を評価する 他の種類臓器および生物全体の機能のための萎縮。
伝統的に、細胞死の研究は壊死から始まりますが、アポトーシスは体の一般的な病理学的および生理学的プロセスのいくつかを伴い、時には調節するため、アポトーシスは確かにはるかに一般的です。
表在性壊死表在性壊死は侵食と呼ばれます。 プロセスが深くなる状況では、潰瘍が確立されます。 壊死の領域は黄色がかった灰色で、乾燥していて、輝きがありません。 壊死が発生して間もなく、患部の粘稠度は通常と変わらないが、徐々に緩くなる。 赤い地殻に代表される大きなフレアの周りに重要な反応ゾーンが形成されます。
この病変の設置につながる理由は、ビタミンEやセレンの欠乏など、さまざまです。 最も影響を受ける筋肉グループは、大腿筋、肩甲帯、横隔膜、および心筋です。 ガリナセアでは、腹部の筋肉のワックス状の壊死が損傷します。 巨視的には、筋肉は白、黄色、光沢のある、ワックス状の溝を示しています。 一貫性が遅く、後処理の剛性が低い。
壊死(ギリシャ語から。 ネクロス-死んだ)-病原性因子の影響下での生体内の細胞および組織の壊死、死。 このタイプの細胞死は遺伝的に制御されていません。
壊死の原因。 壊死を引き起こす要因:
-物理的(銃創、放射線、電気、低および 高温-凍傷と火傷);
脂肪壊死-脂肪組織の壊死。 生産メカニズムはさまざまです。 皮下脂肪組織の損傷は、特に胸骨で、長期の脱出を伴って発生します。 膵臓の壊死、膵臓の破裂から放出される酵素は、脂肪組織と相互作用します 腹腔; 白色の同心の成熟した病巣が形成され、周囲の組織によって十分に境界が定められています。
チャンスキリングは、特殊なタイプの凝固壊死です。 これは、細胞内で発生する微生物によって引き起こされる慢性疾患によるものです。 それはすべての組織と器官で発生します。 影響を受けた臓器には、牛乳と同様に、乾燥した、脂肪の多い、脂っこい、白灰色または黄色がかった塊の結節性またはびまん性の蓄積があります。
-毒(酸、アルカリ、重金属の塩、酵素、薬物、エチルアルコールなど);
-生物学的(細菌、ウイルス、原生動物など);
-アレルギー(エンド抗原およびエキソ抗原、例えば、感染性アレルギーおよび自己免疫疾患におけるフィブリノイド壊死、アルサス現象);
-血管(心臓発作-血管壊死);
湿性壊死は、組織の破壊が急速に起こり、影響を受けた組織が解凍される状況で発生します。 このタイプの壊死は、水分を保持し、凝固タンパク質が不足している組織構造に影響を及ぼします。 中枢神経系が最も頻繁に影響を受け、肉眼で見える病変は、軟化、および顕微鏡での軟化と呼ばれます。
あざや特定の寄生虫の幼虫の移動や脳梗塞によって引き起こされる外傷を伴う赤い発疹が連続して発生します。 壊死の領域では持続します たくさんの赤みがかった黒い色の血。 粗さは、神経にゆっくりと作用する要因の結果です。 サイトはゼラチン状の一貫性と灰色をしています。
-trophoneurotic(褥瘡、非治癒性潰瘍)。
病原性因子の作用機序に応じて、次のようなものがあります。
-直接壊死、因子の直接作用(外傷性、毒性および生物学的壊死)により、
-間接壊死これは、血管系および神経内分泌系(アレルギー性、血管性および栄養尿性壊死)を介して間接的に発生します。
壊死の進展と結果は、壊死領域のサイズと影響を受ける臓器によって異なります。 通常、壊死の発生の前後で、多くのファージ細胞が移動してデトリタスを除去します。 この段階の後、小さな発生の場合、その領域はほぼ完全に補充されるか、瘢痕が形成されます。 壊死の大きなフレアを完全に取り除くことはできず、葉の領域は結合組織に囲まれ、攻撃を形成します。
壊疽の設置につながる理由に応じて、それは知られています。 一次壊疽。 二次壊疽。 病変は特に筋肉で顕著であり、その領域は腫れ、触知可能で、赤黒で、独特の油臭があります。 乾燥壊疽は皮膚にあり、灌漑面積が不十分な物体が標的になります。 乾性壊疽の原因はさまざまです:機械的、毒性、細菌性。 皮膚の最も影響を受ける領域は、耳、尾、紋章、バービット、手足の四肢です。 乾燥壊疽のある皮膚は明らかに健康な茶色がかった茶色に限定されており、弾力性と感受性がありません。
壊死の形態学的兆候
壊死の前に壊死の期間があり、その形態学的基質はジストロフィー性変化である。
A.初期の変更: V 初期期間壊死細胞は形態学的に変化していません。 電子顕微鏡または組織化学によって認識できる変化が現れるまでに1〜3時間かかり、光学顕微鏡によって変化が検出されるまでに少なくとも6〜8時間かかる必要があります。 巨視的な変化はさらに後で発生します。 たとえば、心筋梗塞の患者が狭心症発作(心筋への血流が不十分な痛み)の発症から数分後に死亡した場合、剖検では壊死の構造的証拠は明らかになりません。 急性発作後2日目に死亡した場合、変化は明らかです。
進行性の脱水症のために、彼は羊皮紙になり、ボロボロになります。 その間、皮膚部分は皮膚として取り除かれます。 湿性壊疽は、肺、子宮、および腸に影響を与える高度に血管新生された臓器で発生します。 肺感染症は、異物や臓器の吸入、嚥下障害、誤嚥による肺炎を引き起こす薬液の誤用によって順次発生します。 子宮のガンマは、子宮への外傷性介入を伴う骨の折れる労働を通じて継続的に発達します。
B.組織化学的変化:細胞へのカルシウムイオンの流入は、不可逆的な損傷および壊死の形態学的兆候の出現と密接に関連しています。 正常細胞では、細胞内カルシウム濃度は細胞外液中の濃度の約0.001です。 この勾配は、カルシウムイオンを細胞外に活発に輸送する細胞膜によって維持されます。 虚血の結果として、または様々な毒性物質の影響下で細胞が損傷した場合、細胞内のカルシウム蓄積は、変化が不可逆的である場合にのみ観察されることが実験的に証明されています。 カルシウムは、エンドヌクレアーゼ(加水分解、DNA切断)、ホスホリパーゼ(膜破壊)、およびプロテアーゼ(破壊、細胞骨格の消化)を活性化します。 それらの活性の増加は、組織化学的方法によって検出されます。 レドックス酵素(コハク酸デヒドロゲナーゼなど)の活性は急激に低下するか、消失します。
腸では、壊疽は地形の変化の結果です。 混雑が最初に発生し、続いて逆流閉塞による静脈梗塞が発生します。 損傷した部分は黒っぽいまたは緑色で、ガスと内容物によって強く押され、腐った壊れやすい壁があります 外観、ホーンの匂い。
局在化に関係なく、壊疽領域は充血の領域を通して明らかに健康に制限されています、それは緩く、触診に忍び寄り、不快な臭いがあります。 乾燥した皮膚壊疽は審美的な結果を示し、動物は皮膚を除去した後に変形します。 湿った壊疽とガス状壊疽は、組織の分解に起因する生成物の動き(安全)により、動物の生命を危険にさらします。
B.カーネルの変更:細胞壊死の重要で明白な形態学的兆候の1つは、核の構造の変化です。 死んだ細胞のクロマチンは凝縮して大きな塊になります。 核は体積が減少し、しわが寄り、密度が高く、非常に好塩基性になります。つまり、ヘマトキシリンで濃い青色に染まります。 このプロセスは核濃縮(しわ)と呼ばれます。 次に、ピクノティック核は、リソソームデオキシリボヌクレアーゼの作用(核溶解)の結果として、多数の小さな好塩基性粒子(核崩壊)に破裂するか、溶解(溶解)する可能性があります。 その後、体積が増加し、ヘマトキシリンで弱く染色され、核の輪郭が徐々に失われます。 壊死が急速に進行すると、核濃縮段階なしに核が溶解します。
D.細胞質の変化:細胞が壊死した約6時間後、その細胞質は均質になり、好酸性になります。つまり、エオシンで染色するとピンクなどの強酸性染料で染色されます。 これは、光学顕微鏡で検出された最初の変化であり、細胞質タンパク質の凝固とリボソームの破壊(消失)の結果として発生します。 リボソームRNAは、正常な細胞質に好塩基性の色相を与えます。 心筋細胞の筋原線維などの特殊な細胞小器官が最初に消失します。 ミトコンドリアの腫れと細胞小器官の膜の破壊(破壊)は、細胞質の空胞化を引き起こします。 最後に、それ自体のリソソームから放出される酵素で細胞を消化すると、細胞溶解(自己消化)が引き起こされます。 したがって、タンパク質の凝固は細胞質で起こり、通常はそれらの凝固に置き換わります。
D.細胞間物質の変化間質物質と繊維構造の両方をカバーします。 ほとんどの場合、フィブリノイド壊死に特徴的な変化が発生します。コラーゲン、弾性および細網線維は、緻密で均質なピンク色の、時には好塩基性の塊に変わり、断片化、塊状の崩壊、または溶解を起こす可能性があります。 あまり一般的ではありませんが、浮腫、溶解、線維性構造の粘液が観察されます。これは、コリコート壊死の特徴です。
壊死の臨床的および形態学的形態
壊死は、さまざまな臨床的および形態学的変化によって現れます。 違いは、臓器や組織の構造的および機能的特徴、壊死の速度と種類、およびその発生の原因と発生条件によって異なります。 壊死の臨床的および形態学的形態の中で、凝固(乾性)壊死および凝固(湿性)壊死が区別される。
凝固(乾燥)壊死
このタイプの壊死では、死んだ細胞は数日間その形を保ちます。 核を欠く細胞は、凝固した均質なピンク色の細胞質の塊として現れます。
凝固壊死のメカニズムはよく理解されていません。 細胞質タンパク質の凝固により、リソソーム酵素の作用に耐性があり、その結果、液化が遅くなります。
凝固壊死は通常、タンパク質が豊富で体液が乏しい臓器、たとえば腎臓、心筋、副腎、脾臓で発生します。これは通常、不十分な循環と無酸素症、物理的、化学的、その他の損傷因子の作用の結果です。ウイルス感染を伴う、または細菌および非細菌起源の毒性物質の作用下での肝細胞の凝固壊死(図6.1)。 凝固壊死は、それとともに発生する死んだ領域が乾燥していて、密で、崩れていて、白または黄色であるという事実によって特徴付けられるので、乾燥とも呼ばれます。
凝固壊死には以下が含まれます:
A.心臓発作-血管(虚血性)壊死の一種 内臓(脳を除く)。 これは最も一般的なタイプの壊死です。
B.乾酪壊死結核、梅毒、ハンセン病、およびリンパ肉芽腫症を発症します。 特定の感染性肉芽腫に最も多く見られるため、特定とも呼ばれます。 内臓では、白っぽい黄色の組織の乾燥した崩れかけた限られた領域が明らかになります。 梅毒肉芽腫では、非常に多くの場合、そのような領域はもろくはありませんが、アラビアの接着剤を連想させるペースト状です。 これは、混合(つまり、細胞外および細胞内)タイプの壊死であり、実質と間質(細胞と繊維の両方)の両方が同時に死にます。 顕微鏡的には、そのような組織領域は、ヘマトキシリンとエオシンで染色された構造のない均質なピンクのように見え、核クロマチン(核崩壊)の塊がはっきりと見えます。
B.ワキシーまたはゼンカー壊死(腸チフスとチフス、コレラなどの重度の感染症を伴う、しばしば前腹壁と大腿部の内転筋の筋肉壊死);
D.フィブリノイド壊死-壊死の種類 結合組織フィブリノイド腫脹の結果として。 フィブリノイド壊死は、アレルギー性疾患および自己免疫疾患(例、リウマチ、関節リウマチ、全身性エリテマトーデス)で見られます。 コラーゲン繊維と中膜の平滑筋が最もひどく損傷しています。 血管。 細動脈のフィブリノイド壊死は、悪性高血圧症で観察されます。 この壊死は、正常なコラーゲン線維構造の喪失と、顕微鏡でフィブリンを模倣する均質で明るいピンク色の壊死物質の蓄積を特徴としています。 「フィブリノイド」は「フィブリノイド」とは異なることに注意してください。後者は、血液凝固や炎症などのフィブリンの蓄積を指します。 フィブリノイド壊死の領域には、さまざまな量の免疫グロブリンと補体、アルブミン、コラーゲンとフィブリンの分解産物が含まれています。
D.脂肪壊死:
1.酵素的脂肪壊死:脂肪壊死は、膵臓酵素が管から周囲の組織に漏れるときに、急性膵炎および膵臓損傷で最も一般的に発生します。 膵リパーゼは脂肪細胞のトリグリセリドに作用し、それらをグリセロールと脂肪酸に分解し、血漿カルシウムイオンと相互作用してカルシウム石鹸を形成します。 同時に、不透明な白い(チョークのような)プラークと結節(脂肪壊死)が膵臓の周囲の脂肪組織に現れます。
膵炎では、リパーゼが血流に入り、続いて広範囲に分布し、体の多くの部分に脂肪壊死を引き起こす可能性があります。 最も一般的に損傷を受けた皮下脂肪と骨髄。
2.非酵素的脂肪壊死:非酵素的脂肪壊死は、乳腺、皮下脂肪組織、および腹腔で観察されます。 ほとんどの患者は外傷の病歴があります。 非酵素的脂肪壊死は、外傷が根本的な原因として特定されていない場合でも、外傷性脂肪壊死とも呼ばれます。 非酵素的脂肪壊死は、泡沫状の細胞質、好中球、およびリンパ球を伴う多数のマクロファージの存在を特徴とする炎症反応を引き起こします。 これに続いて線維症が起こり、このプロセスは腫瘍と区別するのが難しい場合があります。
E.壊疽(ギリシャ語から。 ガングレイナ-火):これは、外部環境と通信し、その影響下で変化する組織の壊死です。 「壊疽」という用語は、組織壊死がさまざまな重症度の二次細菌感染によって複雑になることが多い、または外部環境と接触して二次変化を起こす臨床的および形態学的状態を指すために広く使用されています。 乾いた、湿った、ガス壊疽と床ずれがあります。
1.乾性壊疽-これは、外部環境と接触している組織の壊死であり、微生物の関与なしに進行します。 乾性壊疽は、虚血性凝固組織壊死の結果として四肢に最も頻繁に発生します。 壊死組織は黒く乾燥しており、隣接する生存組織と明確に区別されています。 健康な組織との境界では、境界の炎症が発生します。 色の変化は、硫化水素の存在下でのヘモグロビン生成色素の硫化鉄への変換によるものです。 例は乾性壊疽です:
アテローム性動脈硬化症およびその動脈の血栓症(アテローム性動脈硬化症性壊疽)を伴う四肢、閉塞性動脈内膜炎;
凍傷または火傷を伴う;
レイノー病または振動病の指;
チフスやその他の感染症のある皮膚。
治療は以下で構成されます 外科的切除死んだ組織、境界線はガイドとして機能します。
2.湿性壊疽:重度の細菌感染症の壊死組織の変化に重なる結果として発症します。 微生物酵素の作用下で、二次凝集が起こります。 細胞自体では形成されないが、外部から浸透する酵素による細胞溶解は、ヘテロリシスと呼ばれます。 微生物の種類は壊疽の局在に依存します。 湿性壊疽は通常、水分が豊富な組織で発生します。 それは四肢で発生する可能性がありますが、肺炎(インフルエンザ、はしか)の合併症として肺で、腸間膜動脈の閉塞(血栓症、塞栓症)を伴う腸などの内臓でより頻繁に発生する可能性があります。 感染症(通常はしか)によって衰弱した子供は、頬の軟部組織である会陰の湿った壊疽を発症する可能性があります。これは、ノマ(ギリシャ語のノメ-水がん)と呼ばれます。 急性炎症細菌の増殖により、壊死領域が浮腫性で赤黒になり、死んだ組織が広範囲に液化されます。 湿性壊疽では、壊死性炎症が広がる可能性がありますが、隣接する健康な組織から明確に区別されていないため、外科的に治療することは困難です。 バクテリアの活力の結果として、特定の匂いが発生します。 非常に高い死亡率。
3.ガス壊疽:ガス壊疽は、傷が嫌気性菌に感染したときに発生します。 ウェルシュ菌およびこのグループの他の微生物。 それは、細菌の酵素活性の結果としての広範な組織壊死およびガス形成を特徴とする。 主な症状は湿性壊疽に似ていますが、組織内にガスが追加されています。 捻髪音(触診でのパチパチという現象)は、ガス壊疽の一般的な臨床症状です。 死亡率も非常に高いです。
4.褥瘡(褥瘡):壊疽の一種として、床ずれが分離されます-床と骨の間で圧迫を受ける体の表面部分(皮膚、軟組織)の壊死。 したがって、床ずれは、仙骨の領域、椎骨の棘突起、および大腿骨の大転子にしばしば現れます。 その起源により、これは、血管および神経が圧迫されるため、栄養尿性壊死であり、心血管、腫瘍性、感染性または神経性疾患に苦しむ重篤な患者の組織栄養障害を悪化させる。
コリキューション(ウェット)壊死
コリキューション(ウェット)壊死は、死んだ組織の融合を特徴としています。 それは、タンパク質が比較的少なく、体液が豊富な組織で発生します。そこでは、加水分解プロセスに適した条件があります。 細胞溶解は、それ自体の酵素の作用(自己消化)の結果として起こります。 湿性液化壊死の典型的な例は、脳の灰色の軟化(虚血性梗塞)の焦点です。
主な肉眼的兆候は常に病変内の脳組織の弾力性の低下であるため、脳梗塞はしばしば軟化と呼ばれます。 初日は、チアノーゼ性の色合いのはっきりと限定された領域で表され、手触りが柔らかいです。 初日の終わりまでに、焦点はより明確になり、青ざめます。 次の日には、この領域の脳の物質はさらにたるんで、黄色がかった色になり、時には緑がかった色合いになります。 最初の数週間は、浮腫のために脳の体積がわずかに増加します。 1〜1.5か月後。 梗塞の部位では、濁った液体と破片を含むかなり明確に定義された空洞が形成されます。 心臓発作の正確なタイミングを決定することは、外観だけでなく、組織像においても非常に困難です。
微視的には、脳組織は均質で、構造がなく、弱く ピンク色ヘマトキシリンおよびエオシンで染色した場合。 死んだ組織の吸収は、脂肪顆粒球のように見えるマクロファージによって行われます。
壊死の臨床症状
全身症状:壊死では、通常、発熱(壊死細胞および組織からの発熱性物質の放出による)および好中球性白血球増加症(急性炎症反応の存在による-境界炎症)が現れます。 壊死細胞内容物の放出:壊死細胞の細胞質内容物の放出された成分(例えば、酵素)は血流に入り、そこでそれらの存在は壊死の局在化の診断である。 これらの酵素は、さまざまな実験方法で検出できます(表6.1)。 酵素の出現の特異性は、体のさまざまな組織における酵素の主な局在に依存します。 たとえば、クレアチンキナーゼのMBアイソザイムのレベルの増加は、この酵素が心筋細胞にのみ見られるため、心筋壊死の特徴です。 アスパラギン酸アミノトランスフェラーゼ(AST)のレベルの上昇は、この酵素が心筋だけでなく肝臓や他の組織にも見られるため、特異性が低くなります。 トランスアミナーゼの出現は、肝細胞壊死の特徴です。
局所症状:胃腸管の粘膜の潰瘍は、出血または出血(例えば、出血性消化性潰瘍)によって複雑になる可能性があります。 浮腫の結果としての組織体積の増加は、限られた空間(例えば、虚血性または出血性壊死を伴う頭蓋腔内)での圧力の深刻な増加につながる可能性があります。
機能不全:壊死は、臓器の機能障害、例えば、心筋の広範な壊死(梗塞)の結果としての急性心不全(急性冠状動脈性心臓病)の発生につながる。 臨床症状の重症度は、影響を受ける組織の種類、総量に対する体積、および残りの生体組織の機能の維持に依存します。 一方の腎臓の壊死は、腎臓全体が失われた場合でも、もう一方の腎臓がその喪失を補うことができるため、腎不全を引き起こしません。 しかし、大脳皮質の対応するセクションの小さな領域の壊死は、対応する筋肉群の麻痺につながります。
壊死の結果。壊死は不可逆過程です。 比較的好ましい結果で、反応性炎症は死んだ組織の周りで起こり、それは死んだ組織を区切る。 このような炎症は境界と呼ばれ、境界のゾーンは境界ゾーンと呼ばれます。 このゾーンでは、血管が拡張し、多発性浮腫が発生し、多数の白血球が出現し、加水分解酵素を放出して壊死塊を溶かします。 壊死塊はマクロファージに吸収されます。 これに続いて、結合組織の細胞が増殖し、壊死の領域を置き換えるか、または大きくなります。 死んだ塊を結合組織に置き換えるとき、彼らは彼らの組織について話します。 このような場合の壊死部位に瘢痕(心臓発作部位の瘢痕)が形成されます。 結合組織による壊死部位の汚れは、そのカプセル化につながります。 カルシウム塩は、乾性壊死の際に死んだ塊に、そして組織化された壊死の中心に沈着する可能性があります。 この場合、壊死の焦点の石灰化(石化)が発生します。 場合によっては、壊死の領域では、骨の形成が認められます-骨化。 組織の残骸の吸収と莢膜の形成により、通常は湿性壊死で発生し、ほとんどの場合脳で発生し、壊死部位に空洞嚢胞が現れます。
壊死の好ましくない結果は、壊死の焦点の化膿性(敗血症)融解である。 隔離とは、自己消化を受けず、結合組織に置き換わらず、生体組織の間に自由に配置される死んだ組織の領域の形成です。 隔離は通常、骨髄の炎症を伴う骨で発生します-骨髄炎。 そのような隔離器の周りに、隔離カプセルと膿で満たされた空洞が形成されます。 非常に多くの場合、隔離者は、完全に割り当てられた後にのみ閉じられる瘻孔を通して空洞を離れます。 一種の隔離-切断-指の端の拒絶。
壊死の意味。それはその本質によって決定されます-「局所死」と機能からのそのようなゾーンの除外、したがって、重要な器官、特にそれらの広い領域の壊死はしばしば死につながります。 そのようなものは、心筋梗塞、脳の虚血性壊死、腎臓の皮質物質の壊死、進行性肝壊死、急性膵炎、膵臓壊死を合併している。 多くの場合、組織の壊死が原因です 重篤な合併症多くの疾患(脊髄軟化症を伴う心臓破裂、出血性および虚血性脳卒中を伴う麻痺、大規模な床ずれによる感染症、組織崩壊産物の体への曝露による中毒、例えば、四肢の壊疽など)。 壊死の臨床症状は非常に多様である可能性があります。 脳または心筋の壊死の領域で発生する異常な電気的活動は、てんかん発作または心不整脈につながる可能性があります。 壊死した腸の蠕動運動の違反は、機能的(動的)腸閉塞を引き起こす可能性があります。 壊死組織への出血、例えば、肺壊死を伴う喀血(喀血)がしばしば観察されます。
体内の細胞死は、壊死とアポトーシスの2つの方法で発生する可能性があります。 アポトーシスは、細胞自体がその死の過程に積極的に関与する細胞死の一種です。 セルは自己破壊します。 アポトーシスは、壊死とは異なり、活発なプロセスであり、病因因子への曝露後、特定の遺伝子の活性化、タンパク質、酵素の合成を伴う、遺伝的にプログラムされた反応のカスケードが引き起こされ、細胞の効果的かつ迅速な除去につながります組織から。
アポトーシスの理由:
1.胚発生の間、アポトーシスはさまざまな組織の原基の破壊と器官の形成に重要な役割を果たします。
2.アポトーシスは、その発達サイクルを完了した老化細胞、例えば、サイトカインの供給を使い果たしたリンパ球を経験します。
3.成長中の組織では、娘細胞の特定の部分がアポトーシスを起こします。 死にかけている細胞の割合は、全身ホルモンと局所ホルモンによって調節することができます。
4.アポトーシスの原因は、損傷因子の弱い影響である可能性があり、強度が高くなると、壊死(低酸素、電離放射線、毒素など)につながる可能性があります。
アポトーシスの病因:
修復システムで修復できない核にDNA損傷が発生すると、細胞はアポトーシスを起こします。 このプロセスは、p53遺伝子によってコードされるタンパク質によって監視されます。 p53タンパク質の作用下でDNA欠損を除去することが不可能な場合、アポトーシスプログラムが活性化されます。
多くの細胞には受容体があり、その影響がアポトーシスの活性化を引き起こします。 最もよく研究されているのは、リンパ球に見られるFas受容体と、多くの細胞に見られる腫瘍壊死因子-α(TNF-α)受容体です。 これらの受容体は、自己反応性リンパ球の除去およびフィードバック方式での細胞集団のサイズの一定性の調節において重要な役割を果たします。
抗炎症性サイトカイン、ステロイドホルモン、一酸化窒素(NO)、フリーラジカルなど、さまざまな代謝物やホルモンがアポトーシスを活性化する可能性があります。
細胞のアポトーシスは、組織に酸素が不足しているときに活性化されます。 その活性化の理由は、フリーラジカルの作用、DNA修復のエネルギー依存プロセスの破壊などである可能性があります。
アポトーシスは、細胞間マトリックス、基底膜、または隣接する細胞との接触を失った細胞を経験します。 腫瘍細胞におけるアポトーシスのこのメカニズムの喪失は、転移する能力の出現につながります。
一部のウイルスタンパク質は、ウイルスが感染細胞内で自己組織化した後、細胞アポトーシスを活性化する可能性があります。 隣接する細胞によるアポトーシス小体の吸収は、ウイルスによるそれらの感染につながります。 AIDSウイルスは、表面にCD4受容体を持つ非感染細胞のアポトーシスを活性化することもできます。
アポトーシスを防ぐ要因もあります。 性ホルモンや炎症性サイトカインなどの多くの代謝物やホルモンは、アポトーシスを遅らせる可能性があります。 アポトーシスは、細胞死のメカニズムの欠陥によって劇的に遅くなる可能性があります。たとえば、p53遺伝子の変異や、アポトーシスを阻害する遺伝子(bcl-2)の活性化などです。 多くのウイルスは、自身の構造タンパク質の合成期間中、自身のDNAを細胞ゲノムに組み込んだ後、アポトーシスを阻害する能力を持っています。
アポトーシスの形態学的症状
壊死(壊死)-細胞、組織、臓器、または体の一部の壊死。病因。 組織壊死は、打撲傷、挫滅、圧迫、火傷、凍傷、毒物、毒素、電流、放射エネルギー、酸、アルカリ、嫌気性微生物、内分泌および植物への曝露で発生します 神経系。 凝固(乾性)壊死と凝固(湿性)壊死を区別します。 乾性壊死は次の場合に発生します 熱傷、電気的傷害、重金属の塩、ホルムアルデヒド、毒素、酸への暴露。
凝固壊死(壊死凝固em)は、臓器や組織の壊死であり、凝固、圧縮、乾燥、および組織タンパク質の凝固塊への変換(壊死caseosd)の結果として発生します。 組織の壊死は、血流の停止と利用可能な水分の活発な浸出に関連しています。 影響を受ける組織は、乾燥した、もろい、暗褐色または灰黄色で、明確な境界線があります。 消耗、失血、感染症、寄生虫症により、死んだ基質の拒絶反応が遅れ、再生過程が遅くなり、体の保護機能が低下し、動物の全身状態が急激に悪化します。 死んだ組織の拒絶部位では、潰瘍が発生し、化膿性プロセスの発生により膿瘍が形成され、開腹時に瘻孔が形成されます。 乾性壊死は、新生児の乳房、脾臓、腎臓、臍帯断端でより頻繁に観察されます。
Colliquation necrosis(necrosis colliquationem)は、死んだ組織の腫れ、軟化、液化を特徴とし、腐敗臭のある形のない液化した灰色の塊を形成します。 死んだ組織は水分が過剰であるため、境界線はゆっくりと形成され、コロイドの親水性のために環境への戻りが遅くなります。 湿性壊死は、壊死桿症、足腐れ、臍炎、実質器官の血管の血栓症で記録されます。 壊疽はそれ自体で発生する可能性があり、またはその発達の前に組織壊死が起こります。 骨、腱、靭帯、筋膜、腱膜の壊死は一般に壊死と呼ばれ、皮膚、粘膜、筋肉の壊死は壊疽と呼ばれます。